-
饮用水中含有砷会导致砷中毒,水体中溶解的砷主要以As( Ⅲ)亚砷酸盐和As(V)砷酸盐形式存在。
(1)砷与磷为同一主族元素,磷的原子结构示意图为___________________。
(2)根据元素周期律,下列说法正确的是____________________(填字母代号)。
a.最高价氧化物对应水化物的酸性:S>P>As b. 原子半径:S>P>As c.非金属性:S>P>As
(3)关于地下水中砷的来源有多种假设,其中一种认为是富含砷的黄铁矿(FeS2)被氧化为Fe(OH)3,同时生成SO42-,导致砷脱离矿体进入地下水。FeS2被O2氧化的离子方程式为_________________________。
(4)去除水体中的砷,可先将As(Ⅲ )转化为As(V),选用NaClO可实现该转化。
已知:投料前水样pH=5.81,0.1 mol/L NaClO溶液pH=10.5,溶液中起氧化作用的物质是次氯酸。
研究NaClO投加量对As(Ⅲ)氧化率的影响得到如下结果:
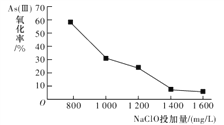
产生此结果的原因是_________________________。
(5)强阴离子交换柱可以吸附以阴离子形式存在的As(V),从而达到去除As的目的。
已知:一定条件下,As(V)的存在形式如下表所示:
| pH | <2 | 2~7 | 7~11 | 11~14 |
| 存在形式 | H3AsO4 | H2AsO4- | HAsO42- | HAsO42-、AsO43- |
pH=6时,NaClO氧化亚砷酸(H3AsO3)的离子方程式是_____________________。
-
下列说法错误的是( )
A.含有磷元素生活污水排入江河易引起水体富营养化,造成藻类过度繁殖影响水质
B.“食用色素”、“亚硝酸盐”在某些食品添加剂中允许有,符合限量不会引起中毒
C.航天服主要成分是由碳化硅、陶瓷和碳纤维复合而成的,是一种有机材料
D.实行“汽车下乡”政策、大力推广使用家用小轿车不利于节能减排
-
自然界水体中的碳元素主要以碳酸盐、碳酸氢盐和有机物形式存在。水体中有机物含量是水质的重要指标,常用总有机碳衡量(总有机碳= )。某学生兴趣小组用如下实验方法测定采集水样的总有机碳。
)。某学生兴趣小组用如下实验方法测定采集水样的总有机碳。
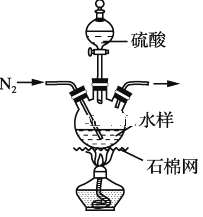
步骤1:量取50 mL水样,加入足量硫酸,加热,通N2,并维持一段时间(装置如图,夹持类仪器省略)。
步骤2:再向水样中加入过量的K2Cr2O7溶液(可将有机物中的碳元素氧化成CO2),加热,充分反应,生成的CO2完全被100mL 0.206 mol·L-1的Ba(OH)2溶液吸收。
步骤3:将吸收CO2后的浊液过滤并洗涤沉淀,再将洗涤得到的滤液与原滤液合并,加水配制成500mL溶液。量取25.00mL溶液于锥形瓶中,加入几滴酚酞试剂,并滴加0.05mol·L-1的H2C2O4溶液,发生反应:Ba(OH)2+H2C2O4===BaC2O4↓+2H2O 恰好完全反应时,共消耗H2C2O4溶液20.00 mL。
(1)步骤1的目的是____。
(2)用H2C2O4溶液滴定至终点时,溶液颜色变化是____。
(3)计算水样的总有机碳(以mg·L-1表示),并写出计算过程。____
-
人体正常的血红蛋白应含Fe2+。若误食外表与食盐相近的亚硝酸盐,则导致血红蛋白中的Fe2+转化成Fe3 +而中毒,服用维生素C可解除亚硝酸盐中毒,下列叙述中正确的是:
A.亚硝酸盐是还原剂
B.维生素C是还原剂
C.维生素C是氧化剂
D.亚硝酸盐被氧化
-
人体正常的血红蛋白应含Fe2+。若误食外表与食盐相近的亚硝酸盐,则导致血红蛋白中的Fe2+转化成Fe3 +而中毒,服用维生素C可解除亚硝酸盐中毒,下列叙述中正确的是:
A.亚硝酸盐是还原剂
B.维生素C是还原剂
C.维生素C是氧化剂
D.亚硝酸盐被氧化
-
人体正常的血红蛋白中应含 。若误食亚硝酸盐,则导致血红蛋白中
。若误食亚硝酸盐,则导致血红蛋白中 转化为高铁血红蛋白而中毒。服用维生素C可解除亚硝酸盐中毒。下列叙述中正确的是
转化为高铁血红蛋白而中毒。服用维生素C可解除亚硝酸盐中毒。下列叙述中正确的是
A.亚硝酸盐是还原剂 B.维生素C是氧化剂
C.维生素C将 还原为
还原为 D.亚硝酸盐被氧化
D.亚硝酸盐被氧化
-
生活污水和某些工业废水中的含氮化合物经转化最终会以硝酸盐的形式进入水体,若大量排放会造成水体富营养化。用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为环境修复研究的热点之一。Fe还原水体中NO3-的反应原理如右图所示。
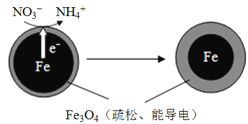
(1)下列说法属于水体污染的危害的有______(填字母)。
a.加剧水资源短缺 b.危害人体健康
(2)NO3-中氮元素的化合价为______。
(3)Fe在反应过程中发生的是______(选填“氧化”或“还原”)反应。
(4)将足量铁粉投入某水体样本中,经一段时间后,测得溶液中离子浓度的有关数据如下(其他离子忽略不计)。
| 离子 | Na+ | H+ | NO3− | NH4+ | Fe2+ |
| 浓度/(mol·L−1) | 5.0×10−2 | 5.0×10−2 | 6.4×10−1 | y | 2.4×10−1 |
表中y =______。
-
人体血红蛋白中含有 离子,如果误食亚硝酸盐,会使人中毒,因为亚硝酸盐会使
离子,如果误食亚硝酸盐,会使人中毒,因为亚硝酸盐会使 离子转变成
离子转变成 离子,生成高铁血红蛋白而丧失与
离子,生成高铁血红蛋白而丧失与 结合的能力。服用维生素C可缓解亚硝酸盐的中毒,这说明维生素C具有( )
结合的能力。服用维生素C可缓解亚硝酸盐的中毒,这说明维生素C具有( )
A. 酸性 B. 碱性 C. 氧化性 D. 还原性
-
[s1] 人体血红蛋白中含有Fe3+离子,如果误食亚硝酸盐,会使人中毒,因为亚硝酸盐会使Fe2+离子转变成为Fe3+离子,生成高铁血红蛋白而丧失与O2结合的 能力,服用维生素C可以缓解亚硝酸盐中毒,这说明维生素C具有……………………………………………………( )
A.酸性 B.碱性 C.氧化性 D.还原性
[s1]33.
-
人体血红蛋白中含有Fe3+离子,如果误食亚硝酸盐,会使人中毒,因为亚硝酸盐会使Fe2+离子转变成为Fe3+离子,生成高铁血红蛋白而丧失与O2结合的能力,服用维生素C可以缓解亚硝酸盐中毒,这说明维生素C具有( )
A.酸性 B.碱性 C.氧化性 D.还原性

 )。某学生兴趣小组用如下实验方法测定采集水样的总有机碳。
)。某学生兴趣小组用如下实验方法测定采集水样的总有机碳。
