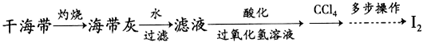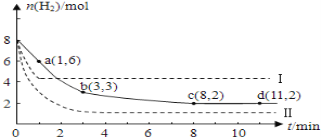-
利用海洋资源可以获得很多物质。如从海水中可以得到食盐等许多化工原料,可以通过蒸馏获得淡水,从海洋植物中提取碘等。
(一)从海水得到的粗盐中常含有杂质需要分离提纯,在除去悬浮物和泥沙之后,要用以下试剂①盐酸、②Na2CO3、③NaOH、④BaCl2来除去食盐水中的Ca2+、 Mg2+、SO42-。
(1)为有效除去Ca2+、 Mg2+、SO42-,加入试剂的合理顺序为___________。
a.先加 NaOH,后加Na2CO3,再加 BaCl2
b.先加NaOH,后加BaCl2,再加Na2CO3
C.先加BaCl2,后加NaOH,再加Na2CO3
(2)加入Na2CO3过程中发生反应的离子方程式为_______________________。
(3)判断试剂BaCl2己经足量的方法是_______________________。
(二)海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海带中提取碘的流程如下:
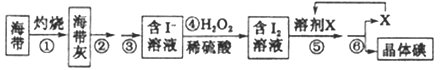
(1)实验时灼烧海带应在___________(填仪器名称)内进行。
(2)步骤④中反应的离子方程式是_______________。
(3)步骤⑤的实验操作为____________,应选用的一种溶剂X可以是____________。
a.苯、酒精 b.四氯化碳、苯 c.汽油、酒精
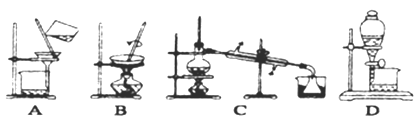
(4)步骤⑥的实验操作应选用下图中的_____________。
-
利用海洋资源可以获得很多物质 如从海水中可以得到食盐等许多化工原料,可以通过蒸馏获得淡水,从海洋植物中提取碘等.
如从海水中可以得到食盐等许多化工原料,可以通过蒸馏获得淡水,从海洋植物中提取碘等.
 一
一 从海水得到的粗盐中常含有杂质需要分离提纯,在除去悬浮物和泥沙之后,要用以下试剂①盐酸、②Na2 CO3、③NaOH、④BaCl2来除去食盐水中的
从海水得到的粗盐中常含有杂质需要分离提纯,在除去悬浮物和泥沙之后,要用以下试剂①盐酸、②Na2 CO3、③NaOH、④BaCl2来除去食盐水中的 、
、 、
、 .
.
(1)为有效除去Ca2+、Mg2+、SO42-,加入试剂的合理顺序为______
a.先加 NaOH,后加Na2 CO3,再加 BaCl2
b.先加NaOH,后加BaCl2,再加Na2 CO3
C.先加BaCl2,后加NaOH,再加Na2 CO3
(2)判断试剂BaCl2己经足量的方法是______________________。
 二
二 海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在
海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在 实验室里从海带中提取碘的流程如下:
实验室里从海带中提取碘的流程如下:
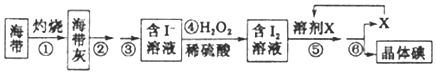
(1)实验时灼烧海带应在______________(填仪器名称)内进行
(2)步骤④中反应的离子方程式是_______________________________。
(3)步骤⑤的实验操作为____________,应选用的一种溶剂X可以是_____________。
a.苯、酒精 b.四氯化碳、苯 c.汽油、酒精
(4)步骤⑥的实验操作应选用如图中的______。
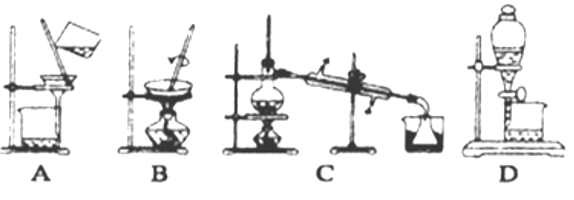
-
从自然资源中获得以下物质可以不用化学方法的是( )
A.用植物种子提取油
B.用海水制取粗食盐和淡水
C.用可燃冰制取甲烷气体燃料
D.用辉铜矿(主要成分为Cu2S)冶炼金属铜
-
海洋资源的利用具有广阔前景。
(1)无需经过化学变化就能从海水中获得的物质是________(填序号)
A.Cl2 B.淡水 C.烧碱 D.食盐
(2)从海水中提取溴的主要步骤是向浓缩的海水中通入氯气,将溴离子氧化,该反应的离子方程式是________________________。
(3)下图是从海水中提取镁的简单流程。
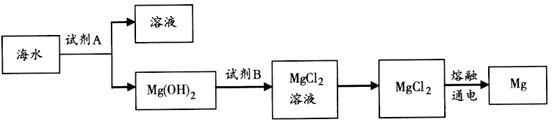
①工业上常用于沉淀Mg2+的试剂A是________, 转化为MgCl2的离子方程式是________________________________。
转化为MgCl2的离子方程式是________________________________。
②由无水MgCl2制取Mg的化学方程式是________________________。
(4)海带灰中富含以I-形式存在的碘元素。实验室提取I2的途径如下所示:
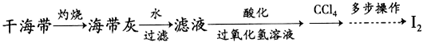
①灼烧海带至灰烬时所用的主要仪器名称是________________。
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式____________________________。
反应结束后,再加入CCl4作萃取剂,振荡、静置,可以观察到CCl4层呈________色。
-
海洋资源的利用具有广阔前景。
(1)无需经过化学变化就能从海水中获得的物质是________(填序号)
A.Cl2 B.淡水 C.烧碱 D.食盐
(2)从海水中提取溴的主要步骤是向浓缩的海水中通入氯气,将溴离子氧化,该反应的离子方程式是________________________。
(3)下图是从海水中提取镁的简单流程。

①工业上常用于沉淀Mg2+的试剂A是________,转Mg(OH)2化为MgCl2的离子方程式是________________________________。
②由无水MgCl2制取Mg的化学方程式是________________________。
(4)海带灰中富含以I-形式存在的碘元素。实验室提取I2的途径如下所示:

①灼烧海带至灰烬时所用的主要仪器名称是________________。
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式_______________________。
反应结束后,再加入CCl4作萃取剂,振荡、静置,可以观察到CCl4层呈________色。
-
海洋资源的利用具有广阔前景。
(1)无需经过化学变化就能从海水中获得的物质是________(填序号)。
A.Cl2 B.淡水 C.烧碱 D.食盐
(2)从海水中提取溴的主要步骤是向浓缩的海水中通入Cl2,将Br-氧化,该反应的离子方程式是____。
(3)下图是从海水中提取镁的简单流程。

①工业上常用于沉淀Mg2+的试剂A是________,转Mg(OH)2化为MgCl2的离子方程式是____________。
②由无水MgCl2制取Mg的化学方程式是________________________。
(4)海带灰中富含以I-形式存在的碘元素。实验室提取I2的途径如下所示:

①灼烧海带时所用的主要仪器名称是________________。
②向酸化的滤液中加H2O2溶液,写出该反应的离子方程式_______________________。
反应结束后,再加入CCl4作萃取剂,振荡、静置,可以观察到CCl4层呈________色。
-
海洋资源的利用具有广阔前景。
(1)无需经过化学变化就能从海水中获得的物质是________(填序号)。
A.Cl2 B.淡水 C.烧碱 D.食盐
(2)从海水中提取溴的主要步骤是向浓缩的海水中通入Cl2,将Br-氧化,该反应的离子方程式是____。
(3)下图是从海水中提取镁的简单流程。
①工业上常用于沉淀Mg2+的试剂A是________,转Mg(OH)2化为MgCl2的离子方程式是____________。
②由无水MgCl2制取Mg的化学方程式是________________________。
(4)海带灰中富含以I-形式存在的碘元素。实验室提取I2的途径如下所示:

①灼烧海带时所用的主要仪器名称是________________。
②向酸化的滤液中加H2O2溶液,写出该反应的离子方程式_______________________。
反应结束后,再加入CCl4作萃取剂,振荡、静置,可以观察到CCl4层呈________色。
-
海洋资源的利用具有广阔前景。
(1)无需经过化学变化就能从海水中获得的物质是(______)(填序号)
A.Cl2 B.淡水 C.烧碱 D.食盐
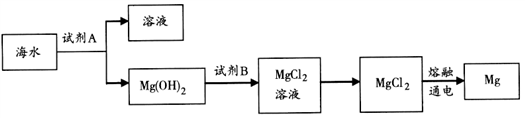
(2)下图是从海水中提取镁的简单流程。

①操作A是 _______________________。
②无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为____________________________ 。
③海水提镁的过程,为什么要将海水中的氯化镁转变为氢氧化镁,再转变为氯化镁? _____________________________________________ 。
(3)海带灰中富含以I-形式存在的碘元素。实验室提取I2的途径如下所示:

①灼烧海带至灰烬时所用的主要仪器名称是(________)(填序号)
a.坩埚 b.试管 c.蒸发皿 d.烧杯
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式________________________________。
③用CCl4提取碘时除了用CCl4还可以选用的试剂是(________)(填字母序号)
a.苯 b.乙醇 c.乙酸
④为检验用CCl4提取碘后的水溶液中是否还含有碘单质。请写出该实验的实验步骤、现象及结论:________。
(4)利用海底的“可燃冰”制作的燃料电池的总反应式为CH4+2O2+2KOH = K2CO3+3H2O,则该燃料电池的负极的电极反应为__________________。
(5)海底的煤经综合利用开发的副产物CO2能生产甲醇燃料,其反应的方程式为:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。某科学实验将6 mol CO2和8 mol H2充入2 L的密闭容器中,测得H2的物质的量随时间变化如图实线所示。a,b,c,d括号内数据表示坐标。
CH3OH(g)+H2O(g)。某科学实验将6 mol CO2和8 mol H2充入2 L的密闭容器中,测得H2的物质的量随时间变化如图实线所示。a,b,c,d括号内数据表示坐标。
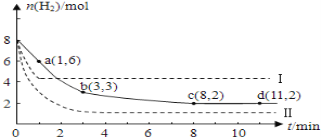
①a点正反应速率_________(填“大于、等于或小于”)a点逆反应速率。
②平衡时CO2的物质的量浓度是___________mol/L。
③能够说明该反应达到化学平衡状态的标志是_______(双选)。
A.单位时间内消耗1molCO2,同时生成3mol H2 B.混合气体的密度不随时间变化
C.CH3OH、H2的浓度不再随时间变化 D.CH3OH和H2O浓度相等
-
二十一世纪被称为海洋世纪,许多国家十分重视海水资源的综合利用。不需要化学变化就能够从海水中获得的物质是
A.氯、溴、碘 B.钠、镁、铝
C.烧碱、氢气 D.食盐、淡水
-
海水占地球总储水量的97.2%。若把海水淡化和化工生产结合起来,既可以解决淡水资源缺乏的问题,又可以充分利用海洋资源。
(1)目前国际上实用的“海水淡化”主要技术之一是蒸馏法。蒸馏法是将海水变成蒸汽,蒸汽经过冷却而得高纯度淡水,由此可判断蒸馏法是____________________(填物理变化、化学变化);
(2)工业上利用电解饱和食盐水可制得重要化工产品,又称为“氯碱工业”。电解饱和食盐水的化学方程式为___________________________________________;
(3)实验室用MnO2和浓盐酸为原料制备氯气,该反应的化学方程式为_____________,尾气处理的化学方程式为_______________________________________。工业上制备漂白粉的化学方程式________________________________________。
(4)将实验室制的氯气配成新制的氯水含有多种微粒,试用化学方程式解释下列现象。
①将氯水滴加紫色石蕊溶液中,先变红后褪色________________________________。
②将氯水滴入硝酸银溶液中,有白色沉淀生成___________________________。