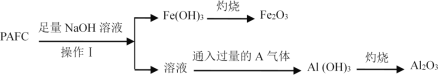-
一种新型高效净水剂PAFC(聚合氯化铁铝[AlFe(OH)nC16-n]m),广泛用于日常生活用水和工业污水的处理。某化工厂欲以工业生产废料(金属铁、铝及其氧化物)为原料制取PAFC,设计生产流程如下:
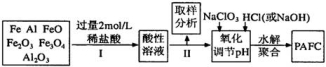
请回答下列问题:
(1)用l0 mol/L的浓盐酸配制2mol/L的稀盐酸,所用玻璃仪器除量筒和玻璃棒外,还有 。
A.容量瓶 B.烧杯 C.烧瓶 D.胶头滴管
(2)下列关于PAFC的说法中正确的有( )
A.PAFC是一种无机高分子化合物
B.PAFC中Fe显+2价
C.PAFC溶于水电离出OH—,是碱
D.PAFC在强酸性和强碱性溶液中均不能稳定存 在
在
(3)步骤Ⅱ中取样分析的目的是( )
A.测定溶液中Fe2+与Fe3+的含量比
B.测定原料是否完全溶解
C.测定溶液中Fe2+的含量,以确定加入NaClO3的量
D.测定溶液中Al3+的含量
(4)写出向溶液中加入NaClO3时,发生反应的离子方程式为______________________。
(5)该化工厂的化验室为测定产品PAFC中A1和Fe的含量,进行下列试剂的选择和基本操作:测定时所需的试剂有_______________。
A.NH3·H2O B.NaOH C.CO2 D .NaClO3
.NaClO3
(6)在测定过程中的操作顺序是: 过滤、___________、灼烧、_________、称量。(写操作名称)。
(7)测定时,直接称量的是____________和_____________的质量(填化学式)。
-
一种新型高效净水剂PAFC(聚合氯化铁铝[AlFe(OH)nC16-n]m),广泛用于日常生活用水和工业污水的处理。某化工厂欲以工业生产废料(金属铁、铝及其氧化物)为原料制取PAFC,设计生产流程如下:
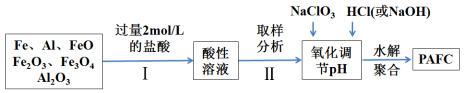
请回答下列问题:
(1)用l0 mol/L的浓盐酸配制2mol/L的稀盐酸,所用玻璃仪器除量筒和玻璃棒外,还有 。
A.容量瓶 B.烧杯 C.烧瓶 D.胶头滴管
(2)下列关于PAFC的说法中正确的是( )
A.PAFC是一种有机高分子化合物 B.PAFC中Fe显+2价
C.PAFC溶于水能电离出OH—,是一种碱 D.PAFC在强酸性和强碱性溶液中均不能稳定存在
(3)步骤Ⅱ中取样分析的目的是( )
A.测定溶液中Fe2+与Fe3+的含量比 B.测定原料是否完全溶解
C.测定溶液中Fe2+的含量,以确定加入NaClO3的量 D.测定溶液中Al3+的含量
(4)写出向溶液中加入NaClO3时,发生反应的离子方程式为 。
(5)该化工厂的化验室为测定产品PAFC中A1和Fe的含量,进行下列试剂的选择和基本操作:
① 测定时所需的试剂有__________________。
A.NH3·H2O B.NaOH C.CO2 D.NaClO3
② 测定时,直接测定的是____________和_____________的质量(填化学式)。
③ 在测定过程中的操作顺序是:过滤、____________、灼烧、____________、称量。(写操作名称)。
-
(16分)
高效净水剂聚合氯化铝铁(PAFC)的组成可表示为[AlFe(OH)nCl6-n]m,该物质广泛应用于日常生活用水和工业废水的处理。
(1)为检测PAFC中铝和铁元素的含量,采用如图所示流程进行。
回答下列问题:
①PAFC中铁元素的化合价为_________。
②步骤I中的试剂A是 (从“氢氧化钠溶液”、“氨水”中选择)
步骤Ⅲ中的试剂B是 。
③步骤Ⅱ的操作是 ,用到的主要玻璃仪器 。
(2)某工厂欲以工业废料(铁、铁和铝的氧化物)为原料制取PAFC,设计如下流程:

①在废料中加入过量稀盐酸,发生多个离子反应,请在空白处补全离子方程式:
FeO+2H+ Fe2++H2O Al2O3+6H+
Fe2++H2O Al2O3+6H+ 2Al3++3H2O
2Al3++3H2O
Fe2O3+6H+ 2Fe3++3H2O
2Fe3++3H2O
②所得酸性溶液中,不能确定是否一定存在的阳离子是 (填序号)。
A.Al3+ B.Fe2+ C.Fe3+ D.H+
为证明该离子确实存在,可采用的操作(必须指明所采用的试剂及观察到的现象)是: 。
③往酸性溶液中加入试剂X的目的是(用离子方程式表示) 。
-
Ӏ.高效净水剂聚合氯化铝铁(PAFC)的组成可表示为[AlFe(OH)nCl6-n]m,该物质广泛应用于日常生活用水和工业废水的处理。某工厂欲以工业废料(金属铝、铁及其氧化物)为原料制取PAFC,设计如下流程:

(1)PAFC中铁元素的化合价为_________。
(2)废料与稀盐酸混合后发生了多个化学反应,在发生的这些反应中,请写出一个是氧化还原反应但不属于四大基本反应类型的反应的离子方程式______________________________。
(3)所得酸性溶液中,不能确定是否一定存在的阳离子是___________,欲确认该离子是否存在最常用的试剂名称为____________________。
(4)试剂X最好是下列中的__________
A.Fe B.HNO3 C.氯水 D.高锰酸钾溶液
(5)水解形成的聚合物分散在水中的粒子直径在1nm~100nm之间,请用简单的实验操作验证该分散系 ____________________________________________________________________________。
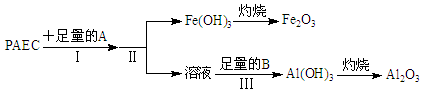
Ⅱ.为检测PAFC中Al和Fe含量,采用如图所示流程进行。
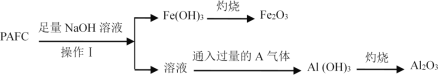
回答下列问题:
(6)操作I的名称______________________。
(7)通入过量的A气体的离子方程式为 ______________。
-
高效净水剂聚合氯化铝铁(PAFC)的组成可表示为[AlFe(OH)nCl6-n]m,该物质广泛应用于日常生活用水和工业废水的处理。
(1)为检测PAFC中铝和铁元素的含量,采用如图所示流程进行:
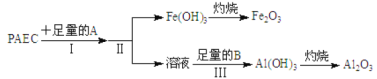
回答下列问题:
①PAFC中铁元素的化合价为__________。
②步骤I中的试剂A是__________ (从氢氧化钠溶液、氨水中选择)步骤III中的试剂B是__________。
③步骤II的操作是__________。
(2)某工厂欲以工业废料(铁、铁和铝的氧化物)为原料制取PAFC,设计如下流程:
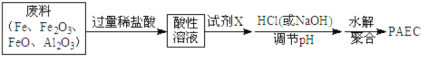
①所得酸性溶液中,不能确定是否一定存在的阳离子是_________(填序号)。
A.Al3+ B.Fe2+ C.Fe3+ D.H+
为证明该离子确实存在,可采用的操作(必须指明所采用的试剂及观察到的现象)是:_____。
②往酸性溶液中加入试剂X的目的是(用离子方程式表示)___________。
-
Ⅰ.高效净水剂聚合氯化铝铁(PAFC)的组成可表示为[AlFe(OH)nCl6﹣n]m,该物质广泛应用于日常生活用水和工业废水的处理。该物质可溶于盐酸产生相应的金属阳离子。为检测PAFC中铝和铁元素的含量,采用如图所示流程进行:
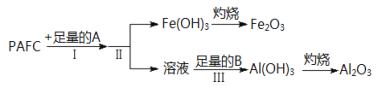
回答下列问题:
⑴PAFC中铁元素的化合价为_____,如何检验该元素的存在___________________
⑵步骤I中的试剂A是_______________(从“氢氧化钠溶液”、“氨水”中选择)步骤Ⅲ中的试剂B是_____________,离子方程式是__________
⑶步骤Ⅱ的操作是______________________
Ⅱ. ⑴甲同学用氢氧化钠溶液和氯化亚铁溶液制备氢氧化亚铁沉淀,该同学将氢氧化钠溶液加入氯化亚铁溶液中,观察到的现象是____________,反应过程中发生反应的化学方程式是_________。乙同学通过如下改进制备氢氧化亚铁:
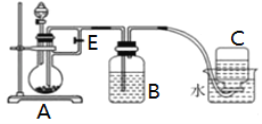
实验提供的试剂:铁屑、3mol/L硫酸溶液、NaOH溶液。请回答下列问题:
⑵①分液漏斗中盛装的试剂是______________溶液 (从“H2SO4”和“NaOH”中选择)。
②实验开始时应将止水夹E___________ (从“打开”和“关闭”中选择)。
-
聚合硫酸铁(简称PFS,化学式为[Fe(OH)n(SO4)3-n/2]m )是一种新型高效的无机高分子絮凝剂,广泛用于水的处理,现用一定质量的铁的氧化物(如下图)为原料来制取聚合硫酸铁。实验步骤如下: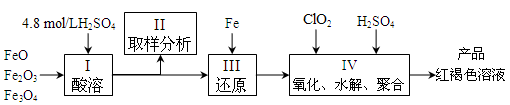
(1)实验室用18.4mol/L的浓硫酸配制250mL4.8mol/L的硫酸溶液,所用的玻璃仪器除烧杯、玻璃棒和量筒外,还需的玻璃仪器__________。定容操作中若俯视容量瓶刻度线,所配硫酸溶液浓度将___________(填“偏高”、“偏低”或“无影响”)
(2)步骤Ⅱ取样分析溶液中的Fe2+、Fe3+的含量,目的是_______。
A.确定下一步还原所需铁的量 B.控制溶液中Fe2+与Fe3+含量比
C.确定氧化Fe2+所需ClO2的量 D.确保铁的氧化物酸溶完全
(3)写出步骤Ⅳ中用ClO2氧化Fe2+时的离子方程式:____________________。(还原产物为Cl-)
(4)为了分析产品聚合硫酸铁溶液中SO42-与Fe3+物质的量之比,有人设计了以下操作:
(I)取25mL聚合硫酸铁溶液,加入足量的BaCl2溶液,产生白色沉淀,白色沉淀经过过滤,洗涤、干燥后,称重,其质量为mg。
(II)另取25mL聚合硫酸铁溶液,加入足量铜粉,充分反应后过滤、洗涤,将滤液和洗液合并配成250mL溶液,取该溶液25.00mL与0.1000 mol/L V mL KMnO4酸性溶液恰好完全反应,MnO4-被还原为Mn2+。
回答下列问题:
① 根据(II)步骤中判断Cu2+、Fe2+、MnO4-、Fe3+氧化性由强到弱的顺序:__________。
② 聚合硫酸铁中SO42-与Fe3+的物质的量之比为____________(用含m、V的代数式表示)。
-
聚合硫酸铝铁(PAFS)是一种高效净水剂,其组成表示为[AlFe(OH)x(SO4)(3- )]y。为检测PAFS中Al的含量,设计如下流程。
)]y。为检测PAFS中Al的含量,设计如下流程。

回答下列问题:
(1)实验中需配制1.0mol/L的NaOH溶液100mL,所需仪器除了玻璃棒、托盘天平、量筒、药匙、烧杯、胶头滴管,还缺少的仪器为__。
(2)PAFS中铁元素的化合价为_______;沉淀A的化学式为_________。
(3)如图所示,过滤操作中的一处错误是__________。
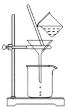
(4)生成沉淀B的离子方程式为______。
(5)PAFS中Al元素的质量分数为_______(用同m、n的代数式表示)。
-
(11分)聚合氯化铝铁(PAFC)是一种高效净水剂,其组成可表示为[ ]。
]。
为检测PAFC中Al的含量,采用下图所示流程。
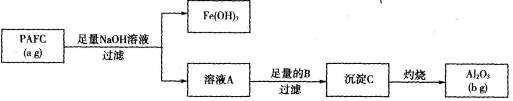
(1)PAFC中铁元素的化合价为_______.
(2)溶液A中含铝元素的溶质是______,它属于____(填“酸”、“碱”、“盐”)。
(3)如图所示,过滤操作中的一处错误是__________________.
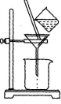
(4)物质B可能是下列试剂中的_______(填代号)。
a.NH3 b.CO2 c.NaOH溶液 d.HNO3溶液
判断流程中沉淀C是否洗净的方法是______________________(描述操作、现象和结论)。
(5)PAFC中A1元素的质量分数为____________(用含有a、b的代数式表示)。
-
高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂。工业上制备高铁酸钾以及高铁酸钾处理污水的部分流程如下:
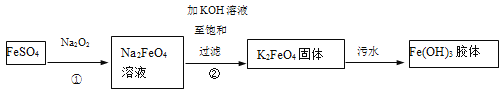
以下说法不正确的是
A.①中一定发生了氧化还原反应
B.污水处理中产生Fe(OH)3胶体,使悬浮物聚沉,利用了胶体具有较强吸附能力的特点
C.另一种在碱性条件下制备K2FeO4的反应可能是:2Fe(OH)3+3ClO-=2FeO42-+3Cl-+4H+ +H2O
D.K2FeO4还可以用于处理废水,例如可以把废水中的CN-转化为两种无毒气体,反应过程中,CN-做还原剂,被K2FeO4氧化

在
.NaClO3