-
(1)在短周期主族元素中,氯及其相邻元素的电负性由大到小的顺序是(用元素符号表示)
(2)A、B、C为同一短周期金属元素。依据下表数据分析,C元素在化合物中的主要化合价为;第二电离能(I2)B小于A的原因是 。
| 电离能/kJ·mol-1 | I1 | I2 | I3 | I4 |
| A | 500 | 4600 | 6900 | 9500 |
| B | 740 | 1500 | 7700 | 10500 |
| C | 580 | 1800 | 2700 | 11600 |
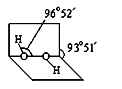
(3)已知过氧化氢分子的空间结构如右图所示,分子中氧原子采取杂化;通常情况下,H2O2与水任意比互溶的主要原因是。
(4)R是1~36号元素中未成对电子数最多的原子。R3+在溶液中存在如下转化关系:
R3+  R(OH)3
R(OH)3  [R(OH)4]-
[R(OH)4]-
①基态R原子的价电子排布式为________。
②[R(OH)4]-中存在的化学键是________。
A.离子键 B.极性键 C.非极性键 D.配位键
-
A、B、C、D四种元素处于同一周期.在同族元素中,A的气态氢化物沸点最高,B的最高价氧化物对应水化物的酸性在同周期中最强,C的电负性介于A、B之间,D与B相邻.
(1)C原子的价电子排布式为________.
(2)A、B、C三种原子的第一电离能由大到小的顺序是(写元素符号)________.
(3)B的单质分子中存在________个π键;B的气态氢化物BH3分子中的中心原子轨道采用________杂化.B和D形成一种超硬、耐磨、耐高温的化合物,该化合物属于________晶体,其硬度比金刚石________(填“大”或“小”).
(4)A的气态氢化物的沸点在同族中最高的原因________.
-
A、B、C、D四种元素处于同一周期,在同族元素中,A的气态氢化物的沸点最高,B的最高价氧化物对应的水化物的酸性在同周期中是最强的,C的电负性介于A、B之间,D与B相邻。
(1)C原子的价电子排布式为________。
(2)A、B、C三种元素原子的第一电离能由大到小的顺序是(写元素符号)________。
(3)B的单质分子中存在________个 键。
键。
(4)D和B形成一种超硬、耐磨、耐高温的新型化合物,该化合物属于________晶体,其硬度比金刚石________(填“大”或“小”)。
(5)A的气态氢化物的沸点在同族中最高的原因是________。
-
A、B、C、D四种元素处于同一周期,在同族元素中,A的气态氢化物的沸点最高,B的最高价氧化物对应的水化物的酸性在同周期中是最强的,C的电负性介于A、B之间,D与B相邻.
(1)C原子的价电子排布式为______;
(2)A、B、C三种元素原子的第一电离能由大到小的顺序是(写元素符号)______;
(3)B的单质分子中存在______个π键;
(4)D和B形成一种超硬、耐磨、耐高温的新型化合物,该化合物属于晶体,其硬度比金刚石______(填“大”或“小”);
(5)A的气态氢化物的沸点在同族中最高的原因是______.
-
处于同一周期的A,B,C,D四种短周期元素,其气态原子获得一个电子所放出的能量大小顺序为 。则下列说法中,正确的是( )
。则下列说法中,正确的是( )
a.元素的非金属性依次增强
b.元素的电负性依次减小
c.元素的第一电离能依次增大
d.最高价氧化物对应水化物的酸性依次减弱
A.ad B.bd C.ac D.cd
-
位于同一周期的四种短周期非金属元素A、B、C、D,其原子对键合电子的吸引力由大到小的顺序为 。下列有关元素A、B、C、D的说法正确的是 ( )
。下列有关元素A、B、C、D的说法正确的是 ( )
a.元素的非金属性依次增强;
b.元素的电负性依次减小;
c.元素的第一电离能依次增大;
d.最高价氧化物对应水化物 均存在
均存在 的酸性依次减弱。
的酸性依次减弱。
A.ad B.bd C.ac D.cd
-
A、B、C、D、E是同一周期的五种主族元素,A和B的最高价氧化物对应的水化物均呈碱性,且碱性B>A,C和D的电负性C>D;E是这五种元素中原子半径最小的元素,则它们的原子序数由小到大的顺序是
A. A、B、C、D、E B. E、C、D、A、B
C. B、A、D、C、E D. C、D、E、B、A
-
位于元素周期表前四周期的五种元素A、B、C、D、E,原子序数依次增大.A元素原子的最外层电子排布可表示为:asaap2a,B元素在地壳中含量居第二位,C与B位于同一周期,且是该周期元素中电负性最大的元素,D元素的+3价离子的3d亚层为半充满,E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子.
根据以上信息回答下列问题:
(1)E的元素符号为______,其基态原子的电子排布式为______.
(2)A的氢化物比下周期同族元素的氢化物沸点还要高,其原因是______.
(3)B元素可分别与A元素、C元素形成两种常见化合物,这两种化合物的熔沸点高低顺序为______(用化学式表示),原因是______.
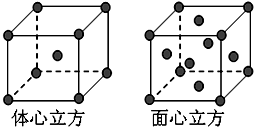
(4)D元素的单质晶体在不同温度下有两种堆积方式,晶胞分别如下图所示.面心立方晶胞和体心立方晶胞中实际含有的D原子个数之比为______,两种堆积模型中与该元素一个原子等距离且最近的原子数之比为:______.
-
与氯元素同周期且金属性最强的元素位于周期表的第____周期___族。与该元素相邻的短周期主族元素原子半径从大到小的顺序是_____(用元素符号表示)
-
氮、磷、砷是同族元素,请回答下列问题。
(1)氮与元素周期表同周期的相邻元素的第一电离能由小到大的顺序为:_____________(用元素符号表示)。
(2)氨水溶液中存在多种氢键,任意表示出其中一种:____________________。
(3)PH3和NH3与卤化氢的反应相似,产物的结构和性质也相似。下列对PH3与HI反应产物的推断正确的是___________(填序号)。
a.不能与NaOH反应 b.含离子键、共价键 c.能与水反应
(4)氮原子间能形成氮氮三键,而砷原子间不易形成三键的原因:_____________________。
(5)X+中所有电子正好充满K、L、M三个电子层,它与N3-形成的晶体结构如图所示。

①X的核外电子排布式为________________________。与同一个N3-相连的X+有______个。
②X的高价阳离子(X2+)在水溶液中存在离子[X(H2O)4]2+,则X2+与H2O之间的键型为_____。
③请画出[X(H2O)4]2+离子的结构式_________________(用元素符号写结构式)。

R(OH)3
[R(OH)4]-

