-
位于元素周期表前四周期的五种元素A、B、C、D、E,原子序数依次增大.A元素原子的最外层电子排布可表示为:asaap2a,B元素在地壳中含量居第二位,C与B位于同一周期,且是该周期元素中电负性最大的元素,D元素的+3价离子的3d亚层为半充满,E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子.
根据以上信息回答下列问题:
(1)E的元素符号为______,其基态原子的电子排布式为______.
(2)A的氢化物比下周期同族元素的氢化物沸点还要高,其原因是______.
(3)B元素可分别与A元素、C元素形成两种常见化合物,这两种化合物的熔沸点高低顺序为______(用化学式表示),原因是______.
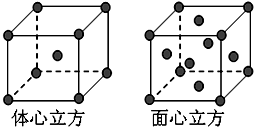
(4)D元素的单质晶体在不同温度下有两种堆积方式,晶胞分别如下图所示.面心立方晶胞和体心立方晶胞中实际含有的D原子个数之比为______,两种堆积模型中与该元素一个原子等距离且最近的原子数之比为:______.
-
X、Y、Z、W为短周期元素,且原子序数依次增大,X2-和Y+核外电子排布相同,X、Z位于同一主族,Z、W位于同一周期,W的最外层电子数是X、Y最外层电子数之和。下列说法不正确的是
A. 原子半径Y>Z>X
B. X 分别与Y、Z形成的化合物均至少有两种
C. 最高价氧化物对应水化物的酸性:W>Z
D. 氢元素在与X、Y、Z分别形成的化合物中,化合价均为+1
-
X、Y、Z、Q、R五种元素的原子序数依次增大.其中:X的最外层电子排布为 ;Y是元素周期表中电负性最大的元素;Y、Z位于同一主族;Q基态原子核外的M能层中有两个未成对电子和三个空轨道;R位于第四周期ⅥB族。
;Y是元素周期表中电负性最大的元素;Y、Z位于同一主族;Q基态原子核外的M能层中有两个未成对电子和三个空轨道;R位于第四周期ⅥB族。
请回答下列问题:
 元素基态原子的电子排布式为 ______ ,它的最高价氧化物的水化物的化学式为 ______ 。
元素基态原子的电子排布式为 ______ ,它的最高价氧化物的水化物的化学式为 ______ 。
 分子的立体构型是 ______ ,中心原子的杂化方式是 ______ 。
分子的立体构型是 ______ ,中心原子的杂化方式是 ______ 。
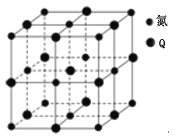
 与氮元素形成的一种化合物晶胞如图所示,该化合物的化学式为 ______。该晶体中与氮原子距离相等且最近的氮原子有 ______ 个。
与氮元素形成的一种化合物晶胞如图所示,该化合物的化学式为 ______。该晶体中与氮原子距离相等且最近的氮原子有 ______ 个。
 化合物
化合物 熔点为
熔点为 ,沸点为
,沸点为 ,熔融态不导电,可知
,熔融态不导电,可知 的晶体类型是 ______
的晶体类型是 ______  与热水反应的化学方程式为 ______ 。
与热水反应的化学方程式为 ______ 。
-
已知A、B、C、D、E、F为前4周期的6种元素,原子序数依次增大,其中A位于周期表的s的区,其原子中电子层数和未成对电子数相同;B原子价电子排布式为nsnnpn,B和E同主族,D原子的最外层电子数是其内层的3倍;F元素位于元素周期表的第4行、第11列。试回答下列问题:
(1)基态F原子的核外电子排布式为 。
(2)关于B2A2的下列说法中正确的是 (填选项序号)。
①B2A2中的所有原子都满足8电子稳定结构
②每个B2A2分子中σ键和π键数目比为1:1
③B2A2是由极性键和非极性键构形成的非极性分子
④B2A2中心原子的杂化类型为sp杂化
(3)B、C、D三种元素第一电离能由大到小的顺序排列为 (用元素符号表示)。
(4)C的单气态氢化物与C的最高价氧化物对应的水化物反应生成一种盐H,H晶体中存在的化学键类型有 (填选项序号)。
①离子键 ②共价键 ③氢键 ④配位键 ⑤金属键
(5)基态E原子的最高能层具有的原子轨道数为 ;B和E的最高价氧化物中,熔沸点较高的是 (写化学式);
(6)F单质的晶体堆积方式为面心立方最密堆积,其配位数为 ;若F的相对分子质量为M,它的晶胞棱长为acm,则F晶体的密度为 g·cm-3。(阿伏伽德罗常数为NA)
-
X、Y、Z、W、M、Q、R六种元素均位于前四周期,且原子序数依次增大。其相关信息如下:X的核外电子总数等于其电子层数;Y的最外层电子数是次外层的3倍;Z原子的价层电子排布为nsn-1npn-2;Q的外围电子排布为(n+1)d4n(n+2)sn; W、M、R最外层电子只有1个。回答下列问题:
(1)Q元素位于周期表第_____族。Q金属配合物Q(CO)n的中心原子的价电子数与配体提供的电子总数之和为18,则n=_____。M的一种重要化合物用于检查司机是否酒驾,该化合物的化学式______,如果司机酒驾检查时该物质显示的颜色变化是_____________________。
(2)关于R单质晶体的说法正确的是______________。
①晶体中的化学键具有方向性和饱和性
②晶体中不存在阴阳离子间的相互作用
③晶体导电是因为在外加电场作用下产生自由电子
④单质具有光泽是因为金属阳离子吸收并放出可见光
⑤晶体中原子的堆积方式为‥ABCABC•••‥型。
(3)离子化合物中阴阳离子半径之比是决定晶体构型的重要因素之一,配位数与离子半径之比存在如下关系:

已知,在QY中Q离子的半径为70pm,Y离子的半径为140pm,分析以上信息,可以推导出该晶体结构与常见_______晶体(填写化学式)阴阳离子的配位数相同。与阴(阳)离子配位的这几个阳(阴)离子,在空间构成的立体形状为_______________。
(4)W的原子半径为r,其晶体的空间利用率______________(用含r的表达式表示)。
(5)已知SiH4在碱的催化作用下,剧烈发生水解,反应方程式为:SiH4 +(n+2)H2O= SiO2.nH2O + 4H2,已知每1mol SiH4水解反应中转移4mol电子,则C,H,Si三种元素的电负性由大到小的顺序为___________。
(6)X射线衍射测定发现,I3AsF6中存在I3+离子,I3+离子的几何结构为______,中心原子的杂化方式为_____
(7)已知金刚石中碳原子的连接方式如下图,则12g金刚石中含有的六元环的数目是________个。

-
Q、R、T、W、X、Y、Z为原子序数依次增大的前四周期元素,其中R、T、W是同周期相邻元素,Q、R最外层电子排布可表示为asa,bsbbpa(a≠b):X的基态原子中占据哑铃形原子软道的电子数为10,Y与X为同周期主族元素,基态Z原子核外电子填充在7个能级中,且价层电子有3对成对电子。
(1)四种分子①RY3②TQ4③WQ3④Q2X键角由大到小排列的顺序是_____________(填序号).
(2)微粒W3-的空间构型为_____________。
(3)XTW-的等电子体中属于分子的有_____________(填化学式,写出一种即可),XTW-的电子式为_____________;
(4)R的某种钠盐晶体,其阴离子Mm-(含Q、R、O三种元素)的球棍模型如下图所示:在Mm-中,R原子轨道杂化类型为_____________,m=_____________。(填数字)

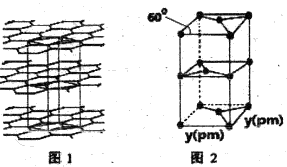
(5)T的某种单质的片层与层状结构如图1所示.其中层间距离为xpm,图2为从结构中取出的晶胞,若晶胞的边长为ypm,则T的该种单质的密度为_____________g•cm-3。(1pm=10-12m)
-
[s1] X、Y、Z、M是周期表前四周期中的四种常见元素,原子序数依次增大,其相关信息如下表:
| 元素 | 相关信息 |
| X | 原子最外层电子数是内层电子数的2倍 |
| Y | 基态原子最外层电子排布为 |
| Z | 与Y同周期,第一电离能小于Y |
| M | 与X形成的合金为目前用量最多的金属材料 |
(1)Z位于周期表第________周期第族。Y、Z的氢化物稳定性较强的是________(写化学式)。
(2)X与氢可形成一种原子个数比为1:1的化合物,相对分子质量为78,该分子中存在________个 键。H—X、H—Y、H—Z三种共价键中,键长最长的是________。
键。H—X、H—Y、H—Z三种共价键中,键长最长的是________。
(3)M元素基态原子的电子排布式是________。
(4)已知下列数据:
 M(s)+
M(s)+ Z2(g) MZ(s) △H=-272.kJ·mol-1
Z2(g) MZ(s) △H=-272.kJ·mol-1
 2M(s)+
2M(s)+ Z2(g) M2Z3(s) △H=-824.2.kJ·mol-1
Z2(g) M2Z3(s) △H=-824.2.kJ·mol-1
MZ转化为M2Z3的热化学方程式是________
[s1]18.
-
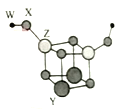
短周期主族元素W、X、Y、Z的原子序数依次增大,四种元素可以组成一种分子簇,其分子结构如图所示,(球大小表示原子半径的相对大小),W、X位于不同周期,X原子的最外层电子数是次外层电子数的3倍,Z的族序数等于其周期数,下列说法中正确的是
A.Y、Z的简单离子均不影响水的电离平衡
B.工业上获得Y、Z单质均可采用电解它们的熔融氯化物
C.Y的最高价氧化物对应水化物的碱性比Z的弱
D.相同条件下,W单质的沸点比X单质的低
-
短周期主族元素W、X、Y、Z的原子序数依次增大,四种元素可以组成一种分子簇,其分子结构如图所示(球的大小表示原子半径的相对大小),W、X位于不同周期,X原子的最外层电子数是次外层电子数的3倍,Z的族序数等于其周期数,下列说法中正确的是( )。
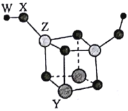
A.W和X可以组成原子个数比为2:1和1:1的离子化合物
B.工业上可采用电解Z的熔融氯化物的方法制得单质Z
C.Z的最高价氧化物对应水化物的碱性比Y的强
D.X、Y、Z三种元素的离子半径由小到大顺序为Z<Y<X
-
X、Y、Z、W是元素周期表中前30号元素,且原子序数依次增大。其相关信息如下表:
| 元素 | 相关信息 |
| X | X原子基态时最外层电子数是其内层电子总数的2倍 |
| Y | Y的基态原子最外层电子排布式为nsnnpn+2 |
| Z | Z元素的最高正价与负价代数和为6 |
| W | W基态原子未成对电子数是前30号元素中最多的 |
(1)W位于元素周期表第________周期第________族,其基态原子最外层有________个电子。
(2)X的第一电离能比Y的________(填“大”或“小”),1mol X22-中含有的 键数目为________。
键数目为________。
(3)X和Y的气态氢化物中,较稳定的是________(写化学式),Y的同族元素(包括Y)的最简单氢化物中沸点最低的是________。
(4)写出KZY3与HZ浓溶液反应制取Z2的化学方程式,并标出电子转移的方向和数目。
(5)已知:X(s)+Y2(g)=XY2(g) ΔH 1= -393.5 kJ•mol-1
XY(g) +1/2Y2(g)=XY2(g) ΔH 2= -282.9 kJ•mol-1
则X(s)与Y2(g)反应生成XY(g)的热化学反应方程式为________。







