-
(12分)已知:I2+2S2O===S4O+2I-。相关物质的溶度积常数见下表:
物质
Cu(OH)2
Fe(OH)3
CuCl
CuI
Ksp
2.2×10-20
2.6×10-39
1.7×10-7
1.3×10-12
(1)某酸性CuCl2溶液中含有少量的FeCl3,为得到纯净的CuCl2·2H2O晶体,加入________,(填化学式)调至pH=4,使溶液中的Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)=________。过滤后,将所得滤液低温蒸发、浓缩结晶,可得到CuCl2·2H2O晶体。
(2)在空气中直接加热CuCl2·2H2O晶体得不到纯的无水CuCl2,原因是________ (用化学方程式表示)。由CuCl2·2H2O晶体得到纯的无水CuCl2的合理方法是________。
(3)某学习小组用“间接碘量法”测定含有CuCl2·2H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取0.36 g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。用0.1000 mol/L Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00 mL。
①可选用________作滴定指示剂,滴定终点的现象是________。
②CuCl2溶液与KI反应的离子方程式为________。
③该试样中CuCl2·2H2O的质量百分数为________。
高二化学填空题中等难度题查看答案及解析
-
已知:I2+2S2O32-=S4O62-+2I-。相关物质的溶度积常数见下表:
物质
Cu(OH)2
Fe(OH)3
CuCl
CuI
Ksp
2.2×10-20
2.6×10-29
1.7×10-7
1.3×10-12
(1)某酸性CuCl2溶液中含有少量的FeCl3,为得到纯净的CuCl2﹒2H2O晶体,加入 调至pH=4,使溶液中的Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)= ;过滤后,将所得滤液低温蒸发、浓缩结晶,可得到CuCl2﹒2H2O晶体。
(2)在空气中直接加热CuCl2﹒2H2O晶体得不到纯的无水CuCl2,原因是 。(用化学方程式表示)。由CuCl2﹒2H2O晶体得到纯的无水CuCl2的合理方法是 。
(3)某学习小组用“间接碘量法”测定含有CuCl2﹒2H2O晶体的试样(不含能与I―发生反应的氧化性质杂质)的纯度,过程如下:取0.36 g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。用0.1000 mol·L-1Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00 mL。
①可选用 作滴定指示荆,滴定终点的现象是 。
②CuCl2溶液与KI反应的离子方程式为 。
③该试样中CuCl2﹒2H2O的质量百分数为 。
高二化学填空题困难题查看答案及解析
-
已知:I2+2S2O32-=S4O62-+2I-
相关物质的溶度积常数见下表:
物质
Cu(OH)2蓝色
Fe(OH)3红褐
CuCl白色
CuI白色
Ksp
2.2×10-20
2.6×10-39
1.02×10-6
1.3×10-12
(1)某酸性CuCl2溶液中含有少量的FeCl3,为得到纯净的CuCl2·2H2O晶体,加入___________,调至pH=4,使溶液中的Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)=_________。过滤后,将所得滤液低温蒸发、浓缩结晶,可得到CuCl2·2H2O晶体。
(2)在空气中直接加热CuCl2·2H2O晶体得不到纯的无水CuCl2,原因是__________________(用化学方程式表示)。由CuCl2·2H2O晶体得到纯的无水CuCl2的合理方法是_________________。
(3)某学习小组用“间接碘量法”测定含有CuCl2·2H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取0.36 g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。用0.100 0 mol·L-1 Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00 mL。
可选用_________作滴定指示剂,滴定终点的现象是________________。
CuCl2溶液与KI反应的离子方程式为_____________________。
高二化学填空题中等难度题查看答案及解析
-
已知:I2+2S2O32-==S4O62-+2I-
相关物质的溶度积常数见下表:
物质
Cu(OH)2
Fe(OH)3
CuCl
CuI
Ksp
2.2×10-20
2.6×10-39
1.7×10-7
1.3×10-12
(1)某酸性CuCl2溶液中含有少量的FeCl3,为得到纯净的CuCl2·2H2O晶体,加入_____ ___,调至pH=4,使溶液中的Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)=____ ____。过滤后,将所得滤液低温蒸发、浓缩结晶,可得到CuCl2·2H2O晶体。
(2)在空气中直接加热CuCl2·2H2O晶体得不到纯的无水CuCl2,原因是 (用化学方程式表示)。由CuCl2·2H2O晶体得到纯的无水CuCl2的合理方法是 。
(3)某学习小组用“间接碘量法”测定含有CuCl2·2H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取0.36 g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。用0.100 0 mol·L-1 Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00 mL。
①可选用________作滴定指示剂,滴定终点的现象是 _。
②CuCl2溶液与KI反应的离子方程式为 。
③该试样中CuCl2·2H2O的质量百分数为__________________。
高二化学填空题困难题查看答案及解析
-
Ⅰ.已知:I2+2S2O=S4O+2I-。相关物质的溶度积常数见下表:
物质
Cu(OH)2
Fe(OH)3
CuCl
CuI
Ksp
2.2×10-20
2.6×10-39
1.7×10-7
1.3×10-12
(1)某酸性CuCl2溶液中含有少量的FeCl3,为得到纯净的CuCl2·2H2O晶体,加入 ,(填化学式)调至pH=4,使溶液中的Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)= 。过滤后,将所得滤液低温蒸发、浓缩结晶,可得到CuCl2·2H2O晶体。
(2)由CuCl2·2H2O晶体得到纯的无水CuCl2的合理方法是 。
(3)某学习小组用“间接碘量法”测定含有CuCl2·2H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取0.36 g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。用0.1000 mol/L Na2S2O3标准溶液滴定,用淀粉溶液作指示剂,到达滴定终点时,消耗Na2S2O3标准溶液20.00 mL。
①CuCl2溶液与KI反应的离子方程式为 。
②该试样中CuCl2·2H2O的质量百分数为 。
Ⅱ.乙醇是重要的有机化工原料,可由乙烯直接水合法生产。
已知:乙烯气相直接水合反应C2H4(g)+H2O(g)=C2H5OH(g) △H=—45.5KJ·mol-1
下图为气相直接水合法乙烯的平衡转化率与温度、压强的关系(其中
=1:1)

(4)图中压强(
、
、
、
)由大到小顺序为 。
(5)计算乙烯水合制乙醇反应在图中A点(P2=7.85Mpa,乙烯平衡转化率为20%)的平衡常数Kp= (要求写出解题过程)。
本小题提示:用平衡分压代替平衡浓度计算,分压=总压×物质的量分数。
高二化学实验题极难题查看答案及解析
-
已知:I2+2S2O32-=S4O62-+2I-
相关物质的溶度积常数见下表:
物质
Cu(OH)2
Fe(OH)3
CuCl2
CuI
Ksp
2.2×10-20
2.6×10-29
1.7×10-7
1.3×10-12
(1)某酸性CuCl2溶液中含有少量的FeCl3 ,为得到纯净的CuCl2.H2O 晶体,加入______,调至pH=4,使溶液中的Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)=_______。过滤后,将所得滤液低温蒸发、浓缩结晶,可得到CuCl2.H2O晶体。
(2)在空气中直接加热CuCl2.H2O晶体得不到纯的无水CuCl2,原因是__________(用化学方程式表示)。由CuCl2.H2O晶体得到纯的无水CuCl2的合理方法是_____________。
(3)某学习小组用“间接碘量法”测定含有CuCl2.H2O的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取0.36g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。用0.1000mol/LNa2S2O3标准溶液20.00mL。
①可选用______作滴定指示剂,滴定终点的现象是__________。
②CuCl2溶液与KI反应的离子方程式为__________。
③该试样中CuCl2.H2O的质量百分数为_______。
高二化学填空题中等难度题查看答案及解析
-
已知:I2+2S2O32-=S4O62-+2I-;CuI是不溶于水的白色沉淀。
相关物质的溶度积常数见下表:
物质
Cu(OH)2
Fe(OH)3
CuCl
CuI
Ksp
2.2×10-20
2.6×10-39
1.7×10-7
1.3×10-12
(1)某酸性CuCl2溶液中含有少量的FeCl3,为得到纯净的CuCl2·2H2O晶体,加入_________,调至pH=4,使溶液中的Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)=_________。过滤后,将所得滤液低温蒸发、浓缩结晶,可得CuCl2·2H2O晶体。
(2)在空气中直接加热CuCl2·2H2O晶体得不到纯的无水CuCl2,原因是(用文字叙述):____________________________________________。由CuCl2·2H2O晶体得到纯的无水CuCl2的合理方法是______________________________。
(3)某学习小组用“间接碘量法”测定含有CuCl2·2H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取0.36 g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。用0.100 0 mol·L-1 Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00 mL。
①可选用_______________作滴定指示剂,滴定终点的现象是________________________。
②CuCl2溶液与KI反应的离子方程式为___________________________________________。
③该试样中CuCl2·2H2O的质量百分数为__________________
高二化学综合题中等难度题查看答案及解析
-
己知:I2+2S2O32-=S4O62-+2I-。相关物质的溶度积常数见下表:
物质
Cu(OH)2
Fe(OH)3
CuCl
CuI
Ksp
2.2×10-20
2.6×l0-39
1.7×l0-7
1.3×l0-12
(1)某酸性CuCl2溶液中含有少量的FeCl3,为得到纯净的CuC12·2H2O晶体,常加入CuO或Cu(OH)2,调至pH=4,使溶液中的Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)=_____________。 过滤后,将所得滤液低温蒸发、浓缩结晶,可得到CuCl2·2H2O晶体。
(2)在空气中直接加热CuCl2·2H2O晶体得不到纯的无水CuC12, 原因是(用化学方程式表示)_____________________________,由CuCl2·2H2O晶体得到纯净的无水CuCl2的合理方法是________________________________________________。
(3)某学习小组用“间接碘量法”测定含有CuCl2·2H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取1.44g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀(CuI)。将反应后的溶液稀释为100 mL,用0.1000mol/LNa2S2O3标准溶液(溶液呈弱碱性)进行滴定,滴定结果如下表所示。
滴定次数
待测溶液的体积/mL
标准溶液的体积/mL
滴定前刻度
滴定后刻度
1
25.00
0.02
22.03
2
25.00
2.00
21.98
3
25.00
0.20
20.22
①可选用__________作滴定指示剂,滴定终点的现象是_________________________。
②滴定过程中操作滴定管的图示正确的是_____________。

③若滴定时出现下列情况,测定结果偏高的是___________。
a.滴定前用蒸馏水冲洗锥形瓶 b.滴定前滴定管尖嘴有气泡,滴定后气泡消失
c.酸式滴定管滴至终点时俯视读数 d.酸式滴定管用蒸馏水洗后,未用标准液润洗
④CuCl2溶液与KI反应的离子方程式为______________________________。
⑤该试样中CuCl2·2H2O的质量百分数为____________________。
高二化学实验题困难题查看答案及解析
-
已知:I2+2 S2O32-
S4O62-+2I-。相关物质的溶度积常数见下表:
物质
Cu(OH)2
Fe(OH)3
CuCl
CuI
Ksp
2.2×10-20
2.6×10-39
1.7×10-7
1.3×10-12
(1)某酸性CuCl2溶液中含有少量的FeCl3,为得到纯净的CuCl2•2H2O晶体,加入________;调至pH=4,使溶液中的Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)=_____________;过滤后,将所得滤液低温蒸发、浓缩结晶,可得到CuCl2•2H2O晶体。
(2)在空气中直接加热CuCl2•2H2O晶体得不到纯的无水CuCl2,原因是________________。(用化学方程式表示)。由CuCl2•2H2O晶体得到纯的无水CuCl2的合理方法是_______________。
(3)某学习小组用“间接碘量法”测定含有CuCl2•2H2O晶体的试样(不含能与I-发生反应的氧化性质杂质)的纯度,过程如下:取0.36 g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。用0.1000 mol/L Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00 mL。已知:CuCl2溶液与KI反应的离子方程式为Cu2+ + 4I- = 2CuI↓ + I2
①可选用___________作滴定指示剂,滴定终点的现象是_________________。
②该试样中CuCl2•2H2O的质量百分数为___________________________。
高二化学综合题困难题查看答案及解析
-
(1)现用氯化铜晶体(CuCl2·2H2O,含少量FeCl2杂质)制取纯净的CuCl2·2H2O,先将其制成水溶液,后按如图步骤进行提纯:
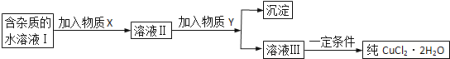
已知:相关物质的溶度积常数见下表:
物质
Cu(OH)2
Fe(OH)3
Fe(OH)2
Ksp
2.0×10ˉ20
1.0×10ˉ38
1.64×10ˉ14
请回答下列问题:
①请从下列物质中选出第一步中需加入的X(__________)
a.NaClO b.H2O2 c.KMnO4 d.HNO3
②溶液Ⅱ中含有少量的Fe3+,如何检验该离子的存在:_____________________________。
③若此时溶液中的c(Cu2+)=0.02mol/L,为得到纯净的CuCl2·2H2O晶体,可加入CuO固体,使溶液中的Fe3+完全转化为Fe(OH)3沉淀且不沉淀Cu2+,调节pH的范围是_______。(通常认为残留在溶液中的离子浓度小于或等于1×10ˉ5 mol/L时就认为沉淀完全)。
④由溶液Ⅲ得到CuCl2·2H2O晶体的操作是___________________________________。
(2)镉镍可充电电池在现代生活中有广泛应用,它的充、放电反应按下式进行:Cd+2NiO(OH)+H2O
Cd(OH)2+2Ni(OH)2
回答下列问题:
①放电时,金属Cd作_______极;
②充电时的阳极电极反应式为_____________________________________________。
③充电时,当电路中通过0.2moleˉ,阴极质量将_______(填“增加”、“减少”)___g。
高二化学填空题困难题查看答案及解析