-
NH3是一种重要的化工原料。
(1)不同温度、压强下.合成该平衡体系NH3的物质的量分数如图 (N2和H2的起始物质的量之比为1:3)。

①分析图中数据,升高温度,该反应的平衡常数K值____(填“增大”“减小”或“不变”)。
②如果开始时向密闭容器中投入1.0mol N2 和3.0mol H2,则在500℃、3×107Pa条件下达到平衡时N2 的平衡转化率=_______。(保留两位有效数字)
③液氨和水颇为相像,它能溶解多种无机及有机分子,其电离方程式可表示为2NH3  NH4++ NH2一(某温度下其离子积常数为10-30)。液氨中的pNH4与水中的pH相似,则该温度下液氨的pNH4=____。
NH4++ NH2一(某温度下其离子积常数为10-30)。液氨中的pNH4与水中的pH相似,则该温度下液氨的pNH4=____。
(2)以氨气代替氢气研发氨清洁燃料电池是当前科研的一个热点。氨燃料电池使用的电解质溶液是KOH溶液。该电池负极的电极反应式为_________________。
(3)NH3也是造成水体富营养化的重要因素之一,用次氯酸钠水解生成的次氯酸将水中的NH3转化为氮气除去,其相关反应的热化学方程式如下:
反应I: NH3 (aq)+HClO(aq)=NH2Cl(aq)+H2O(l) △H1=akJ/mol;
反应II :NH2Cl(aq)+HClO(aq)=NHCl2(aq) +H2O(l) △H2=bkJ/mol;
反应III: 2NHCl2(aq) +H2O(l)=N2(g)+HClO( aq)+3HCl( aq) △H3=ckJ/mol。
①2NH3(aq)+3HClO(aq)==N2 (g)+3HCl(aq)+3H2O(l) △H=________kJ/mol
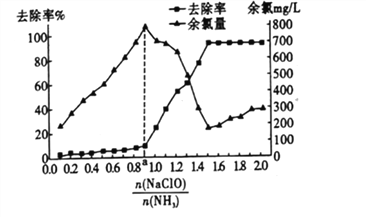
②已知在水溶液中NH2Cl较稳定,NHCl2不稳定易转化为氮气。在其他条件不变的情况下,改变 对溶液中次氯酸钠去氨氮效果与余氯(溶液中+1价氯元素的含量)的影响如图所示。a点之前溶液中发生的主要反应为_______(填序号)。
对溶液中次氯酸钠去氨氮效果与余氯(溶液中+1价氯元素的含量)的影响如图所示。a点之前溶液中发生的主要反应为_______(填序号)。
A.反应I、I I B.反应I

③除氨氮过程中最佳的 值约为______________。
值约为______________。
-
NH3是一种重要的化工原料。
(1)不同温度、压强下.合破氦平衡休系NH3的物质的量分数如图 (N2和H2 的起始物质的量之比为1:3)。

①分析图中数据,升商温度,该反应的平衡常数K值____(填“增大”“城小”或“不变”)。
②下列关于合成氨的说法正确是_____(填序号)。
A.工业上合成氨,为了提高氨的含量压强越大越好
B.使用催化剂可以提高氨气的产率
C.合成氨反应△H<0、△S<0,该反应高温条件下一定能自发进行
D.减小n(N2): n(H2) 的比值,有利于提高N2 的转化率
③如果开始时向密闭容器中投入1.0mol N2 和3.0mol H2,则在500C、3×107Pa条件下达到平衡时N2 的平衡 转 化率=_______。(保留两位有效数字)
(2)以氨气代替氢气研发氨燃料电池是当前科研的一一个热点。氨燃料电池使用的电解质溶液是KOH溶液。该电池负极的电极反应式为_________________。
(3)NH3也是造成水体富营养化的重要因素之一,用次氯酸钠水解生成的次氯酸将水中的NH3转化为氮气除去,其相关反应的热化学方程式如下:
反应I: NH3 (aq)+HClO(aq)=NH2Cl(aq)+H2O(l) △H1=akJ/mol;
反应II :NH2Cl(aq)+HClO(aq)=NHCl(aq)v △H2=bkJ/mol;
反应III: 2NHCl2(aq) +H2O(l)=N2(g)+HClO( aq)+3HCl( aq) △H3=ckJ/mol。
①2NH3(aq)+3HClO(aq)==N2(g)+ H2O(l) △H=________kJ/mol
②已知在水溶液中NH2Cl较稳定,NHCl2不稳定易转化为氮气。在其他条件不变的情况下,改变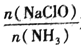 对溶液中次氯酸钠去氨氮效果与余氯(溶液中+1价氯元素的含量) 的影响如图l4所示。a点之前溶液中发生的主要反应为_______(填序号)。
对溶液中次氯酸钠去氨氮效果与余氯(溶液中+1价氯元素的含量) 的影响如图l4所示。a点之前溶液中发生的主要反应为_______(填序号)。
A.反应I、I I B.反应I
③除氨氮过程中最佳的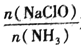 值约为______________。
值约为______________。
-
氨是一种重要的化工原料,氨的合成与应用是当今重要研究内容之一。不同温度、压强下,合成氨平衡体系中NH3的物质的量分数见下表(N2和H2起始物质的量之比为1∶3)。
|  压强(Mpa) 压强(Mpa)
 氨的平 氨的平
衡含量(%) 温度(℃) | 0.1 | 10 | 20 | 30 | 60 | 100 |
| 200 | 15.3 | 81.5 | 86.4 | 89.9 | 95.4 | 98.8 |
| 300 | 2.2 | 52.0 | 64.2 | 71.0 | 84.2 | 92.6 |
| 400 | 0.4 | 25.1 | 38.2 | 47.0 | 65.2 | 79.8 |
| 500 | 0.1 | 10.6 | 19.1 | 26.4 | 42.2 | 57.5 |
| 600 | 0.05 | 4.5 | 9.1 | 13.8 | 23.1 | 31.4 |
回答下列有关问题:
(1)利用表中数据推断得出合成氨的反应是__________反应(填“放热”、“吸热”或“无热量变化”)。
(2)根据表中数据,在200℃和100MPa时,平衡体系中NH3的物质的量分数最高,而实际工业生产不选用该条件的主要原因是___________________________________。
(3)一定条件下,对在密闭容器中进行的合成氨反应达平衡后,其他条件不变时,若同时压缩容器的体积和升高温度达新平衡后,与原平衡相比,请将有关物理量的变化的情况填入下表中(填“增大”、“减小”或“可能增大也可能减小”):
(4)将1molH2和1molN2通入一体积不变的密闭容器中,在一定温度和催化剂作用下,反应达到平衡,测得NH3的物质的量为0.3mol,此时若移走0.5molH2和0.5molN2,则反应达到新的平衡时,NH3的物质的量为_____________(选填答案编号)。
A.0.3mol B.0.15mol C.小于0.15mol D.大于0.15mol,小于0.3mol
-
NH3是一种重要的化工原料,可用来制备肼、硝酸、硝酸铵和氯胺等。
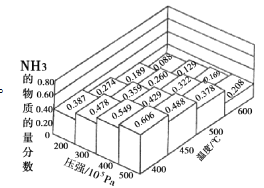
(1)N2和H2以物质的量之比为1∶3在不同温度和压强下发生反应:N2+3H2 2NH3,测得平衡体系中NH3的物质的量分数如图。
2NH3,测得平衡体系中NH3的物质的量分数如图。
①下列途径可提高氨气产率的是_____(填序号)。
a.采用常温条件 b.采用适当的催化剂 c.将原料气加压 d.将氨液化,不断移去液氨
②上图中所示的平衡体系中NH3的物质的量分数为0.549和0.478时,该反应的平衡常数分别为K1、K2,则K1 ___(选填“>”或“<”或“=”)K2。
(2)肼(N2H4)是一种火箭燃料。已知:N2(g)+2O2(g)=2NO2(g) ∆H=+67.7kJ·mol-1
N2H4(g)+O2g)=N2(g)+2H2O(g) ∆H =-534.0 kJ·mol-1
NO2(g)=1/2N2O4(g) ∆H =-28.0 kJ·mol-1
①反应2N2H4(g)+ N2O4(g)=3N2(g) + 4H2O(g)的∆H =_____ kJ·mol-1。
②氨气与次氯酸钠溶液反应生成肼的离子方程式为_________。
(3)电解硝酸工业的尾气NO可制备NH4NO3,其工作原理如图。
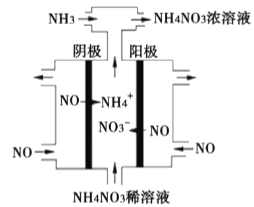
①阴极的电极反应式为__________。
②将电解生成的HNO3全部转化为NH4NO3, 则通入的NH3与实际参加反应的NO的物质的量之比至少为_________。
(4)饮用水消毒时,氯胺(NH2Cl等)在酸性条件下具有良好的效果,其原因是_____________。
-
已知:N2(g)+3H2(g) 2NH3(g) △H=-92kJ/mol。起始反应物为
2NH3(g) △H=-92kJ/mol。起始反应物为 和
和 ,物质的量之比为1:3,且总物质的量不变,在不同压强和温度下,反应达到平衡时,体系中
,物质的量之比为1:3,且总物质的量不变,在不同压强和温度下,反应达到平衡时,体系中 的物质的量分数如下表:
的物质的量分数如下表:
| 温度 压强 | 400℃ | 450℃ | 500℃ | 600℃ |
| 20MPa | 0.387 | 0.274 | 0.189 | 0.088 |
| 30MPa | 0.478 | 0.359 | 0.260 | 0.129 |
下列说法正确的是
A.体系中 的物质的量分数越大,则正反应速率越大
的物质的量分数越大,则正反应速率越大
B.反应达到平衡时, 和
和 的转化率之比为1∶1
的转化率之比为1∶1
C.反应达到平衡时,放出的热量均为92.4kJ
D.600℃,30MPa下反应达到平衡时,生成 的物质的量最多
的物质的量最多
-
一定条件下NH3(g)和NO(g)发生反应:2NH3(g)+8NO(g)  5N2O(g)+3H2O(g)。设起始时
5N2O(g)+3H2O(g)。设起始时 ,恒压下,平衡时NH3的体积分数φ(NH3)与Z和T(温度)的关系如图所示,下列说法正确的是
,恒压下,平衡时NH3的体积分数φ(NH3)与Z和T(温度)的关系如图所示,下列说法正确的是
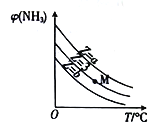
A. 升高温度,该反应的平衡常数(K)减小
B. b<3<a
C. M点对应的平衡混合物中
D. 温度不变时,M点对应的平衡在加压后φ(NH3)增大
-
如图表示平衡混和物中X的百分含量在不同的压强下,随温度变化的情况在下列平衡状态中,X可以代表用下横线标明的物质(反应中各物质均为气态)的是( )

A. N2+3H2 2NH3 +Q
2NH3 +Q
B. H2+I2 2HI +Q
2HI +Q
C. 2SO3 2SO2+O2 - Q
2SO2+O2 - Q
D. 4NH3+5O2 4NO+6H2O +Q
4NO+6H2O +Q
-
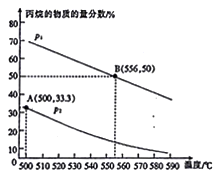
利用液化石油气中的丙烷脱氢可制取丙烯:C3H8(g) C3H6 (g)+H2 (g) △H。起始时,向一密闭容器中充入一定量的丙烷,在不同温度、压强下测得平衡时反应体系中丙烷的物质的量分数如图所示(已知pl为0.1 MPa)。
C3H6 (g)+H2 (g) △H。起始时,向一密闭容器中充入一定量的丙烷,在不同温度、压强下测得平衡时反应体系中丙烷的物质的量分数如图所示(已知pl为0.1 MPa)。
(1)反应的△H_________(填“>”“<”或“=’’,下同)
(2)以丙烯为燃料、熔融碳酸盐为电解质制作新型电池,放电时CO32-移向该电池的______(填“正极,或“负极”),当消耗2.8 L(标准状况)C3H6时,电路中转移电子的物质的量为__________。
(3)根据图中B点坐标计算,556℃时该反应酌平衡常数为______Pa(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数),若图中A、B两点对应的平衡常数用K(A)、K (B)表示,则K(A) _____(填“>” “<”或“=”)K(B)。
-
定温度、压强和有铁触媒的条件下,在密闭容器中充入N2、H2和NH3 。若起始时n(N2)=x mol、n(H2)=y mol、n(NH3)=z mol (x、y、z均不为0 ),平衡时,n(N2)=0.1mol、n(H2)=0.3mol、n(NH3)=0.08mol。下列有关判断不合理的是( )
A.x : y =1 : 3
B.N2、H2的转化率不相等
C.平衡时,H2与NH3的生成速率之比为3 : 2
D.x的取值范围为0<x<0.14
-
定温度、压强和有铁触媒的条件下,在密闭容器中充入N2、H2和NH3 。若起始时n(N2)=x mol、n(H2)=y mol、n(NH3)=z mol (x、y、z均不为0 ),平衡时,n(N2)=0.1mol、n(H2)=0.3mol、n(NH3)=0.08mol。下列有关判断不合理的是 ( )
A.x : y =1 : 3
B.N2、H2的转化率不相等
C.平衡时,H2与NH3的生成速率之比为3 : 2
D.x的取值范围为0<x<0.14

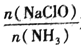 对溶液中次氯酸钠去氨氮效果与余氯(溶液中+1价氯元素的含量) 的影响如图l4所示。a点之前溶液中发生的主要反应为_______(填序号)。
对溶液中次氯酸钠去氨氮效果与余氯(溶液中+1价氯元素的含量) 的影响如图l4所示。a点之前溶液中发生的主要反应为_______(填序号)。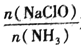 值约为______________。
值约为______________。

 对溶液中次氯酸钠去氨氮效果与余氯(溶液中+1价氯元素的含量)的影响如图所示。a点之前溶液中发生的主要反应为_______(填序号)。
对溶液中次氯酸钠去氨氮效果与余氯(溶液中+1价氯元素的含量)的影响如图所示。a点之前溶液中发生的主要反应为_______(填序号)。
 值约为______________。
值约为______________。



