一定条件下NH3(g)和NO(g)发生反应:2NH3(g)+8NO(g) 5N2O(g)+3H2O(g)。设起始时
,恒压下,平衡时NH3的体积分数φ(NH3)与Z和T(温度)的关系如图所示,下列说法正确的是
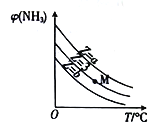
A. 升高温度,该反应的平衡常数(K)减小
B. b<3<a
C. M点对应的平衡混合物中
D. 温度不变时,M点对应的平衡在加压后φ(NH3)增大
高三化学选择题中等难度题
一定条件下NH3(g)和NO(g)发生反应:2NH3(g)+8NO(g) 5N2O(g)+3H2O(g)。设起始时
,恒压下,平衡时NH3的体积分数φ(NH3)与Z和T(温度)的关系如图所示,下列说法正确的是

A. 升高温度,该反应的平衡常数(K)减小
B. b<3<a
C. M点对应的平衡混合物中
D. 温度不变时,M点对应的平衡在加压后φ(NH3)增大
高三化学选择题中等难度题
一定条件下NH3(g)和NO(g)发生反应:2NH3(g)+8NO(g) 5N2O(g)+3H2O(g)。设起始时
,恒压下,平衡时NH3的体积分数φ(NH3)与Z和T(温度)的关系如图所示,下列说法正确的是

A. 升高温度,该反应的平衡常数(K)减小
B. b<3<a
C. M点对应的平衡混合物中
D. 温度不变时,M点对应的平衡在加压后φ(NH3)增大
高三化学选择题中等难度题查看答案及解析
在甲、乙、丙三个不同密闭容器中按不同方式投料,一定条件下发生反应(起始温度和起始体积相同): N2(g)+3H2(g)2NH3(g) △H<0,相关数据如下表所示:
| 容器 | 甲 | 乙 | 丙 |
| 相关条件 | 恒温恒容 | 绝热恒容 | 恒温恒压 |
| 反应物投料 | lmol N2、3molH2 | 2mol NH3 | 2mol NH3 |
| 平衡时容器体积 | V甲 | V乙 | V丙 |
| 反应的平衡常数K | K甲 | K乙 | K丙 |
| 平衡时NH3的浓度/mol/L | c甲 | c乙 | c丙 |
| 平衡时NH3的反应速率/mol/(L·min) | v甲 | v乙 | v丙 |
下列说法正确的是
A. V甲> V丙 B. K乙>K丙 C. c乙>c甲 D. V甲= V丙
高三化学null困难题查看答案及解析
在甲、乙、丙三个不同密闭容器中按不同方式投料,一定条件下发生反应(起始温度和起始体积相同):N2(g)+3H2(g)2NH3(g) ΔH<0,相关数据如下表所示:
| 容器 | 甲 | 乙 | 丙 |
| 相关条件 | 恒温恒容 | 绝热恒容 | 恒温恒压 |
| 反应物投料 | 1mol N2、3mol H2 | 2mol NH3 | 2mol NH3 |
| 平衡时容器体积 | V甲 | V乙 | V丙 |
| 反应的平衡常数K= | K甲 | K乙 | K丙 |
| 平衡时NH3的浓度/mol·L-1 | c甲 | c乙 | c丙 |
| 平衡时NH3的反应速率/mol·L-1·min-1 | v甲 | v乙 | v丙 |
下列说法正确的是
A.V甲>V丙 B.K乙<K丙 C.c乙>c甲 D.v甲=v丙
高三化学选择题困难题查看答案及解析
在甲、乙、丙三个不同密闭容器中按不同方式投料,一定条件下发生反应(起始温度和起始体积相同):N2(g)+3H2(g)2NH3(g) ΔH<0,相关数据如下表所示:
| 容器 | 甲 | 乙 | 丙 |
| 相关条件 | 恒温恒容 | 绝热恒容 | 恒温恒压 |
| 反应物投料 | 1mol N2、3mol H2 | 2mol NH3 | 2mol NH3 |
| 平衡时容器体积 | V甲 | V乙 | V丙 |
| 反应的平衡常数K= | K甲 | K乙 | K丙 |
| 平衡时NH3的浓度/mol·L-1 | c甲 | c乙 | c丙 |
| 平衡时NH3的反应速率/mol·L-1·min-1 | v甲 | v乙 | v丙 |
下列说法正确的是
A.V甲>V丙 B.K乙>K丙 C.c乙>c甲 D.v甲=v丙
高三化学选择题困难题查看答案及解析
在甲、乙、丙三个不同密闭容器中按不同方式投料,一定条件下发生反应(起始温度和起始体积相同):N2(g)+3H2(g)2NH3(g) △H<0相关数据如下表所示下列说法正确的是
| 容器 | 甲 | 乙 | 丙 |
| 相关条件 | 恒温恒容 | 绝热恒容 | 恒温恒压 |
| 反应物投料 | 1molN2、3mol的H2 | 2mol的NH3 | 2mol的NH3 |
| 平衡时容器体积 | V甲 | V乙 | V丙 |
| 反应平衡常数K=c2(NH3)/c(N2)∙c3(H2) | K甲 | K乙 | K丙 |
| 平衡时NH3的浓度(mol/L) | C甲 | C乙 | C丙 |
| 平衡时NH3的反应速率(mol/L∙min) | v甲 | v乙 | v丙 |
A.V甲>V乙 B.K乙>K丙 C.c乙>c甲 D.υ甲=υ丙
高三化学选择题困难题查看答案及解析
在甲、乙、丙三个不同密闭容器中,按不同方式投料,起始浓度和起始容积相同,一定条件下发生反应:N2(g)+3H2(g) 2NH3(g) △H
下列说法正确的是( )
A. V甲>V乙 B. K丙>K乙 C. V甲=V丙 D. c乙>c甲
高三化学选择题中等难度题查看答案及解析
一定条件下,在一固定容积的密闭容器中发生如下反应:N2(g)+3H2(g)2NH3(g),若开始时只充入2a mol NH3,达到平衡时,混合气体的压强比起始时增大了40%。若同条件下开始时充入a mo N2和3a mol H2的混合气体,求:
(1)达到平衡时H2的转化率;
(2)平衡时NH3在混合气体中的体积分数。
一定条件下,在一固定容积密闭容器中发生如下反应:N2(g)+3H2(g)2NH3(g),若开始时只充入2a mol NH3,达到平衡时,混合气体的压强比起始时增大了40%。若开始时充入a mo N2和3a mol H2的混合气体,求:
(1)达到平衡时H2的转化率;
(2)平衡时NH3在混合气体中的体积分数。
高三化学选择题中等难度题查看答案及解析
工业上,在催化剂条件下,用NH3作为还原剂将烟气中的NOx还原成无害的氢气和水,反应方程式可表示为:2NH3(g)+NO(g)+NO2(g)2N2(g)+3H2O(g)
(1)一定条件下,在容积为2L的容器内进行该反应,20min时达到平衡,生成N2 0.4mol,则平均反应速率v(NO)=___________________。可从混合气体的颜色变化判断上述反应是否达到平衡,其理由是_______________________________________________。
(2)工业上也用氨水吸收SO2尾气,最终得到(NH4)2SO4,(NH4)2SO4溶液中c(NH4+)与c(SO42-)之比____2:1(选填“>”、“<”、“=”),用离子方程式解释其原因______________________。
(3)与Cl2相比较,ClO2处理水时被还原成Cl-,不生成有机氯代物等有害物质。工业上可用亚铝酸钠和稀盐酸为原料制备ClO2,反应如下:NaClO2+HCl→ClO2↑+NaCl+_____(没有配平)
(4)补全方程式并配平,标出电子转移方向和数目_________________________ 。
(5)该反应中氧化剂和还原剂的物质的量之比是___________。若生成0.2molClO2,转移电子数为_____个。
高三化学综合题中等难度题查看答案及解析
下列说法中,能说明化学平衡一定向正反应方向移动的是
A.N2O4(g) 2NO2(g),改变某一条件后,气体颜色加深
B.N2(g) + 3H2(g) 2NH3(g),改变某一条件后,NH3的体积分数增加
C.H2(g) + I2(g) 2HI(g),单位时间内消耗H2和HI的物质的量之比大于1∶2
D.2SO2(g) + O2(g) 2SO3(g),恒温恒压条件下,充入He
高三化学选择题中等难度题查看答案及解析
低温脱硝技术可用于处理废气中的氮氧化物,发生的化学反应为:
2NH3(g)+NO(g)+NO2(g) 2N2(g)+3H2O
在恒容的密闭容器中,下列有关说法正确的是
A. 平衡时,其他条件不变,升高温度可使该反应的平衡常数增大
B. 平衡时,其他条件不变,增加NH3的浓度,废气中氮氧化物的转化率减小
C. 单位时间内消耗NO和N2的物质的量比为1:2时,反应达到平衡
D. 其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大
高三化学选择题简单题查看答案及解析