A.CH3OH
B.CO2
C.空气
D.H2O
高三化学选择题中等难度题

高三化学选择题中等难度题

高三化学选择题中等难度题查看答案及解析
清洁能源具有广阔的开发和应用前景,可减少污染解决雾霾问题,其中甲醇、甲烷是优质的清洁燃料,可制作燃料电池.
一定条件下用CO和H2合成CH3OH:CO(g)+2H2(g)⇌CH3OH(g)△H=﹣105kJ•mol﹣1.向体积为2L的密闭容器中充入2molCO和4molH2,测得不同温度下容器内的压强(P:kPa)随时间(min)的变化关系如图中Ⅰ、Ⅱ、Ⅲ曲线所示:

(1)Ⅱ和Ⅰ相比,改变的反应条件是 .
(2)反应Ⅰ在6min时达到平衡,在此条件下从反应开始到达到平衡时v(CH3OH)= .
(3)反应Ⅱ在2min时达到平衡,平衡常数K(Ⅱ)= .
(4)比较反应Ⅰ的温度(T1)和反应Ⅲ的温度(T3)的高低:T1 T3(填“>”“<”“=”),判断的理由是 .
高三化学填空题困难题查看答案及解析
(15分)清洁能源具有广阔的开发和应用前景,可减少污染解决雾霾问题,其中甲醇、甲烷是优质的清洁燃料,可制作燃料电池。
Ⅰ、一定条件下用CO和H2合成CH3OH:CO(g)+2H2 (g)CH3OH(g)△H=﹣105kJ•mol﹣1.向体积为2L的密闭容器中充入2mol CO和4mol H2,测得不同温度下容器内的压强(P:kPa)随时间(min)的变化关系如右图中Ⅰ、Ⅱ、Ⅲ曲线所示:

(1)Ⅱ和Ⅰ相比,改变的反应条件是 .
(2)反应Ⅰ在6min时达到平衡,在此条件下从反应开始到达到平衡时v(CH3OH)= .
(3)反应Ⅱ在2min时达到平衡,平衡常数K(Ⅱ)= .
(4)比较反应Ⅰ的温度(T1)和反应Ⅲ的温度(T3)的高低:T1 T3(填“>”“<”“=”),判断的理由是 .
Ⅱ、甲烷和甲醇可以做燃料电池,具有广阔的开发和应用前景,回答下列问题:
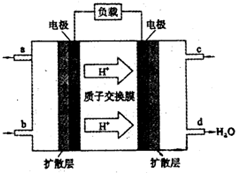
(5)甲醇燃料电池(简称DMFC)由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注。DMFC工作原理如右图所示:

通入a气体的电极是原电池的 极(填 “正”或“负”),其电极反应式为 。
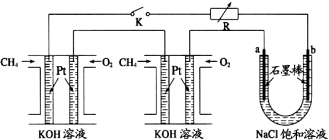
(6)某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验,如图所示U形管中氯化钠溶液的体积为800ml。闭合K后,若每个电池甲烷用量均为0.224L(标况),且反应完全,则理论上通过电解池的电量为 (法拉第常数F=9.65×104C/mol),若产生的气体全部逸出,电解后溶液混合均匀,电解后U形管中溶液的pH为 。
高三化学填空题简单题查看答案及解析
镁燃料电池作为一种高能化学电源,具有良好的应用前景。下图是镁一空气燃料电池工作原理示意图。下列有关该电池的说法正确的是
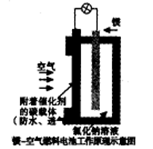
A.该电池Mg作负极,发生还原反应
B.该电池的正极反应式为:
C.电池工作时,电子通过导线由碳电极流向Mg电极
D.当电路中通过0.2mol电子时,消耗的O2体积为1.12L
高三化学选择题中等难度题查看答案及解析
镁燃料电池作为一种高能化学电源,具有良好的应用前景。下图是镁—空气燃料电池工作原理示意图。下列有关该电池的说法正确的是( )
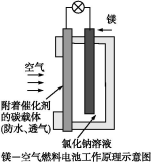
A.该电池Mg作负极,发生还原反应
B.该电池的正极反应式为:O2+2H2O+4e-=4OH-
C.电池工作时,电子通过导线由碳电极流向Mg电极
D.当电路中通过0.2 mol电子时,消耗的O2体积为1.12 L
高三化学选择题中等难度题查看答案及解析
甲醇是一种可再生能源,又是一种重要的化工原料.具有广阔的开发和应用前景。工业上可用如下方法合成甲醇:CO(g)+2H2(g)CH3OH(g).
(1) 已知:①2CH3OH(l)+3O2(g)2CO2(g)+4H2O(g) △H=-1275.6kJ·mol-1;
②2CO(g)+O2(g)2CO2(g) △H=-566.0kJ·mol-1;
③H2O(l)=H2O(g) △H=+44.0kJ·mol-1.
则甲醇液体不完全燃烧生成CO和液态水的热化学方程式为__________。
(2) 在一定温度下,向2L密闭容器中充人1mol CO和2mol H2,发生反应CO(g)+2H2(g)CH3OH(g),5min反应达到平衡,此时CO的转化率为80%。
①前5min内甲醇的平均反应速率为__________;已知该反应在低温下能自发进行,则反应的△H_______0(填“>”“<”或“=”)。
②在该温度下反应的平衡常数K=__________。
③某时刻向该平衡体系中加人CO、H2、CH3OH各0.2mol后,则v正__________v逆(填“>”“=”或“<”)。
④当反应达到平衡时,__________(填字母)。
a.混合气体的压强不再发生变化 b.反应物不再转化为生成物
c.v正(CO)=2v逆(H2) d.v(H2)=2v(CH3OH)
e.三种物质的浓度比恰好等于化学方程式中各物质的化学计量数之比
(3) "甲醇---过氧化氢燃料电池"的结构主要包括燃料腔、 氧化剂腔和质子交换膜三部分.放电过程中其中一个腔中生成了CO2。
①放电过程中生成H+的反应,发生在__________腔中,该腔中的电极反应式为__________.
②该电池工作过程中,当消耗甲醇4.8g时.电路中通过的电量为__________(法拉第常数F=9.65×104C·mol-1)
高三化学综合题中等难度题查看答案及解析
高三化学填空题中等难度题查看答案及解析
甲醇作为基本的有机化工产品和环保动力燃料具有广阔的应用前景,CO2 加氢合成甲醇是合理利用 CO2 的有效途径.由 CO2 制备甲醇过程可能涉及反应如下:
反应Ⅰ:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)△H1=﹣49.58kJ•mol﹣1
反应Ⅱ:CO2(g)+H2(g)⇌CO (g)+H2O(g)△H2
反应Ⅲ:CO(g)+2H2(g)⇌CH3OH(g)△H3=﹣90.77kJ•mol﹣1,回答下列问题:
(1)反应Ⅱ的△H2= ,反应 I 自发进行条件是 (填“较低温”、“较高温”或“任何温度”).
(2)在一定条件下 3L 恒容密闭容器中,充入一定量的 H2和 CO2 仅发生反应Ⅰ,实验测得反应物在不同起始投入量下,反应体系中 CO2的平衡转化率与温度的关系曲线,如图 1 所示.
①H2和 CO2的起始的投入量以 A 和 B 两种方式投入
A:n(H2)=3mol,n(CO2)=1.5mol
B:n(H2)=3mol,n(CO2)=2mol,曲线 I 代表哪种投入方式 (用 A、B 表示)
②在温度为 500K 的条件下,按照 A 方式充入 3mol H2 和 1.5mol CO2,该反应 10min 时达到平衡:
a.此温度下的平衡常数为 ;500K 时,若在此容器中开始充入 0.3molH2和 0.9mol CO2、0.6molCH3OH、xmolH2O,若使反应在开始时正向进行,则 x 应满足的条件是 .
b.在此条件下,系统中 CH3OH 的浓度随反应时间的变化趋势如图 2 所示,当反应时间达到 3min时,迅速将体系温度升至 600K,请在图2中画出 3~10min 内容器中 CH3OH 浓度的变化趋势曲线.
(3)固体氧化物燃料电池是一种新型的燃料电池,它是以固体氧化锆氧化钇为电解质,这种固体 电解质在高温下允许氧离子(O2﹣)在其间通过,该电池的工作原理如图 3 所示,其中多孔电极均 不参与电极反应,图3是甲醇燃料电池的模型.
①写出该燃料电池的负极反应式 .
②如果用该电池作为电解装置,当有 16g 甲醇发生反应时,则理论上提供的电量最多为 mol.
高三化学填空题困难题查看答案及解析
甲醇燃料电池被认为是21世纪电动汽车的最佳候选动力源,其工作原理如图所示。下列有关叙述正确的是( )。
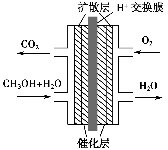
A.通氧气的一极为负极
B.H+从正极区通过交换膜移向负极区
C.通甲醇的一极的电极反应式为CH3OH+H2O-6e-=CO2↑+6H+
D.甲醇在正极发生反应,电子经过外电路流向负极
高三化学选择题中等难度题查看答案及解析
甲烷和甲醇可以做燃料电池,具有广阔的开发和应用前景,回答下列问题
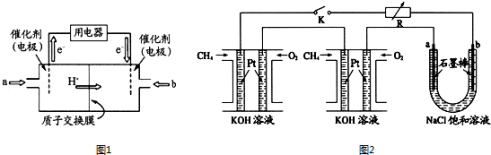
(1)甲醇燃料电池(简称DMFC)由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注.DMFC工作原理如图1所示:通入a气体的电极是原电池的 极(填“正”“负”),其电极反应式为 .
(2)某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验,如图2所示U形管中氯化钠溶液的体积为800ml.闭合K后,若每个电池甲烷用量均为0.224L(标况),且反应完全,则理论上通过电解池的电量为 (法拉第常数F=9.65×104C/mol),若产生的气体全部逸出,电解后溶液混合均匀,电解后U形管中溶液的pH为 .
高三化学填空题困难题查看答案及解析