-
工业合成氨的原理为N2(g)+3H2(g) 2NH3(g),请回答下列问题:
2NH3(g),请回答下列问题:
(1)已知拆开1mol H﹣H键、1mol N≡N、1mol N﹣H键分别需要吸收的能量为436kJ、946kJ、391kJ。则由N2和H2反应生成1mol NH3需要放出_________的热量。
(2)若N2、H2、NH3的起始浓度依次为0.2mol/L、0.3mol/L、0.2mol/L,当反应达平衡时,浓度分别是a、b、c(mol/L),则各物质的浓度有可能的是___________。
A.c=0.5mol/L B.b=0.5mol/L
C.c=0.4mol/L D.a=0.3mol/L
(3)若在2L密闭容器中,充入1 mol N2和3mol H2,2min时达到平衡。测得平衡时N2的浓度为0.3 mol/L。
①2min内v(NH3)=___________。
②平衡时容器的压强与起始时压强之比___________。
-
工业合成氨的反应N2+3H2===2NH3的能量变化如图所示,请回答有关问题:
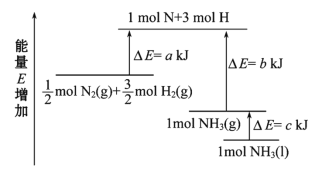
(1)合成1 mol NH3(l)________(填“吸收”或“放出”)________ kJ的热量。
(2)已知:拆开 1 mol H—H键、1 mol N—H键、1 mol N≡N 键分别需要的能量是436 kJ、391 kJ、946 kJ。则图中的a=________ kJ;1 mol N2(g) 完全反应生成NH3(g)产生的能量变化为________ kJ。
(3)推测反应 2NH3(l)=== 2N2 (g)+3H2(g) 比反应2NH3(g)=== 2N2 (g)+3H2(g) ______(填“吸收”或“放出”)的热量________(填“多”或“少”)。
-
(16分)I.(4分)已知拆开1mol H—H键,1mol N三N键分别需要吸收的能量为436kJ,946kJ;形成1mol N—H键,会放出能量391kJ,在反应N2 + 3H2== 2NH3中,每生成2mol NH3 ___ _热量(填:吸收或放出)_____ kJ。
II.(6分)我国经济发展对能源的需求与日俱增。一种新型燃料电池是将两根特制电极插入氢氧化钾溶液中,然后从两极分别通入甲烷和氧气,其电极反应式为:
X极:CH4+10OH- -8e- == CO32-+7H2O Y极:4H2O+2O2+8e- ==8OH-
(1)指出该电池的正极__________(X或Y)极
(2)在标准状况下,通入5.6L甲烷气体,完全反应后有__________mol电子转移;
(3)该电池的电解质溶液的PH变化是_______ ___(填升高、降低、不变)
III.(6分)利用Cu + 2FeCl3 = CuCl2 + 2FeCl2反应,设计一个原电池。
(1)画出装置图(在图中标出电极材料、正负极、电解质溶液)。
(2)写出电极反应方程式
负极: 正极:
-
(4分)已知拆开1mol H—H键, 1mol N三N键分别需要吸收的能量为436kJ , 946kJ;形成1mol N—H键,会放出能量391kJ,在反应N2 + 3H2  2NH3中,每生成2mol NH3 ____热量(填:吸收或放出)_____kJ(各2分)。
2NH3中,每生成2mol NH3 ____热量(填:吸收或放出)_____kJ(各2分)。
-
已知拆开1mol H–H键, 1mol N≡N键分别需要吸收的能量为436kJ 、946kJ;形成1mol N–H键,会放出能量391kJ,在反应N2 + 3H2  2NH3中,每生成2mol NH3,
2NH3中,每生成2mol NH3,
A.放出92 kJ热量 B.吸收92 kJ热量
C.放出209kJ热量 D.吸收209kJ热量
-
工业合成氨的反应:N2(g)+3H2(g)  2NH3(g)是一个可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知形成1mol H-H键、1mol N—H键、1mol N
2NH3(g)是一个可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知形成1mol H-H键、1mol N—H键、1mol N N键放出的能量分别为436KJ、391KJ、946KJ。则:
N键放出的能量分别为436KJ、391KJ、946KJ。则:
(1)若1mol N2完全反应生成NH3可______(填“吸收”或“放出)热量_____KJ。
(2)如果将1mol N2 和 3mol H2混合,在一定条件下使其充分反应,反应放出的热量总小于上述数值,其原因是_____________________________________________________。
(3)实验室模拟工业合成氨时,在容积为2L的密闭容器中进行,反应经过10min后,生成10mol NH3,则用N2表示的化学反应速率是________mol·L -1·min-1。
(4)一定条件下,当成合成氨反应达到化学平衡时,下列说法正确的是(____)
a.正反应速率和逆反应速率相等
b.正反应速率最大,逆反应速率为0
c.N2的转化率达到最大值
d. N2和H2的浓度相等
e.N2、H2和NH3的体积分数相等
f.反应达到最大限度
-
已知拆开1mol H-H键,1mol N三N键分别需要吸收的能量为436kJ,946kJ;形成1mol N-H键,会放出能量391kJ,在反应N2+3H2
 2NH3中,每生成2mol NH3,________热量(填:吸收或放出)________ kJ.
2NH3中,每生成2mol NH3,________热量(填:吸收或放出)________ kJ.
-
工业上合成氨反应为:N2+3H2 2NH3,回答下列问题:
2NH3,回答下列问题:
(1)反应过程中拆开的化学键是_______;
(2)反应放热,从价键角度分析,反应放热的原因是_______,下列图像正确的是_______。

(3)在体积是2L的密闭容器中开始加入1molN2,3molH2,反应过程浓度中,物质的浓度与时间的关系如图所示。
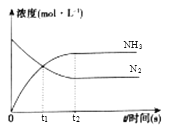
①t1时生成NH3的物质的量是_______;用H2表示的化学反应速率υ(H2)=_______。
②下列各项能表明反应达到化学平衡状态的是_______。
A.容器中气体的密度保持不变
B.容器中气体的压强不变
C.氨气的含量不变
D.拆开3molH—H键同时形成6molN—H键
(4)下列措施中能提高合成氨反应化学反应速率的是_______。
A.使用高效催化剂 B.恒温恒容再充入氢气 C.降低反应温度 D.扩大容器体积
-
工业合成氨反应:N2+3H2  2NH3是一个放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知形成1 mol H-H键、1 mol N-H键、N≡N1mol键放出的能量分别为436 kJ、391 kJ、946 kJ。则:
2NH3是一个放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知形成1 mol H-H键、1 mol N-H键、N≡N1mol键放出的能量分别为436 kJ、391 kJ、946 kJ。则:
(1)若1 mol N2完全反应生成NH3可___(填“吸收”或“放出”)热量___kJ。
(2)如果将1 mol N2和3 mol H2混合,使其充分反应,放出的热量总小于上述数值,其原因是_______________________。
(3)实验室模拟工业合成氨时,在容积为2L的密闭容器内,反应经过10 min后,生成10 mol NH3,则用N2表示的化学反应速率为_____mol/(L·min)。
(4)一定条件下,当合成氨反应达到化学平衡时,下列说法正确的是________
A.正反应速率和逆反应速率相等 B.正反应速率最大,逆反应速率为0
C.N2的转化率达到最大值 D.N2和H2的浓度相等
E.N2、H2和NH3的体积分数相等 F.反应达到最大限度
-
合成氨是工业上的重要反应:N2(g)+3H2(g) 2NH3(g),下列说法不正确的是
2NH3(g),下列说法不正确的是
A. 反应达平衡状态后,各物质浓度不变,反应停止
B. 反应达平衡状态后,单位时间内生成1mol N2的同时消耗3mol H2
C. 在上述条件下,N2不可能100%转化为NH3
D. 使用催化剂是为了加快反应速率,提高生产效率
2NH3(g),请回答下列问题:


