-
钛(Ti)因为具有神奇的性能越来越引起人们的关注,是航空、军工、电力等方面的必需材料,被誉为“空间金属”和“深海金属”。
(1)钛和钛的合金具有很多优良的性能,如熔点高、密度小、可塑性好、易于加工,钛合金与人体有很好的“相容性”。根据它们的主要性能,下列用途不切合实际的是________。
A.用来做保险丝 B.用于制造航天飞机
C.用来制造人造骨 D.用于制造船舶
(2)常温下钛不和非金属、强酸反应。红热时,却可与常见的非金属单质反应。地壳中含钛矿石之一称金红石(TiO2),目前大规模生产钛的方法是:
第一步:金红石、炭粉混合,在高温条件下通入氯气制得TiCl4和一种可燃性气体。该反应的化学方程式:______________________,该反应的还原剂是 ________________________________________________________________________。
第二步:在氩气的气氛中,用过量镁在加热条件下与TiCl4反应制得金属钛。
简述由上述所得产物中获取金属钛的步骤____________________。
高三化学填空题中等难度题查看答案及解析
-
钛因为具有神奇的性能越来越引起人们的关注,常温下钛不和非金属、强酸反应,红热时,却可与常见非金属单质反应。钛是航空、军工、电力等方面的必需原料。地壳中含钛矿石之一为金红石(TiO2),目前大规模生产Ti的方法是:
第一步:金红石、炭粉混合物在高温条件下通入Cl2制得TiCl4和一种可燃性气体。该反应的化学方程式为____________________,该反应的还原剂为________。
第二步:在氩气的气氛中,用过量的Mg在加热条件下与TiCl4反应制得金属钛。
(1)写出此反应的化学方程式:____________________________。
(2)如何由上述所得的产物中获取金属钛?简述实验步骤并写出有关的化学方程式。
________________________________________________________________________________
高三化学填空题简单题查看答案及解析
-
钛有“生物金属”和“未来金属”之称,钛及其化合物的应用正越来越受到人们的关注。
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。
①TiCl4熔点为-24℃,沸点为136.4℃,室温下为无色液体,可溶于甲苯和氯代烃,固态T'iCl4属于________晶体。
②LiBH4中BH4-的空间构型是_________,B原子的杂化轨道类型是________。
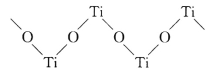
(2)硫酸氧钛晶体中阳离子为链状聚合形式的离子,部分结构如图所示。该阳离子Ti与O的原子个数之比为________,其化学式为_____________________。
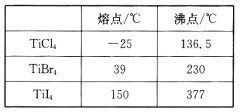
(3)钛与卤素形成的化合物的熔、沸点如表所示,分析TiCl4、TiBr4、TiI4的熔点和沸点呈现一定规律的原因:______________________________。
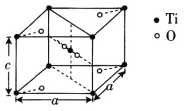
(4)TiO2晶胞是典型的四方系结构,其晶胞结构如图所示,晶胞参数为a nm和c nm,设NA为阿伏加德罗常数的值,该晶体的密度为___________(写出表达式)g·cm-3。
高三化学综合题中等难度题查看答案及解析
-
钛和钛的合金已被广泛用于制造电讯器材、人造骨骼、化工设备、飞机等航天航空材料,被誉为“未来世界的金属”。试回答下列问题:
(1)钛有
Ti和
Ti两种原子,它们互称为 。Ti元素在元素周期表中的位置是第 周期,第 族;基态原子的电子排布式为 ;按电子排布Ti元素在元素周期表分区中属于 区元素
(2)偏钛酸钡在小型变压器、话筒和扩音器中都有应用。偏钛酸钡晶体中晶胞的结构如图所示,它的化学式是
(3)二氧化钛作光催化剂能将居室污染物甲醛、苯等有害气体可转化为二氧化碳和水,达到无害化。有关甲醛、苯、二氧化碳及水说法正确的是 。
A.苯与B3N3H6互为等电子体
B.甲醛、苯分子中碳原子均采用sp2杂化
C.苯、二氧化碳是非极性分子,水和甲醛是极性分子
D.水的沸点比甲醛高得多,是因为水分子间能形成氢键
高三化学填空题困难题查看答案及解析
-
钛(22Ti)由于其特殊的性能被誉为“未来世纪的金属”。钛铁矿主要成分为FeTiO3(含有少量MgO、SiO2等杂质),Li4Ti5O12和LiFePO4都是锂离子电池的电极材料,可利用钛铁矿来制备,工艺流程如下:
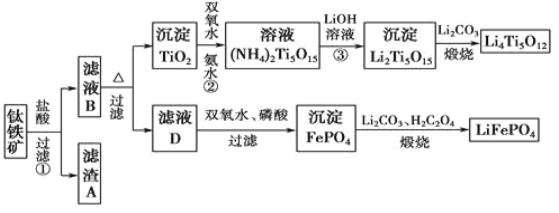
(1)Ti位于元素周期表中的位置为________。钛铁矿在预处理时需要进行粉碎,其原因是_______。
(2)过程①中,铁的浸出率结果如图所示。由图可知,当铁的浸出率为80%时,所采用的实验条件是_________。

(3)过程②中固体TiO2与双氧水、氨水反应转化成(NH4)2Ti5O15溶液时,Ti元素的浸出率与反应温度的关系如图所示,反应温度过高时,Ti元素浸出率下降的原因是___________。

(4)写出由滤液D生成FePO4的离子方程式____________________________________。
(5)由流程图可知FePO4制备LiFePO4的化学方程式是_________________________。
高三化学综合题中等难度题查看答案及解析
-
钛(22Ti)由于其特殊的性能被誉为“未来世纪的金属”。钛铁矿主要成分为FeTiO3(含有少量MgO、SiO2等杂质),Li4Ti5O12和LiFePO4都是锂离子电池的电极材料,可利用钛铁矿来制备,工艺流程如下:

⑴钛铁矿在预处理时需要进行粉碎,其原因是__________________________________。
⑵过程①中,铁的浸出率结果如图所示。由图可知,当铁的浸出率为80%时,所采用的实验条件是_________________________。

⑶过程②中固体TiO2与双氧水、氨水反应转化成(NH4)2Ti5O15溶液时,Ti元素的浸出率与反应温度关系如图所示,反应温度过高时,Ti元素浸出率下降的原因是_______________________。
⑷写出由滤液D生成FePO4的离子方程式_____________________________________________
⑸由流程图可知FePO4制备LiFePO4的化学方程式是_________________________。
高三化学工业流程简单题查看答案及解析
-
地球表面十公里厚的地层中,含钛元素达千分之六,比铜多61倍,金属钛(Ti)被誉为21世纪金属,其单质和化合物具有广泛的应用价值。氮化钛(Ti3N4)为金黄色晶体,由于具有令人满意的仿金效果,越来越多地成为黄金的代替品。以TiCl4为原料,经过一系,列反应可以制得Ti3N4和纳米TiO2(如下图)。

图中的M是短周期金属元素,M的部分电离能如下表:
I1
I2
I3
I4
I5
电离能/(kJ·mol-1)
738
1451
7733
10 540
13 630
请回答下列问题:
⑴TiO2为离子晶体,己知晶体中阳离子的配位数为6,阴离子的配位数为3,则阳离子的电子排布式为___________
⑵金属Ti与金属M的晶体原子堆积模式相同,其堆积模型为_________(填写堆积模型名称),晶体中原子在二维平面里的配位数为_____________
⑶室温下TiCl4为无色液体,沸点为136.4℃,由此可知其晶体类型为__________,构成该晶体的粒子的空间构型为_____________
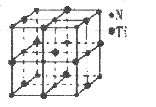
(4)有一种氮化钛晶体的晶胞与NaCl晶胞相似,如下图所示,已知该氮化钛的密度为p g·cm-3,则该晶胞中N、Ti之间的最近距离为_____ pm,(NA为阿伏加德常数的数值,只列算式)。该晶体中与Ti原子距离相等且最近的Ti原子有___________个。
(5)科学家通过X射线探明KC1、MgO、CaO、TiN的晶体与NaCl的晶体结构相似。且知三种离子晶体的晶格能数据如下:
离子晶体
NaCl
KC1
CaO
晶格能/(kJ·mol-1)
786
715
3401
KC1、CaO、TiN三种离子晶体硬度由低到该的顺序为_____________
高三化学简答题中等难度题查看答案及解析
-
钛及其合金具有密度小,强度高,耐腐蚀等优良性能,被广泛用于航天、航空、航海、石油化工、医药等部门,因此,钛被誉为第三金属和战略金属。从钛铁矿提取金属钛(海绵钛)的主要工艺过程如下:

(1)钛铁矿的主要成分是FeTiO3,第一步发生的反应:FeTiO3+C
TiO2+Fe+CO↑,在FeTiO3(钛酸亚铁)中,钛的化合价为________。
(2)第二步:二氧化钛在高温下与焦炭、氯气反应生成四氯化钛和一氧化碳,写出化学方程式:___________,还原产物是____________。
(3)用镁在高温下还原四氯化钛,该反应的环境要求是__________;写出化学方程式:___________。
(4)菱镁矿(主要成分是碳酸镁)煅烧后与焦炭混合在氯化器中高温下通入氯气生成氯化镁,电解熔融氯化镁得到镁。
①写出菱镁矿煅烧及氯化制取氯化镁的化学方程式:______________;
②写出电解熔融氯化镁的电解方程式:____________________。
高三化学工业流程中等难度题查看答案及解析
-
【化学-物质结构与性质】
钛和钛的合金已被广泛用于制造电讯器材、人造骨骼、化工设备、飞机等航天航空材料,被誉为“未来世界的金属”.试回答下列问题:
(1)钛有2248和2250Ti两种原子,它们互称为______.Ti元素在元素周期表中的位置是第______周期,第______族;基态原子的电子排布式为______按电子排布Ti元素的元素周期表分区中属于______区元素.
(2)偏钛酸钡在小型变压器、话筒和扩音器中都有应用.偏钛酸钡晶体中晶胞的结构如右图所示,它的化学式是______.
(3)现有含Ti3+的配合物,化学式为[TiCl(H2O)5]Cl2•H2O.配离子[TiCl(H2O)5]2+中含有的化学键类型是______,该配合物的配体是______.高三化学解答题中等难度题查看答案及解析
-
[选做题——物质结构与性质]
金属钛(Ti)是一种具有许多优良性能的的金属,钛和钛合金被认为是21世纪的重要金属材料。
(l) Ti(BH4)2是一种过渡元素硼氢化物储氢材料。
① Ti2+基态的电子排布式可表示为_____________________。
② BH4-的空间构型是______________________(用文字描述)。
③ 与钛同周期的所有元素的基态原子中,未成对电子数与钛相同的元素有__________种。
(2)二氧化钛(TiO2)是常用的、具有较高催化活性和稳定性的光催化剂,常用于污水处理。
①纳米TiO2催化的一个实例如下图所示。
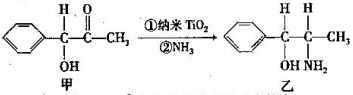
化合物甲的分子中采取
杂化方式的碳原子个数为______________, 化合物乙中采取
杂化的原子的第一电离能由小到大的顺序为________________。
②在 TiO2催化作用下,可将CN-氧化成CNO-,进而得到N2。与CNO-互为等电子体的分子、离子化学式分别为_________________、_______________(各写一种)。
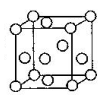
(3)金属钛内部原子的堆积方式与铜相同,都是面心立方堆积方式,如图。若该晶胞的密度为
,阿伏加德罗常数为
,则该晶胞的边长为______________cm。
高三化学填空题简单题查看答案及解析