-
铜单质及其化合物在很多领域中都有重要的用途。请回答以下问题:
(1)超细铜粉可用作导电材料、催化剂等,其制备方法如下:

①NH4CuSO3中金属阳离子的核外电子排布式为______。N、O、S三种元素的第一电离能大小顺序为______________(填元素符号)。
②SO42-的空间构型为________,与SO42-互为等电子体的有机分子的化学式为_________。
(2)某学生用硫酸铜溶液与氨水做了一组实验,CuSO4溶液中加氨水生成蓝色沉淀,再加氨水沉淀溶解,得到深蓝色透明溶液,最后向该溶液中加入一定量乙醇,析出[Cu(NH3)4]SO4·H2O晶体,请解释加入乙醇后析出晶体的原因_______________;在该晶体中存在的化学键的种类有_____________。
(3)氯和钾与不同价态的铜可生成两种化合物,其阴离子均为无限长链结构(如图所示),a位置上Cl原子的杂化轨道类型为________。已知其中一种化合物的化学式为KCuCl3,则另一种化合物的化学式为____________。

(4)用晶体的X射线衍射法可以测得阿伏加德罗常数的值。对金属铜的测定得到以下结果:铜晶胞为面心立方最密堆积,边长为361 pm。又知铜的密度为9.00 g·cm-3,则铜原子的直径约为__________pm,求算阿伏加德罗常数的表达式为________。
-
(14分)铜单质及其化合物在很多领域有重要的用途,如超细铜粉可应用于导电材料、催化剂等领域中。超细铜粉的某制备方法如下:

(1)[Cu(NH3)4]SO4中,N、O、S三种元素的第一电离能从大到小的顺序为: 。
(2) SO42-中硫原子的杂化轨道类型是 :写出一种与SO42-互为等电子体的分子 。
(3)某反应在超细铜粉做催化剂作用下生成 ,则分子中 σ 键与 π 键之比为
,则分子中 σ 键与 π 键之比为
(4)该化合物[Cu(NH3)4]SO4中存在的化学键类型有 。(填字母)
A.离子键 B.金属键 C.配位键 D.非极性键 E.极性键
(5)NH4CuSO3中的金属阳离子的核外电子排布式为 。
(6)铜的某氯化物的晶胞结构如图所示,该化合物的化学式为 。

-
铜单质及其化合物在很多领域有重要的用途,如超细铜粉可应用于导电材料、催化剂等领域中。超细铜粉的某制备方法如下:

(1)[Cu(NH3)4]SO4中,N、O、S三种元素的第一电离能从大到小的顺序为:________。
(2) SO42-中硫原子的杂化轨道类型是________:写出一种与SO42-互为等电子体的分子________。
(3)某反应在超细铜粉做催化剂作用下生成 ,则分子中 σ 键与 π 键之比为________
,则分子中 σ 键与 π 键之比为________
(4)该化合物[Cu(NH3)4]SO4中存在的化学键类型有________。(填字母)
A.离子键 B.金属键 C.配位键 D.非极性键 E.极性键
(5)NH4CuSO3中的金属阳离子的核外电子排布式为________。
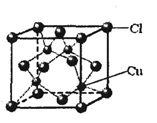
(6)铜的某氯化物的晶胞结构如右图所示,该化合物的化学式为________。
-
铜单质及其化合物在很多领域有重要的用途,如超细铜粉可应用于导电材料、催化剂等领域中.超细铜粉的某制备方法如下:

(1)[Cu(NH3)4]SO4中,N、O、S三种元素的第一电离能从大到小的顺序为:________.
(2)SO42-中硫原子的杂化轨道类型是________:写出一种与SO42-互为等电子体的分子________.
(3)某反应在超细铜粉做催化剂作用下生成 ,则分子中σ键与π键之比为________
,则分子中σ键与π键之比为________
(4)该化合物[Cu(NH3)4]SO4中存在的化学键类型有________.(填字母)
A.离子键 B.金属键 C.配位键 D.非极性键 E.极性键
(5)NH4CuSO3中的金属阳离子的核外电子排布式为________.
(6)铜的某氯化物的晶胞结构如图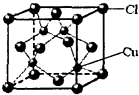 所示,该化合物的化学式为________.
所示,该化合物的化学式为________.
-
铜单质及其化合物在很多领域有重要的用途,如超细铜粉可应用于导电材料、催化剂等领域中。超细铜粉的某制备方法如下:

(1)[Cu(NH3)4]SO4中,N、O、S三种元素的第一电离能从大到小的顺序为:________。
(2) SO42-中硫原子的杂化轨道类型是________:写出一种与SO42-互为等电子体的分子________。
(3)某反应在超细铜粉做催化剂作用下生成 ,则分子中 σ 键与 π 键之比为________。
,则分子中 σ 键与 π 键之比为________。
(4)该化合物[Cu(NH3)4]SO4中存在的化学键类型有________。(填字母)
A.离子键; B.金属键; C.配位键; D.非极性键;E.极性键
(5)NH4CuSO3中的金属阳离子的核外电子排布式为________。
(6)铜的某氯化物的晶胞结构如图所示,该化合物的化学式为________。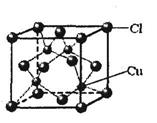
-
铜、铁都是日常生活中常见的金属,它们的单质及其化合物在科学研究和工农业生产中具有广泛用途。
请回答以下问题:
(1)超细铜粉可用作导电材料、催化剂等,其制备方法如下:
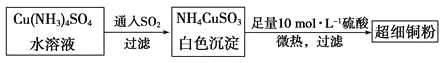
①Cu2+的价电子排布图________________; NH4CuSO3中N、O、S三种元素的第一电离能由大到小顺序为_______________________(填元素符号)。
②SO42-的空间构型为_____________,SO32-离子中心原子的杂化方式为__________。
(2)请写出向Cu(NH3)4SO4水溶液中通入SO2时发生反应的离子方程式:___________。
(3)某学生向CuSO4溶液中加入少量氨水生成蓝色沉淀,继续加入过量氨水沉淀溶解,得到深蓝色透明溶液,最后向该溶液中加入一定量乙醇,析出[Cu(NH3)4]SO4·H2O晶体。
①下列说法正确的是________
a.氨气极易溶于水,是因为NH3分子和H2O分子之间形成3种不同的氢键
b.NH3分子和H2O分子,分子空间构型不同,氨气分子的键角小于水分子的键角
c.Cu(NH3)4SO4所含有的化学键有离子键、极性共价键和配位键
d.Cu(NH3)4SO4组成元素中电负性最大的是氮元素
②请解释加入乙醇后析出晶体的原因_____________________.
-
铜单质及其化合物在很多领域有重要的用途.
(一)如金属铜用来制造电线电缆,超细铜粉可应用于导电材料、催化剂等领域中;CuCl和 都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等.
都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等.
(1)超细铜粉的某制备方法如下:

 中的配体是_______________________ 。
中的配体是_______________________ 。
(2)氯化亚铜 的制备过程是:向
的制备过程是:向 溶液中通入一定量SO2,微热,反应一段时间后即生成CuCl白色沉淀,反应的离子方程式为_______________________________________________________ 。
溶液中通入一定量SO2,微热,反应一段时间后即生成CuCl白色沉淀,反应的离子方程式为_______________________________________________________ 。
(二)波尔多液是一种保护性杀菌剂,广泛应用于树木、果树和花卉上,鲜蓝色的胆矾晶体是配制波尔多液的主要原料.
(1)与铜同周期的所有元素的基态原子中最外层电子数与铜原子相同的元素有 _______________________  填元素符号
填元素符号 。
。
(2)往浓 溶液中加入过量较浓的
溶液中加入过量较浓的 直到原先生成的沉淀恰好溶解为止,得到深蓝色溶液.小心加入约和溶液等体积的
直到原先生成的沉淀恰好溶解为止,得到深蓝色溶液.小心加入约和溶液等体积的 并使之分成两层,静置.经过一段时间后可观察到在两层“交界处”下部析出深蓝色晶体是____________________(写化学式),实验中所加
并使之分成两层,静置.经过一段时间后可观察到在两层“交界处”下部析出深蓝色晶体是____________________(写化学式),实验中所加 的作用是________________________。
的作用是________________________。
(3) 晶体中呈正四面体的原子团是______ ,杂化轨道类型是
晶体中呈正四面体的原子团是______ ,杂化轨道类型是 杂化的原子是____________。
杂化的原子是____________。
-
铜单质及其化合物在很多领域有重要的用途,如金属铜用来制造电线电缆,超细铜粉可应用于导电材料、催化剂等领域中,CuCl和CuCl2都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等。
⑴超细铜粉的某制备方法如下:
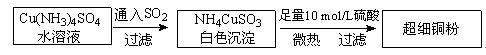
①[Cu(NH3)4]SO4中所含的化学键有________、________、________,
N、O、S三种元素的第一电离能大小顺序为:________>________>________。(填元素符号)
②NH4CuSO3中的金属阳离子的核外电子排布式为:________。
③ NH3分子中N原子的杂化方式为:________。
④与SO2互为等电子体的分子有________(写一种)。
⑵氯化亚铜(CuCl)的某制备过程是:向CuCl2溶液中通人一定量SO2,微热,反应一段时间后即生成CuCl白色沉淀。
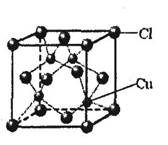
①CuCl的晶胞结构如下图所示,其中Cl原子的配位数为_________。
②CuCl的熔点比CuO的熔点________。(填“高”或“低”)
-
(14分)超细铜粉主要应用于导电材料、催化剂等领域中。超细铜粉的某制备方法如下:

试回答下列问题:
(1)下列关于[Cu(NH3)4]SO4的说法中,正确的有__________。(填字母序号)
A.[Cu(NH3)4]SO4中所含的化学键有离子键、极性键和配位键
B.[Cu(NH3)4]SO4含有NH3分子,其水溶液中也含有NH3分子
C.[Cu(NH3)4]SO4的组成元素中第一电离能最大的是氧元素
D.[Cu(NH3)4]SO4的外界离子的空间构型为正四面体
(2)NH4CuSO3中的金属阳离子的核外电子排布式为_______________。
(3)SO2–3 离子中S硫原子的杂化方式为________,与其互为等电子体的一种分子的分子式是___________。
(4)NH3易液化的原因是___________________。
(5)右图是铜的某种氧化物的晶胞结构示意图,由此可确定该氧化物的化学式_____。

(6)NH4CuSO3与硫酸微热反应的离子方程式为__________________________。
-
超细铜粉主要应用于导电材料、催化剂等领域中.超细铜粉的某制备方法如下:

试回答下列问题:
(1)下列关于[Cu(NH3)4]SO4的说法中,正确的有______.(填字母序号)
A.[Cu(NH3)4]SO4中所含的化学键有离子键、极性键和配位键
B.[Cu(NH3)4]SO4含有NH3分子,其水溶液中也含有NH3分子
C.[Cu(NH3)4]SO4的组成元素中第一电离能最大的是氧元素
D.[Cu(NH3)4]SO4的外界离子的空间构型为正四面体
(2)NH4CuSO3中的金属阳离子的核外电子排布式为:______.
(3)SO 离子中S硫原子的杂化方式为______,与其互为等电子体的一种分子的分子式是______.
离子中S硫原子的杂化方式为______,与其互为等电子体的一种分子的分子式是______.
(4)NH3易液化的原因是______.
(5)如图是铜的某种氧化物的晶胞结构示意图,由此可确定该氧化物的化学式为______.
(6)NH4CuSO3与硫酸微热时除得到超细铜粉外,还可看到溶液变蓝,同时有使品红褪色的气体.则该反应的离子方程式为______ 2NH4++Cu2++Cu+2SO2↑+2H2O






 所示,该化合物的化学式为________.
所示,该化合物的化学式为________. 







