-
醉酒驾车的判定标准:酒精含量大于(等于)每100毫升血液中80毫克/的行为属于醉酒驾车。 根据国家《车辆驾驶人员血液、呼气酒精含量阈值与检验》规定,100毫升血液中酒精含量达到20-80毫克的驾驶员即为酒后驾车,80毫克以上认定为醉酒驾车。交警对驾驶员进行呼气酒精检测的原理是:橙色的K2Cr2O7酸性水溶液乙醇迅速生成蓝绿色Cr3+。下列对乙醇的描述与此测定原理有关的物理性质是( )
A. 乙醇的沸点低 B. 乙醇的密度比水小
C. 乙醇有还原性 D. 乙醇是烃的含氧化合物
高二化学选择题中等难度题查看答案及解析
-
为减少交通事故,新交规明令禁止酒后驾车并对酒后驾车行为予以重罚。为检验驾驶员是否酒后驾车,可采用的检验方法有多种。回答以下问题:
(1)早期曾经采用五氧化二碘和某种高分子化合物X的混合溶液来检测酒精的存在。其原理是:I2O5与CH3CH2OH先发生反应(I2O5+5CH3CH2OH=I2+5Y+5H2O),生成的I2与高分子化合物X作用而变蓝。交警依据此原理来检测驾驶员是否饮酒。则:
X的化学名称是__________;
Y的分子式是____________;
(2)已知:I2O5是白色固体,可用于检验并定量测定空气中CO;两者在常温条件下发生的反应为5CO+I2O5=5CO2+I2(空气中其余气体不与I2O5反应);某同学设计如右实验装置完成上述目的。
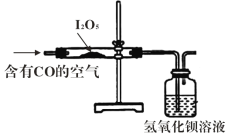
①指出能证明空气中有CO存在的现象。答:__________________________。
②将上述反应生成的碘单质用硫代硫酸钠滴定(反应为I2+2Na2S2O3=Na2S4O6+2NaI),即可根据消耗硫代硫酸钠的量来计算空气中CO的含量。若某次实验时测得参与反应的空气体积为a mL(标准状况下),滴定过程中,共消耗vmL c mol·L-1Na2S2O3溶液。则该空气样品中CO的体积分数是_____________。
③有同学提出只要依据参与反应的空气体积和洗气瓶中白色沉淀的质量也可求得空气中CO的体积分数。此方案是否可行?答:_________________________。
(3)燃料电池酒精检测仪(该电池以硫酸溶液为电解质溶液)也是检测酒精含量的一种方法。总反应是:CH3CH2OH+O2=CH3COOH+H2O。该电池正极电极反应式是______________。
高二化学综合题中等难度题查看答案及解析
-
一种新的酒后驾车人员体内酒精含量的检测装置如右图所示,下列说法不正确的是

A.该检测装置实现了将化学能转化了电能,且单位时间内通过电量越大,酒精含量越高
B.电极A 的反应: H2O + C2H5OH-4e- = CH3COOH + 4H+
C.电极B 是正极,且反应后该电极区pH 值减小
D.电池总反应:O2 + C2H5OH = CH3COOH + H2O
高二化学选择题简单题查看答案及解析
-
碘过量可以导致对健康的不良影响,包括甲状腺功能亢进症(IIH)和自身免疫甲状腺病(AITD)。国家规定,食盐中碘含量的标准为(18~33)mg·kg-1(即;每千克碘盐中含碘元素18~33毫克)。某课外活动小组为测定某碘盐(含KIO3)样品中的碘含量,设计了如下步骤:
Ⅰ.用天平准确称取10.0g碘盐样品,加适量蒸馏水充分溶解,得到100mL溶液;
II.取步骤I中溶液25.00mL用稀硫酸酸化,加入足量KI溶液与碘盐中的KIO3充分反应;
III.以淀粉为指示剂,用物质的量浓度为3.0×10-4mol/L的Na2S2O3标准溶液滴定步骤II所得溶液(滴定时的反应方程式:I2+2S2O32-==2I-+S4O62-),若平行实验三次,记录数据如下:
滴定次数
待测溶液的体积(mI.)
标准Na2S2O3溶液的体积
滴定前读数(mL)
滴定后读数(mL)
1
25.00
1.02
11.03
2
25.00
2.00
11.99
3
25.00
2.20
12.20
(1)步骤II涉及反应的离子方程式为___________________________;
(2)步骤III中滴定终点的现象是____________________________;
(3)根据题中所给数据,计算该碘盐样品中的碘元素含量是_______________mg·kg-1(保留三位有效数字);
(4)以下操作会导致测定结果偏高的是_______。
A.未用标准浓度的Na2S2O3溶液润洗滴定管
B.滴定前锥形瓶有少量水
C.滴定前滴定管尖嘴部分有气泡,滴定后气泡消失
D.观察读数时,滴定前仰视,滴定后俯视
高二化学实验题困难题查看答案及解析
-
去年8月至今年9月,浙江共查处酒后驾驶204596起,其中醉酒驾驶20593起,行政拘留20471人.案件起数,居全国前列.交警执法时,主要测量驾驶员体内的( )
A.醋酸
B.酒精
C.蛋白质
D.葡萄糖高二化学选择题中等难度题查看答案及解析
-
从2011年5月1日起,醉酒驾驶将作为危险驾驶罪被追究驾驶人刑事责任.醇脱氢酶和醛脱氢酶可以帮助酒精的代谢,酶是一种蛋白质,由此判断两种酶中可能不含( )
A.H元素
B.C元素
C.Si元素
D.N元素高二化学选择题中等难度题查看答案及解析
-
公安部发布法令:从2011年5月1日起,醉酒驾驶机动车将一律入刑。下列关于酒精的叙述错误的是
A.化学名称为乙醇 B.易挥发 C.常用作有机溶剂 D.不能燃烧
高二化学选择题简单题查看答案及解析
-
维生素C(化学式:C6H8O6,相对分子质量:176)属于外源性维生素,人体不能自身合成,必须从食物中摄取。每100克鲜榨橙汁中含有大约37.5毫克的维生素C。实验室可用碘量法测定橙汁中维生素C含量。反应的方程式为C6H8O6+I2=C6H6O6+2HI。某学习小组欲用该方法测定市售某橙汁饮料中维生素C的含量。
其实验步骤及相关数据如下。
①标准液的稀释:移取浓度为0.008000mol•L-1的碘标准溶液20.00mL于200mL容量瓶中,定容,摇匀备用。
②移取10.00mL饮料样品(设密度为1.0g•cm-3)于250mL锥形瓶中,加入50mL蒸馏水,2mL指示剂。
③在滴定管中装入稀释后的标准液进行滴定至终点,读取并记录相关数据。
④重复测定3次,数据记录如下表。
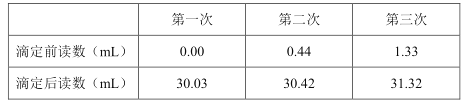
回答下面的问题:
(1)实验中盛装标准溶液应选择_________(填“酸式”或“碱式”)滴定管。滴定前为何要稀释标准溶液?______________________________________________________。
(2)步骤2中加入的指示剂是____________,判断滴定达到终点的现象是_______________。
(3)实验中下列操作可能导致测定结果偏低的是_________
A.稀释标准溶液定容时俯视刻度线
B.滴定结束读数时俯视读数
C.在锥形瓶中加入样品后放置较长时间才开始滴定
D.滴定管尖嘴部分有气泡,滴定后消失
(4)计算该饮料样品中维生素C含量为_________mg/100g。由滴定结果判断该饮料_________(填“是”或“不是”)天然汁。
高二化学实验题困难题查看答案及解析
-
酒后驾车是引发交通事故的重要原因.交警对驾驶员进行呼气酒精检测的原理是:橙色的K2Cr2O7酸性水溶液遇到乙醇迅速变成蓝绿色的Cr3+;下列对乙醇的4条描述中,与酒后驾车酒精测定原理有关的是( )
①乙醇沸点低 ②乙醇密度比水小 ③乙醇有还原性 ④乙醇有兴奋神经作用.
A.②③
B.①③
C.②④
D.①④高二化学选择题中等难度题查看答案及解析
-
酒后驾车是引发交通事故的重要原因。公安部交通管理局新修订的《机动车驾驶证申领和使用规定》于2010年4月1日起正式实行,对酒后驾车加倍处罚,一次性扣12分。交警对驾驶员进行呼气酒精检测的原理是:橙色的K2Cr2O7酸性水溶液与乙醇反应,迅速生成蓝绿色的Cr3+。下列对乙醇的描述与此测定原理有关的是( )
①乙醇沸点低 ②乙醇密度比水小 ③乙醇有还原性 ④乙醇是烃的含氧化合物
A.②④ B.②③ C.①③ D.①④
高二化学单选题中等难度题查看答案及解析