-
关于10mL 0.1mol·L−1的NH3·H2O溶液,下列说法正确的是( )
A. 25℃时,若溶液的pH=11,则Kb(NH3·H2O)=1×10−6
B. 向溶液中加入少量CH3COONa固体,溶液中c(NH3·H2O)/c(NH4+)的值变小
C. 向溶液中加入10mL0.1 mol·L−1盐酸,所得溶液中离子浓度大小顺序为:c(NH4+)>(Cl−)>c(H+)>c(OH−)
D. 向溶液中加入5 mL 0.1 mol·L−1盐酸,所得溶液中离子的浓度一定符合:c(NH4+)+c(H+)=c(Cl−)+c(OH−)
高二化学选择题中等难度题查看答案及解析
-
25℃时,关于体积为20 mL pH=11的氨水,下列说法正确的是( )
A.其pH比0.001mol·L-1的氢氧化钠溶液小 B.c(NH3·H2O)+c(NH4+)=0.001mol·L-1
C.向其中加入20mL pH=3的硫酸,混合溶液pH>7 D.加水稀释至200 mL,溶液的pH等于10
高二化学单选题简单题查看答案及解析
-
25℃时,关于体积为20 mL pH=11的氨水,下列说法正确的是( )
A. 其pH比0.001mol·L-1的氢氧化钠溶液小 B. c(NH3·H2O)+c(NH4+)=0.001mol·L-1
C. 向其中加入20mL pH=3的硫酸,混合溶液pH>7 D. 加水稀释至200 mL,溶液的pH等于10
高二化学单选题简单题查看答案及解析
-
25 ℃时,在10 mL浓度均为0.1 mol·L-1的NaOH和NH3·H2O混合溶液中滴加0.1 mol·L-1盐酸,下列有关溶液中粒子浓度关系正确的是( )
A.加入盐酸至溶液pH=7时:c(Cl-)=c(Na+)
B.加入20 mL盐酸时:c(Cl-)=c(NH4+)+c(Na+)
C.未加盐酸时:c(OH-)>c(Na+)=c(NH3·H2O)
D.加入10 mL盐酸时:c(NH4+)+c(H+)=c(OH-)
高二化学单选题中等难度题查看答案及解析
-
25℃条件下,向10 mL 0.1 mol·Lˉ1的HR溶液中逐滴滴入0.1 mol·Lˉ1的NH3·H2O溶液,所得溶液pH及导电性变化如图。下列分析不正确的是( )
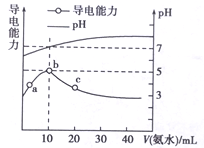
A. a~b点导电能力增强,说明HR为弱酸
B. b点溶液pH=7说明NH4R没有发生水解
C. c点溶液存在c(NH4+)>c(Rˉ)、c(OHˉ)>c(H+)
D. b~c任意点溶液均有c(H+)·c(OHˉ)=KW=1.0×10ˉ14
高二化学选择题困难题查看答案及解析
-
常温下 0.1mol/L 氨水pH为11,则下列说法中不正确的是( )
A. 此溶液中 NH3∙H2O 在常温下的电离度约为1%
B. 若向此溶液中通入少量氨气,NH3∙H2O电离平衡正向移动,水的电离平衡逆向移动
C. 若向其中加入 pH为11的NaOH溶液,NH3∙H2O电离平衡不移动,但n(NH4+)减小
D. 若向其中加入少量水,溶液中n(H+)增大
高二化学单选题困难题查看答案及解析
-
常温下,有下列四种溶液:
①
②
③
④
0.1mol/L
NH3·H2O溶液
pH=11
NaOH溶液
pH=1
H2SO4溶液
pH=3
CH3COOH溶液
下列说法正确的是( )
A.①与③等体积混合,溶液pH<7
B.②与④等体积混合,溶液pH>7
C.将VmL④的溶液浓缩到10—2VmL后,pH与③相同
D.②与③混合,若溶液pH=7,则V(NaOH) : V(H2SO4) =100 : 1
高二化学选择题中等难度题查看答案及解析
-
25 ℃时加水稀释10 mL pH=11的氨水,下列判断不正确的是( )
A. 原氨水的浓度大于10-3mol·L-1
B. 溶液中c(NH4+)/c(NH3·H2O)增大
C. 氨水的电离程度增大,溶液中所有离子的浓度均减小
D. 再加入10 mL pH=3的盐酸充分反应后混合液的pH值肯定大于7
高二化学单选题中等难度题查看答案及解析
-
25℃时,将浓度均为0.1mol·L-1、体积分别为Va和Vb的HX溶液与NH3·H2O溶液不同体积比混合,保持Va+Vb=100mL,Va、Vb与混合液的pH的关系如图所示。下列说法正确的是( )
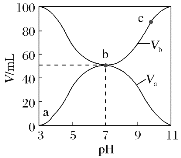
A.Ka(HX)的值与Kb(NH3·H2O)的值相等
B.b点,c(NH4+)+c(HX)=0.05mol·L-1
C.a→c点过程中,一定有c(NH4+)>c(X-)>c(H+)>c(OH-)
D.a、b、c三点,c点时水电离出的c(H+)最大
高二化学多选题中等难度题查看答案及解析
-
25℃条件下,向10 mL 0.1 mol·Lˉ1的HR溶液中逐滴滴入0.1 mol·Lˉ1的NH3·H2O溶液,所得溶液pH及导电性变化如图。下列分析错误的是( )
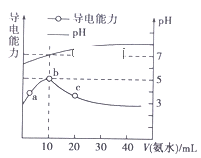
A. a~b点导电能力增强,说明HR为弱酸
B. b点溶液pH=7说明NH4R没有发生水解
C. c点溶液存在c(NH4+)>c(Rˉ)、c(OHˉ)>c(H+)
D. b~c任意点溶液均有c(H+)·c(OHˉ)=KW=1.0×10ˉ14
高二化学单选题困难题查看答案及解析