-
关于0.1mol/LNa2CO3溶液的叙述错误的是( )
A.0.5L该溶液中钠离子的物质的量浓度为0.05mol/L
B.1L该溶液中含有Na2CO3的质量为10.6g
C.从1L该溶液中取出100mL,则取出溶液中Na2CO3的物质的量浓度为0.01mol/L
D.取该溶液10mL,加水稀释至100mL后,Na2CO3的物质的量浓度为0.01mol/L高三化学选择题中等难度题查看答案及解析
-
常温下,下列有关离子浓度之间的关系不正确的是
A. 将CO2通入0.1mol/LNa2CO3溶液至中性,溶液中:2c(CO32-)+c(HCO3-)=0.lmol/L
B. 浓度均为0.1mol/L的CH3COOH与CH3COONa溶液等体积混合后,pH=5,则混合溶液中:c(CH3COO-)-c(CH3COOH)=2×(10-5-10-9)mol/L
C. 将0.2mol/LNaHCO3溶液与0.1mol/LKOH溶液等体积混合:3c(K+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-)
D. 已知Ka(CH3COOH)=Kb(NH3·H2O)=1.8×10-5,则常温下0.1mol/LCH3COONH4中:c(CH3COO-): c(NH3·H2O)=180
高三化学单选题困难题查看答案及解析
-
关于0.1 mol·L-1Na2CO3溶液的叙述中错误的是 ( )
A.0.5 L该溶液中钠离子的物质的量浓度为0.2 mol·L-1
B.1 L该溶液中含有Na2CO3的质量为10.6 g
C.从1 L该溶液中取出100 mL,则取出溶液中Na2CO3的物质的量浓度为0.01 mol·L-1
D.取该溶液10 mL,加水稀释至100 mL后,Na2CO3的物质的量浓度为0.01 mol·L-1
高三化学选择题中等难度题查看答案及解析
-
有关①100mL 0.1mol/LNaHCO3、②100mL 0.1mol/LNa2CO3两种溶液的叙述不正确的是( )
A.溶液中水电离出的H+个数:②>①
B.溶液中阴离子的物质的量浓度之和:②>①
C.①溶液中:
D.②溶液中:高三化学选择题中等难度题查看答案及解析
-
有关①100mL 0.1mol/LNaHCO3、②100mL 0.1mol/LNa2CO3两种溶液的叙述不正确的是( )
A.溶液中水电离出的H+个数:②>①
B.溶液中阴离子的物质的量浓度之和:②>①
C.①溶液中:
D.②溶液中:高三化学选择题中等难度题查看答案及解析
-
常温下,0.1 mol/L氨水溶液中
=1×10-8,下列叙述错误的是
A.该溶液中氢离子的浓度:c(H+ ) = 1×10-9 mol/L
B.0.1 mol/L 氨水溶液与0.1 mol/L HCl溶液等体积混合后所得溶液中:
c(NH4+ ) + c(H+ ) = c(Cl- ) + c(OH-)
C.0.1 mol/L 的氨水溶液与0.05 mol/L H2SO4溶液等体积混合后所得溶液中:
c(NH4+ ) + c(NH3) + c(NH3·H2O) = 2c(SO42-)
D.浓度均为0.1 mol/L 的NH3·H2O和NH4Cl溶液等体积混合后,若溶液呈碱性,则
c(NH4+ )> c (NH3·H2O) > c(Cl-) > c(OH-) > c(H+ )
高三化学选择题困难题查看答案及解析
-
常温下,向20mL某浓度的硫酸溶液中滴入0.1mol/L氨水,溶液中水电离的氢离子浓度随加入氨水的体积变化如图.下列分析不正确的是
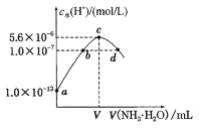
A. 硫酸的浓度为0.05mol/L
B. V=20
C. c点所示的溶液中:c(NH4+)>c(SO42-)>c(H+)>c(OH-)
D. d点所示溶液中:c(NH4+)=c(SO42-)
高三化学单选题中等难度题查看答案及解析
-
常温下,0.1 mol/L氨水溶液中
=1×10-8,下列叙述错误的是
A.该溶液中氢离子的浓度:c(H+ ) = 1×10-9 mol/L
B.0.1 mol/L氨水溶液与0.1 mol/L HCl溶液等体积混合后所得溶液中:
c(NH4+ ) + c(H+ ) = c(Cl- ) + c(OH-)
C.0.1 mol/L的氨水溶液与0.05 mol/L H2SO4溶液等体积混合后所得溶液中:
c(NH4+ ) + c(NH3) + c(NH3·H2O) = 2c(SO42-)
D.浓度均为0.1 mol/L的NH3·H2O和NH4Cl溶液等体积混合后,若溶液呈碱性,则
c(NH4+ )> c(NH3·H2O) > c(Cl-) > c(OH-) > c(H+ )
高三化学选择题极难题查看答案及解析
-
8.0.5LNaOH溶液中有2gNaOH,则此溶液的物质的量浓度为
A.0.05mol•L﹣1 B.0.1 mol•L﹣1
C.0.5 mol•L﹣1 D.1 mol•L﹣1
高三化学单选题简单题查看答案及解析
-
常温下,0.1 mol/L氨水溶液中
=1×10-8,下列叙述不正确的是( )
A.该溶液中氢离子的浓度:c(H+)=1×10-11 mol/L
B.0.1 mol/L氨水溶液与0.1 mol/L HCl溶液等体积混合后所得溶液中:c(N
)+c(H+)=c(Cl-)+c(OH-)
C.0.1 mol/L的氨水溶液与0.05 mol/L H2SO4溶液等体积混合后所得溶液中:c(N
)+c(NH3)+c(NH3·H2O)=2c(S
)
D.浓度均为0.1 mol/L的NH3·H2O和NH4Cl溶液等体积混合后,若溶液呈碱性,则c(N
)>c(NH3·H2O)>c(Cl-)>c(OH-)>c(H+)
高三化学选择题中等难度题查看答案及解析