-
下列有关说法正确的是
A.已知:HI(g)
 H2(g)+
H2(g)+ I2(s) △H =-26.5kJ/mol,由此可知1mol HI气体在密闭容器中充分分解后可以放出26.5kJ的热量
I2(s) △H =-26.5kJ/mol,由此可知1mol HI气体在密闭容器中充分分解后可以放出26.5kJ的热量
B.已知:2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ/mol,则氢气的燃烧热为ΔH=-285.8 kJ/mol
C.肼(N2H4)是一种用于火箭或燃料电池的原料,已知
2H2O(g) + O2(g)=2H2O2(l) △H= +108.3kJ/mol ①
N2H4(l) + O2(g)=N2(g) + 2H2O(g) △H=-534.0kJ/mol ②
则有反应:N2H4(l) + 2 H2O2(l) = N2(g) + 4H2O(l) △H=-642.3kJ/mol
D.含20.0 g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则稀醋酸和稀NaOH溶液反应的热化学方程式为:NaOH(aq)+CH3COOH(aq) = CH3COONa(aq)+H2O(l) ΔH=-57.4 kJ/mol
-
已知:①I2(g)+H2(g) 2HI(g)+26.5kJ、②I2(s)+H2(g)
2HI(g)+26.5kJ、②I2(s)+H2(g) 2HI(g)-9.5kJ,下列分析正确的是
2HI(g)-9.5kJ,下列分析正确的是
A.①是放热反应,无需加热即可发生
B.②需持续不断加热才能发生反应
C.I2(g)和I2(s)的能量关系如图所示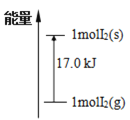
D.1molI2(s)和1molH2(g)的能量之和比2molHI(g)能量高
-
根据碘与氢气反应的热化学方程式
(i)I2(g)+ H2(g)  2HI(g)+ 9.48 kJ (ii) I2(s)+ H2(g)
2HI(g)+ 9.48 kJ (ii) I2(s)+ H2(g) 2HI(g) - 26.48 kJ
2HI(g) - 26.48 kJ
下列判断正确的是
A.1mol I2(s)中通入2gH2(g),反应吸热26.48 kJ
B.1 mol固态碘与1 mol气态碘所含的能量相差17.00 kJ
C. 反应(ii)的反应物总能量比反应(i)的反应物总能量低
D.反应(i)放出的热量多,所以产物的能量低,比反应(ii)的产物更稳定
-
关于反应2HI(g)  H2(g) + I2(g) - 11 kJ,正确的是
H2(g) + I2(g) - 11 kJ,正确的是
A.反应物的总键能低于生成物的总键能
B.1mol I2(g)中通入1mol H2(g),反应放热11kJ
C.等物质的量时,I2(g)具有的能量低于I2(l)
D.平衡时分离出HI(g),正反应速率先减小后增大
-
HI常用作有机反应中的还原剂,受热会发生分解反应。已知443℃时:2HI(g) H2(g)+I2(g) △H=+12.5kJ·mol-1向1L密闭容器中充入1mol HI,443℃时,体系中c(HI)与反应时间t的关系如图所示。下列说法中,正确的是( )
H2(g)+I2(g) △H=+12.5kJ·mol-1向1L密闭容器中充入1mol HI,443℃时,体系中c(HI)与反应时间t的关系如图所示。下列说法中,正确的是( )

A.0~20min内的平均反应速率可表示为v(H2)=0.0045mol·L-1·min-1
B.升高温度,再次平衡时,c(HI)>0.78mol·L-1
C.该反应的化学平衡常数计算式为
D.反应进行40 min时,体系吸收的热量约为0.94kJ
-
H2和I2在一定条件下能发生反应:H2(g)+I2(g) 2HI(g)△H=—a kJ/mol,下列说法正确的是( )
2HI(g)△H=—a kJ/mol,下列说法正确的是( )
已知: (a、b、c均大于零)
(a、b、c均大于零)
A. H2、I2和HI分子中的化学键都是非极性共价键
B. 断开2 mol HI分子中的化学键所需能量约为(c+b+a) kJ
C. 相同条件下,1 mol H2 (g)和1mol I2 (g)总能量小于2 mol HI (g)的总能量
D. 向密闭容器中加入2 mol H2(g)和2 mol I2(g),充分反应后放出的热量为2a kJ
-
H2和I2在一定条件下能发生反应:H2(g)+I2(g)  2HI(g) △H=-a kJ/mol.已知:
2HI(g) △H=-a kJ/mol.已知:
 (a、b、c均大于零)。
(a、b、c均大于零)。
下列说法正确的是
A.H2、I2和HI分子中的化学键都是非极性共价键
B.断开2 mol HI分子中的化学键所需能量约为(c+b+a) kJ
C.相同条件下,1 mol H2 (g)和1mol I2 (g)总能量小于2 mol HI (g)的总能量
D.向密闭容器中加入2 mol H2 (g)和2 mol I2 (g),充分反应后放出的热量为2a kJ
-
H2和I2在一定条件下能发生反应:H2(g)+I2(g)  2HI(g) △H=-a kJ/mol.已知:
2HI(g) △H=-a kJ/mol.已知:
 (a、b、c均大于零)。
(a、b、c均大于零)。
下列说法正确的是
A.H2、I2和HI分子中的化学键都是非极性共价键
B.断开2 mol HI分子中的化学键所需能量约为(c+b+a) kJ
C.相同条件下,1 mol H2 (g)和1mol I2 (g)总能量小于2 mol HI (g)的总能量
D.向密闭容器中加入2 mol H2 (g)和2 mol I2 (g),充分反应后放出的热量为2a kJ
-
H2和I2在一定条件下能发生反应:H2(g)+I2(g) 2HI(g) △H=-a kJ·mol-1已知:下列说法正确的是( )
2HI(g) △H=-a kJ·mol-1已知:下列说法正确的是( )
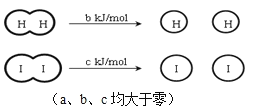
A.H2、I2和HI分子中的化学键都是非极性共价键
B.相同条件下,1 mol H2(g)和1 mol I2(g)的总能量小于2 mol HI(g)的总能量
C.断开2 mol HI分子中的化学键所需能量约为(c+b+a)kJ
D.向密闭容器中加入2 mol H2(g)和2 mol I2(g),充分反应后放出的热量为2a kJ
-
H2和I2在一定条件下能发生反应:H2(g)+I2(g) 2Hl(g) △H=-a kJ/mol。已知:
2Hl(g) △H=-a kJ/mol。已知:

下列说法正确的是
A.H2、I2和HI分子中的化学键都是非极性共价键
B.断开2 mol Hl分子中的化学键所需能量约为(c+b+a))kJ
C.相同条件下,lmol H2(g)和lmol I2(g)总能量小于2 molHl(g)的总能量
D.向密闭容器中加入2 mol H2(g)和2 mol I2(g),充分反应后放出的热量为2a kJ
H2(g)+
I2(s) △H =-26.5kJ/mol,由此可知1mol HI气体在密闭容器中充分分解后可以放出26.5kJ的热量


 (a、b、c均大于零)
(a、b、c均大于零) (a、b、c均大于零)。
(a、b、c均大于零)。 (a、b、c均大于零)。
(a、b、c均大于零)。
