-
在工业上,通过含锌矿石制取应用广泛的锌及其化合物。
(1)Zn在元素周期表中位于_____区,其基态原子价电子排布式为________。
(2)[Zn(CN)4]2-常用于电镀工业中,其中配位原子基态时核外电子的轨道表示式为_____,与CN-互为等电子体的粒子有_____、________(写出两种)。
(3)[Zn(CN)4]2-在水溶液中与甲醛(HCHO)溶液反应可制得HOCH2CN。甲醛分子的立体构型为________.中心原子杂化方式为________;HOCH2CN中元素电负性由大到小的顺序_______,1 mol HOCH2CN分子中,含有σ键的数为_________。
(4)ZnS和HgS晶体在岩浆中先晶出的是________,其原因是___________。
(5)ZnO的一种晶体结构与金刚石类似,4 个锌原子占据金刚石中晶胞内四个碳原子的位置,则该氧化物的密度为______g/cm3(设晶胞参数为apm,NA表示阿伏伽德罗常数)
高三化学填空题中等难度题查看答案及解析
-
在工业上,通过含锌矿石制取应用广泛的锌及其化合物。
(1)Zn在元素周期表中位于_____区,其基态原子价电子排布式为________。
(2)[Zn(CN)4]2-常用于电镀工业中,其中配位原子基态时核外电子的轨道表示式为_____,与CN-互为等电子体的粒子有_____、________(写出两种)。
(3)[Zn(CN)4]2-在水溶液中与甲醛(HCHO)溶液反应可制得HOCH2CN。甲醛分子的立体构型为________.中心原子杂化方式为________;HOCH2CN中元素电负性由大到小的顺序_______,1 mol HOCH2CN分子中,含有σ键的数为_________。
(4)ZnS和HgS晶体在岩浆中先晶出的是________,其原因是___________。
(5)ZnO的一种晶体结构与金刚石类似,4 个锌原子占据金刚石中晶胞内四个碳原子的位置,则该氧化物的密度为______g/cm3(设晶胞参数为apm,NA表示阿伏伽德罗常数)
高三化学填空题中等难度题查看答案及解析
-
硅是重要的半导体材料,是构成现代电子工业的基础。硅及其化合物在工业中应用广泛,在工业上,高纯硅可以通过下列流程制取:

完成下列填空:
(1)氯原子核外有_______种不同能量的电子,硅原子的核外电子排布式是_______________。
(2)碳与硅属于同主族元素,熔沸点SiO2 ________CO2 (填写“>”、“<”或“=”),其原因是_____________________________________________________。
(3)流程中由SiO2制粗硅的反应不能说明碳的非金属性强于硅,原因是_________________;请写出一个能说明碳的非金属性强于硅的化学方程式______________________________。
(4)SiHCl3(g) + H2(g)
Si(s) + 3HCl(g) -Q (Q>0)
①上述反应的平衡常数表达式K=_____________;能使K增大的措施是_______________。
②一定条件下,在固定容积的密闭容器中,能表示上述反应达到平衡状态的是________(选填编号)。
a.3v逆(SiHCl3)=v正(HCl) b.混合气体的压强不变
c.K保持不变 d.c(SiHCl3)∶c(H2)∶c(HCl)=1∶1∶3
③一定温度下,在2L密闭容器中进行上述反应,5min后达到平衡,此过程中固体质量增加0.28g,此时HCl的化学反应速率为 ________________ 。
高三化学综合题中等难度题查看答案及解析
-
【化学一选修3:物质结构与性质】
磷及其化合物在工农业生产上应用非常广泛。
(1)磷元素位于周期表的_______区,基态磷原子价层电子排布图________,最高能层符号________。
(2)磷的三种同素异形体的结构如下图所示。

① 三种同素异形体中能导电的是_______(填名称)。
②白磷易溶于CS2,其原因是___________。
(3)磷酸与Fe3+可形成H3[Fe(PO4)2],Fe、P、O电负性由大到小的顺序是________。与PO43-空间构型相同的分子和阴离子分别是________(各举1例)。
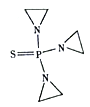
(4)噻替哌的结构简式如右图所示,其中氮原子的杂化轨道类型为_______,1mol噻替哌中含有的σ键数目为______。
(5)磷化铟( InP)是一种半导体材料,可用于光纤通信技术,其晶胞结构如图所示。
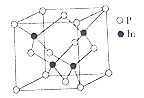
①结构化学上常用原子坐标参数表示晶胞内部各原子的相对位置,晶胞中P原子的坐标参数分别有:P (0,0,0),P(
,0,
);P(0,
,
)等,则距离上述三个P原子最近且等离的In原子的坐标参数为_____。
②已知晶胞参数a=0.587 m,则InP晶体的密度为______g/cm3。
高三化学综合题中等难度题查看答案及解析
-
铁氧体是一种磁性材料,具有广泛的应用。
(1)铁元素位于元素周期表的_________区,其基态原子有___________种能量不同的电子。
(2)工业制备铁氧体常使用水解法,制备时常加入尿素[CO(NH)2]2、醋酸钠等碱性物质,尿素分子中四种不同元素的电负性由大到小的顺序是________,醋酸钠中碳原子的杂化类型是_______。
(3)纳米氧化铁能催化火箭推进剂NH4ClO4的分解,
的结构式为___________(标出配位键),与
互为等电子体的分子有____________(任写一种)。铵盐大多不稳定,NH4F、NH4I中,较易分解的是_______________。
(4)晶体Fe3O4的晶胞如图所示,该晶体是一种磁性材料,能导电。
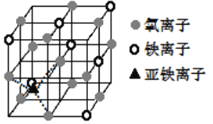
①晶胞中亚铁离子处于氧离子围成的_______________(填空间结构)空隙。
②晶胞中氧离子的堆积方式与某金属晶体原子堆积方式相同,该堆积方式名称为______。
③解释Fe3O4晶体能导电的原因_________;若晶胞的体对角线长为a nm,则Fe3O4晶体的密度为_____________g·cm-3(阿伏加德罗常数用NA表示)。
高三化学综合题中等难度题查看答案及解析
-
短周期主族元素
、
、
、
的原子序数依次增大,
是地壳中含量最多的元素,
原子的最外层有2个电子,
的单质晶体是应用最广泛的半导体材料,
与
位于同一主族。下列说法正确的是( )
A.原子半径:
B.由
、
组成的化合物可表示为
C.
的最高价氧化物对应水化物的酸性比
的强
D.
的简单气态氢化物的热稳定性比
的强
高三化学单选题中等难度题查看答案及解析
-
铝是地壳中含量最多的金属元素,铝及其化合物在日常生活、工业上有广泛的应用。
(1)铝原子核外有_________种不同运动状态的电子,有_________种能量不同的电子,写出铝在元素周期表中的位置:________
(2)氮化铝具有强度高,耐磨,抗腐蚀,熔点可达2200℃。推测氮化铝是________晶体,试比较组成该物质的两微粒半径大小:_______
(3)可用铝和氧化钡反应可制备金属钡:4BaO+2Al
BaO·Al2O3+3Ba↑的主要原因是_______(选填编号)。
a.Al活泼性大于Ba b.Ba沸点比Al的低 c.BaO·Al2O3比Al2O3稳定
(4)工业上用氢氧化铝、氢氟酸和碳酸钠制取冰晶石(Na3AlF6)。其反应物中有两种元素在周期表中位置相邻,可比较它们金属性或非金属性强弱的是_________(选填编号)。
a.气态氢化物的稳定性 b.最高价氧化物对应水化物的酸(碱)性
c.单质与氢气反应的难易 d.单质与同浓度酸发生反应的快慢
(5)描述工业上不用电解氯化铝而是用电解氧化铝的方法获得铝单质的原因:_______
高三化学综合题中等难度题查看答案及解析
-
铜及其化合物在生产生活中有着广泛的应用。请回答下列问题:
(1)铜元素位于元素周期表中_____区,基态Cu原子有______种不同能级的电子。
(2)铜合金可用于制造航母螺旋桨。制造过程中产生的含铜废液可利用铜萃取剂M,通过如下反应实现铜离子的富集回收。
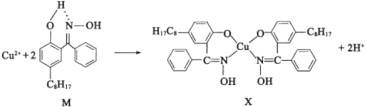
①M所含元素的电负性由大到小的顺序为______(用元素符号表示)。
②X中采用sp3杂化的非金属原子有______(填元素名称)。
(3)在较低温度下CuFeS2与浓硫酸作用时,有少量臭鸡蛋气味的气体Y产生。Y分子的立体构型是_______,Y的沸点比水低的主要原因是_______。
(4)向蓝色{[Cu(H2O)4]2+}硫酸铜溶液中加入稍过量的氨水,溶液变为深蓝色{[Cu(NH3)4]2+}。通过上述实验现象可知,与Cu2+的配位能力:H2O________NH3(填“大于”或“小于”)。
(5)CuCl2和CuCl是铜的两种氯化物。
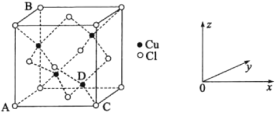
①图中表示的是_______(填“CuCl2”或“CuCl”)的晶胞。
②原子坐标参数可用来表示晶胞内各原子的相对位置,图中各原子坐标参数A为(0,0,0);B为(0,1,1);C为(1,0,0);则D原子的坐标参数为______。
③晶胞中C、D两原子核间距为298 pm,阿伏加德罗常数的值为NA,则该晶体密度为__g·cm-3(列出计算式即可)。
高三化学综合题中等难度题查看答案及解析
-
金属镓有“电子工业脊梁”的美誉,镓及其化合物应用广泛。
(1)基态Ga原子中有_____种能量不同的电子,其价电子排布式为_________。
(2)第四周期的主族元素中,基态原子未成对电子数与镓相同的元素有_______(填元素符号)。
(3)三甲基镓[(CH3)3Ga]是制备有机镓化合物的中间体。
①在700℃时,(CH3)3Ga和AsH3反应得到GaAs,化学方程式为____________________。
②(CH3)3Ga中Ga原子的杂化方式为__________;AsH3的空间构型是________________。
(4)GaF3的熔点为1000℃,GaC13的熔点为77.9℃,其原因是_______________________。
(5)砷化镓是半导体材料,其晶胞结构如图所示。
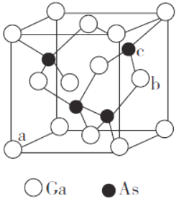
①晶胞中与Ga原子等距离且最近的As原子形成的空间构型为_______。
②原子坐标参数是晶胞的基本要素之一,表示晶胞内部各原子的相对位置。图中a(0,0,0)、b(1,
),则c原子的坐标参数为______________。
③砷化镓的摩尔质量为M g·mol-1,Ga的原子半径为p nm,则晶体的密度为____g·cm-3。
高三化学综合题困难题查看答案及解析
-
金属镓有“电子工业脊梁”的美誉,镓及其化合物应用广泛。
(1)一种镍催化法生产GaN的工艺如图:
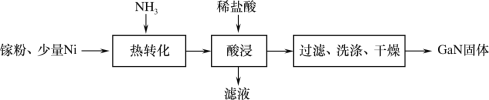
①镓(Ga)的原子结构示意图为
,镓元素在周期表中的位置是___。
②“热转化”时Ga转化为GaN的化学方程式是___。
③“酸浸”操作目的是___。
(2)某学校化学兴趣小组在实验室利用如图装置模拟制备氮化镓:
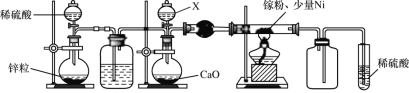
①仪器X中的试剂是__,加热前需先通入一段时间的H2,原因是__。
②取某GaN样品m克溶于足量热NaOH溶液,发生反应GaN+OH﹣+H2O
GaO2-+NH3↑,用H3BO3溶液将产生
NH3完全吸收,滴定吸收液时消耗浓度为cmol/L的盐酸VmL,则样品的纯度是___。
已知:NH3+H3BO3=NH3•H3BO3;NH3•H3BO3+HCl=NH4Cl+H3BO3
高三化学综合题困难题查看答案及解析