-
铜及其化合物在生产生活中有着广泛的应用。请回答下列问题:
(1)铜元素位于元素周期表中_____区,基态Cu原子有______种不同能级的电子。
(2)铜合金可用于制造航母螺旋桨。制造过程中产生的含铜废液可利用铜萃取剂M,通过如下反应实现铜离子的富集回收。
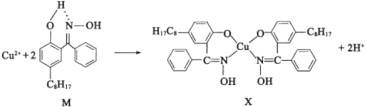
①M所含元素的电负性由大到小的顺序为______(用元素符号表示)。
②X中采用sp3杂化的非金属原子有______(填元素名称)。
(3)在较低温度下CuFeS2与浓硫酸作用时,有少量臭鸡蛋气味的气体Y产生。Y分子的立体构型是_______,Y的沸点比水低的主要原因是_______。
(4)向蓝色{[Cu(H2O)4]2+}硫酸铜溶液中加入稍过量的氨水,溶液变为深蓝色{[Cu(NH3)4]2+}。通过上述实验现象可知,与Cu2+的配位能力:H2O________NH3(填“大于”或“小于”)。
(5)CuCl2和CuCl是铜的两种氯化物。
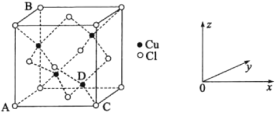
①图中表示的是_______(填“CuCl2”或“CuCl”)的晶胞。
②原子坐标参数可用来表示晶胞内各原子的相对位置,图中各原子坐标参数A为(0,0,0);B为(0,1,1);C为(1,0,0);则D原子的坐标参数为______。
③晶胞中C、D两原子核间距为298 pm,阿伏加德罗常数的值为NA,则该晶体密度为__g·cm-3(列出计算式即可)。
-
元素周期表第四周期的8、9、10列元素为X、Y、Z,它们的化合物在生产生活中有着广泛的应用。回答下列问题(涉及的化学式用元素符号表示)
(1)基态X原子的价电子排布式为______________________,Z2+核外3d能级上有___________对成对电子。
(2)Y3+的一种配离子[Y(N3) (NH3)5]2+中,Y3+的配位数是___________,lmol配离子中所含σ键的数目为___________,配位体N3-中心原子杂化类型为______________________。
(3)Y2+在水溶液中以[Y(H2O)6]2+存在。向含Y2+的溶液中加入过量氨水可生成更稳定的[Y(NH3)6]2+,其原因是____________________________________________。
(4)X离子与KCN形成的蓝色晶体中,X2+、X3+分别占据立方体互不相邻的顶点,而立方体的每条棱上均有一个CN-,K+位于立方体的某恰当位置上。据此可知该晶体的化学式为______________________,立方体中X2+间连接起来形成的空间构型是____________________。
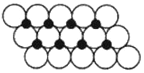
(5)一定温度下,ZO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列,Z2+填充其中(如图),已知O2-的半径为apm,每平方米面积上分散的该晶体的质量为___________g(用含a、NA的代数式表示)。
-
锌、铁、铜及其化合物在生活、生产中有着广泛应用。回答下列问题:
(1)基态Fe3+的核外电子排布式为____________。在第四周期过渡元素中,基态原子未成对电子数最多的元素为____________(用元素符号表示)。
(2)一水合甘氨酸锌[(H2NCH2COO)2Zn·H2O]是一种饲料添加剂,该化合物中所涉及的非金属元素电负性由大到小的顺序是____________(用元素符号表示);甘氨酸分子中N原子的杂化轨道类型为____________;从结构角度解释甘氨酸易溶于水的原因:________________。
(3)铜元素的第一电离能、第二电离能分别为746 kJ·mol-1、1958 kJ·mol-1;锌元素的第一电离能、第二电离能分别为906 kJ·mol-1、1733 kJ·mol-1,铜的第二电离能大于锌的第二电离能,其主要原因是___________________________________________________。
(4)磷酸铁(FePO4)可用于制造磷酸铁锂电池材料,PO 的空间构型为______________。
的空间构型为______________。
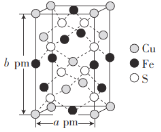
(5)某种化合物由Fe、Cu、S三种元素组成,其晶胞结构如图所示,则化学式为__________,该晶胞上、下底面均为正方形,侧面与底面垂直,若该晶体的密度ρ g·cm-3,设NA为阿伏加德罗常数的值,结合图中的数据计算底面棱长a=____________(只要求列出计算式,用含b的代数式表示)pm。
-
Co、Ni的化合物在生产生活中有着广泛的应用。
(1)Co元素在周期表中的位置是4周期________族。基态Co原子的简化电子排布式为_________。
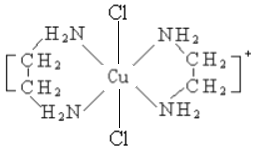
(2)乙二胺NH2-CH2-CH2-NH2(缩写符号en)中N原子的杂化方式为________杂化。en可以与Co形成配合物[Co(en)2Cl2]Cl·HCl·2H2O,配离子结构如下左图所示,中心离子的配位数为_______,配合物晶体中可能存在的作用力有___________。
A 离子键 B 极性共价键 C 非极性共价键 D 配位键 E 氢键
(3)天然氧化镍晶体中总是存在晶体缺陷,如图所示。NixO晶体中x值为 ,若晶体中的Ni分别为Ni2+、Ni3+,此晶体中Ni2+与Ni3+的最简整数比为______。
,若晶体中的Ni分别为Ni2+、Ni3+,此晶体中Ni2+与Ni3+的最简整数比为______。

(4)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列, Ni2+填充其中(如图),己知O2-的半径为a pm,每平方米面积上分散的该晶体的质量为_____g(用a、NA表示)。

-
铁及其化合物在生产生活中有着广泛的应用。回答下列问题:
(1)基态Fe原子的外围电子排布图为____,基态Fe2+中,核外电子占据最高能层的符号是____,Fe2+和Fe3+是铁的两种常见离子,Fe3+的稳定性强于Fe2+,原因是____。
(2)Fe3+可以与SCN—形成一系列不同配位数的红色配合物,所以常用KSCN溶液检验Fe3+的存在,KSCN中四种元素的电负性由小到大的顺序为_______,SCN—的几何构型为______,中心原子的杂化类型为_______。
(3)实验中常用K3[Fe(CN)6]检验Fe2+, K3[Fe(CN)6]晶体中的化学键有_________(填写选项字母)
a.离子键. b.共价键 c,氢键 d .配位键 e.金属键
1mol K3[Fe(CN)6]中含有σ键与π键的数目比为_____________。
(4)FexO为氯化钠型结构,在实际晶体中,由于存在缺陷,x<1。 测得Fe0.92O晶体的晶胞参数a=428.0pm,则该晶体的密度ρ=__________g/cm3 (列出计算式),晶体中最近的两个铁离子间的距离为_______pm。
-
卤族元素在生活中有广泛应用,根据所需知识回答下列问题。
(1)氟元素基态原子的价电子排布图:_________,卤族元素位于元素周期表______区。
(2)在一定浓度的氢氟酸溶液中,部分溶质以二分子缔合(HF)2形式存在,使HF分子缔合的作用力是_______________。
(3)BF3常温下是气体,有强烈的接受弧电子对的倾向。BF3分子的立体构型为______,固态时的晶体类型是_______,BF3与NH3相遇立即生成白色固体,写出该白色固体物质的结构式并标注出其中的配位键_____。
(4)根据下表提供的数据判断,熔点最高、硬度最大的是_______(填化学式)。
| 离子晶体 | NaF | MgF2 | AlF3 |
| 晶格能(KJ·mol-1) | 923 | 2957 | 5492 |
(5)已知NaClO2晶体中阴离子为V型,ClO2-中氯原子的弧电子对数是______,ClO2-中氯原子的杂化轨道类型为_____,HClO4比HClO2酸性强的原因是_______。
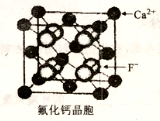
(6)CaF2晶胞如下图所示。已知:NA为阿伏伽德罗常数,棱上相邻的两个Ca2+的核间距为acm,则CaF2的密度可表示为_____g·cm-3。
-
氮及其化合物在生活、生产和科技等方面有重要的应用。砷位于周期表中的第四周期,与氮元素属同一主族元素,其广泛分布与自然界。试回答下列问题:
(1)砷的气态氢化物的电子式为 。
(2)氨和联氨(N2H4)是氮的两种常见化合物,制备联氨可用丙酮做催化剂,将次氯酸钠与氨气反应,该反应中还原剂与氧化剂的物质的量之比为2:1,写出该反应的化学方程式: 。
(3)砷的常见酸性氧化物有As2O3和As2O5,请根据图相关信息写出分解为的热化学方程式: 。

(4)直接供氨式碱性燃料电池的电池反应式为4NH2+3O2=2N2+6H2O,电解 质溶液一般使用氢氧化钾溶液,则负极电极反应式为 。
(5)氨气和二氧化碳在120℃,催化剂作用下反应生成尿素:CO2(g)+2NH3(g)  (NH2)2CO(s)+H2O(g),在密闭反应容器中,混合气体中氨气的含量变化关系如图所示,则氨气的平衡转化率是 。
(NH2)2CO(s)+H2O(g),在密闭反应容器中,混合气体中氨气的含量变化关系如图所示,则氨气的平衡转化率是 。
(6)将一定量的NH2COONH4(s)置于恒温密闭容器中,NH2COONH4(s)  2NH3(g)+CO2(g),其分解达到平衡状态时,该反应的化学平衡常数的表达式为 。
2NH3(g)+CO2(g),其分解达到平衡状态时,该反应的化学平衡常数的表达式为 。
(7)在容积恒定的密闭容器中进行反应2NO(g)+O2(g)  2NO2(g) △H>0,该反应的反应速率(v)随时间(t)变化的关系如图所示,若t2、t4时刻只改变一个条件,下列说法正确的是 (填序号)
2NO2(g) △H>0,该反应的反应速率(v)随时间(t)变化的关系如图所示,若t2、t4时刻只改变一个条件,下列说法正确的是 (填序号)
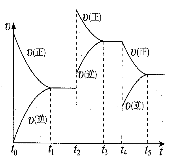
a.在t1-t2时,可依据容器内气体的压强保持不变判断反应已达到平衡状态
b.在t2时,采取的措施可以是升高温度
c.在t3-t4时,可依据容器内气体的密度保持不变判断反应已达到平衡状态
d.在t5时,容器内NO2的体积分数是整个过程中的最大值
-
钛(Ti)和锆(Zr)是同一副族的相邻元素,它们的化合物在生产生活中有着广泛的用途。回答下列有关问题:
(1)钛和锆的价层电子结构相同,请画出基态锆原子的价电子排布图_______。
(2)四氯化锆的沸点为331℃,溶于水;而二氧化锆的沸点为4300℃,难溶于水。分析推测四氯化锆属于_____晶体。
(3)人们经常利用过氧化氢作钛元素的定性检验试剂:向TiOSO4溶液中加入H2O2可以生成橙黄色的较稳定的[TiO(H2O2)]2+。
①在该配合离子中,作为配体的H2O2分子中氧原子的杂化轨道类型为_______。
②S2Cl2的分子结构与H2O2相似,它们均为________(天“极性”或“非极性”)分子
③H2O2的熔点和沸点均高于S2Cl2的主要原因是__________________。
④上述物质中H、O、S、Cl四种元素电负性由大到小的顺序为____________。
(4)巳知TiO2晶胞中Ti4+位于O2-所构成的正八面体的体心,ZrO2晶胞中Zr4+位于O2-所构成的立方体的体心,请根据给出的TiO2晶体和ZrO2晶体的晶胞结构图回答下列问题:
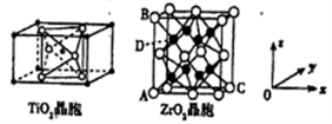
①根据晶胞图分析TiO2晶体中O2-的配位数是_____________。
②TiO2晶体和ZrO2晶体是两种不同类型的晶体结构,决定它们晶体结构不同的重要因素是_______________________________。
③原子坐标参数能够表示晶胞内部各原子的相对位置,二氧化锆晶胞中各原子的坐标参数分别为:A(0,0,0),B(0,0,1),C(1,1,0),则D原子的坐标参数为________。
④已知二氧化锆晶胞的密度为ρg/cm3,设阿伏加德罗常数的数值为NA,则晶体中B、D两原子核间的距离为_______pm。
-
【化学一选修3:物质结构与性质】铜及其化合物在化工生产中有着广泛的应用。回答下列问题:
(1)铜元素在元素周期表中的位置为_________________,基态Cu原子核外电子占据的原子轨道数为____________________。
(2)向硫酸铜溶液中加入乙二胺(H2N-CH2-CH2-NH3)溶液后,每个Cu2+可与两个乙二胺分子形成四配位离子,导致溶液由蓝色变为紫色。
①乙二胺分子中C、N原子的杂化轨道类型分别为_______________、_________________。
②与硫酸根离子互为等电子体的分子为___________(任写一种)。
③四配位离子的结构式为_____________________,该离子中所有元素的电负性由大到小的顺序为____________________________。
(3)硫化亚铜和氧化亚铜均为离子晶体,其中熔点较高的为___________(填化学式),原因为________________________________________________。
(4)下图为铜与氧(O)、钇(Y)、钡(Ba)形成的一种超导体材料的长方体晶胞结构,其晶胞参数如图(i)所示,该结构中有平面正方形(CuO4)和四方锥(CuO6)结构单元如图(ii)所示。
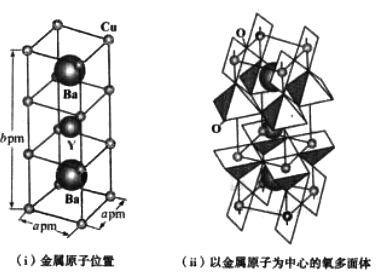
①该超导体材料的化学式为____________________________。
②已知该化合物的摩尔质量为Mg·mol-1,阿伏加德罗常数的值为NA,其密度为____g·cm-3(列出表达式即可)。
-
镁、铁、铜等在工农业生产中有着广泛的应用。回答下列问题:
(1)铜元素位于元素周期表中的___区,其基态原子的价电子排布图为_________。
(2)往硫酸铜溶液中加入过量氨水,可形成[Cu(NH3)4]SO4溶液,该溶液可用于溶解纤维素。
①[Cu(NH3)4]SO4中阴离子的立体构型是_______。
②在[Cu(NH3)4]SO4中,配离子所含有的化学键为________,提供孤电子对的成键原子是_______。
③ 除硫元素外,[Cu(NH3)4]SO4中所含元素的电负性由小到大的顺序为_______。
④NF3与NH3的空间构型相同,中心原子的轨道杂化类型均为_____。但NF3不易与Cu2+形成化学键,其原因是____________。
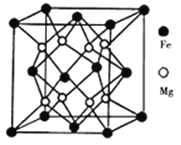
(3)铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。则铁镁合金的化学式为________,若该晶胞的参数为dnm,则该合金的密度为____ g/cm3(不必化简,用NA表示阿伏加德罗常数)。