-
(16分)已知A、B、C、D、E、F、G和H都是元素周期表中前36号的元素,它们的原子序数依次增大。A是周期表中原子半径最小的元素,B原子最外层电子数是内层电子数的两倍,C的基态原子核外有7种不同运动状态的电子,E是电负性最大的元素,F的氢化物和最高价氧化物对应的水化物均为强酸,G、H分别是周期表中1—18纵列中的第10、12纵列元素。请回答下列问题:
(1)D元素在周期表位置是 ,G的核外价层电子排布式为 。
(2)E与A形成的化合物比F与A形成的化合物的沸点 (填“高”或“低”),其原因是 。
(3)B、C原子的第一电离能较大的是 (填元素符号),其原因是 。
(4)BD32-离子中B原子采取 杂化,任写一种与BD互为等电子体的分子的电子式 。
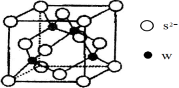
(5)元素H的一种硫化物晶体的晶胞结构如图所示,该硫化物的化学式是 。元素H的氢氧化物可溶于氨水中,生成和铜氨配离子相同配位数的离子,写出该反应的离子方程式为 。
高三化学简答题中等难度题查看答案及解析
-
已知A、B、C、D、E、F为周期表前四周期原子序数依次增大的六种元素。其中A是元素周期表中原子半径最小的元素,B原子最外层电子数是内层电子数的2倍。D、E为同主族元素,且E的原子序数为D的2倍。F元素在地壳中含量位于金属元素的第二位。试回答下列问题:
(1)F元素价层电子排布式为___________________。
(2)关于B2A2的下列说法中正确的是 ________________。
A.B2A2中的所有原子都满足8电子结构
B.每个B2A2分子中σ键和π键数目比为1∶1
C.B2A2是由极性键和非极性键形成的非极性分子
D.B2A2分子中的B-A键属于s—spσ键
(3) B和D形成的一种三原子分子与C和D形成的一种化合物互为等电子体,则满足上述条件的B和D形成的化合物的空间构型是________________。
(4) C元素原子的第一电离能比B、D两元素原子的第一电离能高的主要原因__________。
(5) A与D可以形成原子个数比分别为2∶1,1∶1的两种化合物X和Y,其中 Y含有____________键(填“极性键”“非极性键”),A与C组成的两种化合物M和N所含的电子数分别与X、Y相 等,N的 结构式为________。
(6) E的氢化物的价层电子对互斥理论模型为________,E 原子的杂化方式为________杂化。
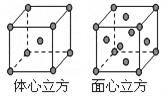
(7) F单质的晶体在不同温度下有两种堆积方式,晶胞分别如右图所示。面心立方晶胞和体心立方晶胞的棱边长分别为acm、bcm,则F单质的面心立方晶胞和体心立方晶胞的密度之比为_________,F原子配位数之比为__________________。
高三化学综合题简单题查看答案及解析
-
已知A、B、C、D、E、F为周期表前四周期原子序数依次增大的六种元素。其中A是元素周期表中原子半径最小的元素,B原子最外层电子数是内层电子数的2倍。D、E为同主族元素,且E的原子序数是D的2倍。F元素在地壳中含量位于金属元素的第二位。回答下列问题:
(1)F元素价层电子排布式为 。
(2)关于B2A2的下列说法中正确的是
A.B2A2 中的所有原子都满足8电子结构
B.每个B2A2分子中
键和
键数目比为1:1
C.B2A2 是由极性键和非极性键形成的非极性分子
D.B2A2分子中的A—B键属于
—
键
(3)B和D形成的一种三原子分子与C和D形成的一种化合物互为等电子体,则满足上述条件的B和D形成的化合物的结构式为
(4)C元素原子的第一电离能比B、D两元素原子的第一电离能都高的主要原因是
(5)D的氢化物比E的氢化物沸点高,其主要原因是 ;E的氢化物的价层电子对互斥模型为 ,E原子的杂化方式为 。
(6)F单质的晶体在不同温度下有两种堆积方式,即面心立方堆积和体心立方堆积,其晶胞的棱边长分别为a cm、b cm,则F单质的这两种晶体密度之比为 ,F原子的配位数之比为 。
高三化学填空题困难题查看答案及解析
-
已知A、B、C、D、E、F为周期表前四周期原子序数依次增大的六种元素。其中A是元素周期表中原子半径最小的元素,B原子最外层电子数是内层电子数的2倍。D、E为同主族元素,且E的原子序数为D的2倍。F元素在地壳中含量位于金属元素的第二位。试回答下列问题:
(1)F元素价层电子排布式为 _______________。
(2)关于B2A2的下列说法中正确的是 _________________。
A. B2A2中的所有原子都满足8电子结构
B. 每个B2A2分子中σ键和π键数目比为1:1
C. B2A2是由极性键和非极性键形成的非极性分子
D. B2A2分子中的B-A键属于s —spσ键
(3)B和D形成的一种三原子分子与C和D形成的一种化合物互为等电子体,则满足上述条件的B和D形成的化合物的空间构型是 ___________________。
(4)C元素原子的第一电离能比B、D两元素原子的第一电离能高的主要原因 _____________________________。
(5)A与D可以形成原子个数比分别为2:1,1:1的两种化合物X和Y,其中 Y含有__________键(填“极性键”“非极性键”),A与C组成的两种化合物M和N所含的电子数分别与X、Y相等, N的结构式为__________。
(6)E的氢化物的价层电子对互斥理论模型为 _______,E 原子的杂化方式为 ________杂化。
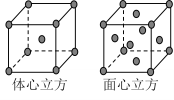
(7)F单质的晶体在不同温度下有两种堆积方式,晶胞分别如右图所示。面心立方晶胞和体心立方晶胞的棱边长分别为acm、bcm,则F单质的面心立方晶胞和体心立方晶胞的密度之比为____________,F原子配位数之比为__________________。
高三化学简答题简单题查看答案及解析
-
已知A、B、C、D、E是短周期中的5种元素,它们的原子序数依次增大.A在周期表中原子半径最小,B原子的最外层电子数是内层电子数的2倍,D元素与A元素同主族.E元素与C元素同主族;E的单质为黄色晶体,易溶于二硫化碳.
①画出A的阴离子的结构示意图______.
②C的单质和D的单质在点燃条件下反应生成化合物X,该反应的化学方程式为______ Na2O2高三化学解答题中等难度题查看答案及解析
-
已知A、B、C、D、E是短周期中的5种元素,它们的原子序数依次增大。A在周期表中原子半径最小,B原子的最外层电子数是内层电子数的2倍,D元素与A元素同主族。E元素与C元素同主族;E的单质为黄色晶体,易溶于二硫化碳。
①画出A的阴离子的结构示意图________。
②C的单质和D的单质在点燃条件下反应生成化合物X,该反应的化学方程式为________
。将产物加入滴有酚酞的水中,观察到的现象为
________。
③将9gB单质在足量的C单质中燃烧,所得气体通入1L1.0mol·L-1NaOH溶液中,完全吸收后,溶液中存在的离子按浓度由大到小的排列顺序是________
________。
④将E的单质在足量的C的单质中燃烧,所得主要气体为Y。将Y通入X中,X与Y可能发生的反应的化学方程式有________
________。
高三化学实验题中等难度题查看答案及解析
-
已知X、Y、Z、W、R是原子序数依次增大的短周期主族元素,其中只有一种金属元素,X是周期表中原子半径最小的元素,Y的最高正价与最低负价绝对值相等,W最外层电子数是最内层电子数的3倍,R是同周期元素中原子半径最小的元素。下列说法不正确的是
A. 原子半径Z>W>R
B. 对应的氢化物的热稳定性:R>W>Y
C. 单质Z可与R的最高价含氧酸发生置换反应
D. W与R所形成的简单离子均能影响水的电离平衡
高三化学选择题困难题查看答案及解析
-
已知有A、B、C、D、E五种短周期元素,其原子序数依次增大,A与B形成的共价化合物的水溶液呈碱性,C元素原子的最外层电子数是最内层电子数的
,D是同周期中单核离子半径最小的元素,E元素的最高正价与最低负价的代数和为6.下列叙述中错误的是
A. B元素的简单气态氢化物与E的氢化物化合,生成物的水溶液呈酸性
B. B、C、E最高价氧化物对应的水化物溶液均能与D元素的氧化物反应
C. 元素B、E分别与元素A构成的含有18个电子的分子中均含有非极性共价键
D. 最高价氧化物对应水化物的碱性:C>D
高三化学选择题中等难度题查看答案及解析
-
已知X、Y、Z、W、R是原子序数依次增大的短周期主族元素,X是周期表中原子半径最小的元素,Y元素的最高正价与最低负价绝对值相等,Z的核电荷数是Y的2倍,W最外层电子数是最内层电子数的3倍.下列说法不正确的是( )
A.原子半径:Z>W>R
B.对应氢化物的稳定性:R>W
C.W与X、W与Z形成的化学键类型完全相同
D.Y的最高价氧化物对应的水化物是弱酸高三化学选择题中等难度题查看答案及解析
-
已知X、Y、Z、W、R是原子序数依次增大的短周期主族元素,X是周期表中原子半径最小的元素,Y元素的最高正价与最低负价绝对值相等,Z的核电荷数是Y的2倍,W最外层电子数是最内层电子数的3倍.下列说法正确的是
A.微粒半径:Z2+>W2->R-
B.对应氢化物的稳定性:W>R
C.W与X、W与Z形成的化合物晶体类型相同
D.Y的最高价氧化物对应的水化物是弱酸
高三化学选择题中等难度题查看答案及解析