-
已知:
(1)H2(g)+1/2O2(g)=H2O(g) △H1=akJ/mol
(2)2H2(g)+O2(g)=2H2O(g) △H2=bkJ/mol
(3)H2(g)+1/2O2(g)=H2O(l) △H3=ckJ/mol
(4)2H2(g)+O2(g)=2H2O(l) △H4=dkJ/mol
下列关系式中正确的是( )
A. a<c<0 B. b>d>0 C. 2a=b<0 D. 2c=d>0
高三化学选择题中等难度题查看答案及解析
-
已知:(1)H2(g)+
O2(g)====H2O(g) ΔH1=" a" kJ·mol-1
(2)2H2(g)+O2(g)====2H2O(g) ΔH2=" b" kJ·mol-1
(3)H2(g)+
O2(g)====H2O(l) ΔH3=" c" kJ·mol-1
(4)2H2(g)+O2(g)====2H2O(l) ΔH4=" d" kJ·mol-1
下列关系式正确的是( )
A.a<c<0 B.b>d>0 C.2a=b<0 D.2c=d>0
高三化学选择题中等难度题查看答案及解析
-
已知(1)H2(g)+1/2O2(g)===H2O(g) △H1=a kJ·mol-1
(2)2H2(g)+O2(g)===2H2O(g) △H2=b kJ·mol-1
(3)H2(g)+1/2O2(g)===H2O(l) △H3=c kJ·mol-1
(4)2H2(g)+O2(g)===2H2O(l) △H4=d kJ·mol-1
下列关系式中正确的是:( )
A.a<c<0 B.b>d>0 C.2a=b<0 D.2c=d>0
高三化学选择题中等难度题查看答案及解析
-
已知:(1)H2(g)+1/2O2(g)===H2O(g) ΔH1=a kJ/mol
(2)2H2(g)+O2(g)===2H2O(g) ΔH2=b kJ/mol
(3)H2(g)+1/2O2(g)===H2O(l) ΔH3=c kJ/mol
(4)2H2(g)+O2(g)===2H2O(l) ΔH4=d kJ/mol下列关系式中正确的是 :
A.a<c<0 B.b>d>0 C.2a=b<0 D.2c=d>0
高三化学选择题简单题查看答案及解析
-
下列说法不正确的是
A.已知H2(g)+
O2(g)===H2O(g) ΔH1=a kJ·mol-1;
2H2(g)+O2(g)===2H2O(g) ΔH2=b kJ·mol-1,则a>b
B.CO的燃烧热为283.0 kJ·mol-1,则
2CO2(g)===2CO(g)+O2(g) ΔH=+566.0 kJ·mol-1
C.若N2(g)+3H2(g)
2NH3(g) ΔH=-d kJ·mol-1,故在某容器中投入1 mol N2与3 mol H2充分反应后,放出的热量小于d kJ
D.HCl和NaOH反应的中和热ΔH=-57.3 kJ·mol-1,则H2SO4和KOH反应的中和热ΔH=-114.6 kJ·mol-1
高三化学选择题中等难度题查看答案及解析
-
已知下列热化学方程式:
①H2(g)+1/2O2(g)=H2O(g) ΔH1=a kJ·mol-1
②2H2(g)+O2(g)=2H2O(g) ΔH2=b kJ·mol-1
③H2(g)+1/2O2(g)=H2O(l) ΔH3=c kJ·mol-1
④2H2(g)+O2(g)=2H2O(l) ΔH4=d kJ·mol-1
下列关系式中正确的是( )
A.a<c<0 B.b>d>0 C.2a=b<0 D.2c=d>0
高三化学选择题中等难度题查看答案及解析
-
(16分)一定条件下合成乙烯:
6H2(g)+2CO2(g)
CH2=CH2(g)+4H2O(g) △H1
已知:2H2(g)+O2(g)=2 H2O(g) △H2=-480 kJ•mol-1
CH2=CH2(g)+3O2(g)=2CO2(g)+2 H2O(g) △H3=-1400 kJ•mol-1
(1)△H1= 。请标出该反应电子转移的方向和数目 。
(2)温度对CO2的平衡转化率和催化剂催化效率的影响如图,下列说法正确的是 。
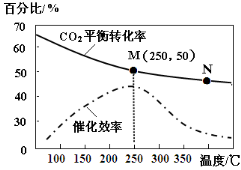
A.生成乙烯的速率:v(M)有可能小于v(N)
B.平衡常数:KM >KN
C.催化剂会影响CO2的平衡转化率
(3)若投料比n(H2)∶n(CO2)=3∶1,则图中M点时,乙烯的体积分数为 (保留两位有效数字)。
(4)为提高CO2的平衡转化率,除改变温度外,还可采取的措施有 (任写一条)。
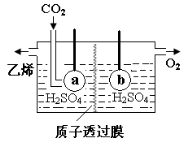
(5)电解法可制取乙烯(下图),电极a接电源的 极,该电极反应式为 。
高三化学填空题困难题查看答案及解析
-
(14分)质子交换膜燃料电池广受关注。
(1)质子交换膜燃料电池中作为燃料的H2通常来自水煤气。
已知:C(s)+O2(g)
CO(g) ΔH1=-110.35kJ·mol-1
2H2O(l)
2H2(g)+O2(g) ΔH2=+571.6kJ·mol-1
H2O(l)
H2O(g) ΔH3=+44.0kJ·mol-1
则C(s)+H2O(g)
CO(g)+H2(g) ΔH4= 。
(2)燃料气(流速为1800mL·h-1;体积分数为50% H2,0.98% CO,1.64% O2,47.38% N2)中的CO会使电极催化剂中毒,使用CuO/CeO2催化剂可使CO优先氧化而脱除。
①160 ℃、CuO/CeO2作催化剂时,CO优先氧化反应的化学方程式为 。
②灼烧草酸铈[ Ce2(C2O4)3]制得CeO2的化学方程式为 。
③在CuO/CeO2催化剂中加入不同的酸(HIO3或H3PO4),测得燃料气中CO优先氧化的转化率随温度变化如图1所示。
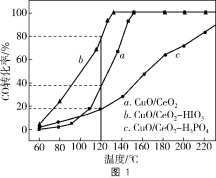
加入 (填酸的化学式)的CuO/CeO2催化剂催化性能最好。催化剂为CuO/CeO2—HIO3,120℃时,反应1h后CO的体积为 mL。
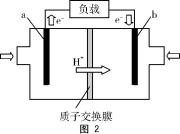
(3)图2为甲酸质子交换膜燃料电池的结构示意图。该装置中 (填“a”或“b”)为电池的负极,负极的电极反应式为 。
高三化学填空题极难题查看答案及解析
-
[2016·江苏]通过以下反应均可获取H2。下列有关说法正确的是
①太阳光催化分解水制氢:2H2O(l)
2H2(g)+O2(g) ΔH1=571.6 kJ·mol−1
②焦炭与水反应制氢:C(s)+H2O(g)
CO(g)+H2(g) ΔH2=131.3 kJ·mol−1
③甲烷与水反应制氢:CH4(g)+H2O(g)
CO(g)+3H2(g) ΔH3=206.1 kJ·mol−1
A.反应①中电能转化为化学能
B.反应②为放热反应
C.反应③使用催化剂,ΔH3减小
D.反应CH4(g)
C(s)+2H2(g)的ΔH=74.8 kJ·mol−1
高三化学选择题中等难度题查看答案及解析
-
通过以下反应均可获取H2.下列有关说法正确的是
①太阳光催化分解水制氢:2H2O(l)=2H2(g)+O2(g) △H1=+571.6kJ•mol﹣1
②焦炭与水反应制氢:C(s)+H2O(g)=CO(g)+H2(g) △H2=+131.3kJ•mol﹣1
③甲烷与水反应制氢:CH4(g)+H2O(g)
CO(g)+3H2(g) △H3=+206.1kJ•mol﹣1.
A. 反应CH4(g)= C(s)+2 H2(g)的△H=+74.8kJ•mol﹣1 。
B. 电解水也可制取氢气和氧气,而且比方法①更方便,更节能。
C. 反应②每生成2g氢气,要吸收131.3kJ的热量,所以该反应没有应用价值。
D. 反应③中,若将各1mol的甲烷与水蒸气混合,要吸收206.1kJ的热量。
高三化学单选题中等难度题查看答案及解析