-
某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如下图所示:
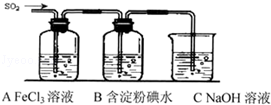
(1)SO2与Fe3+反应的还原、氧化产物分别是 、 (填离子符号)。
(2)下列实验方案可以用于在实验室制取所需SO2的是 。
A.Na2SO3溶液与HNO3
B.Na2SO3固体与浓硫酸
C.固体硫在纯氧中燃烧
D.铜与热浓H2SO4
(3)装置C的作用是 。
(4)如果有280mL SO2气体(已折算为标态)进入C装置中,则C中,50mL NaOH溶液的浓度至少为 mol/L才能达到目的。
(5)在上述装置中通入过量的SO2为了验证A中SO2与Fe3+发生了氧化还原反应,他们取A中的溶液,分成三份,并设计了如下实验:
方案①:往第一份试液中加入KMnO4溶液,紫红色褪去。
方案②:往第一份试液加入KSCN溶液,不变红,再加入新制的氯水,溶液变红。
 方案③:往第二份试液加入用稀盐酸酸化的BaCl2,产生白色沉淀。
方案③:往第二份试液加入用稀盐酸酸化的BaCl2,产生白色沉淀。
上述方案不合理的是 ,原因是 。
(6)能表明I﹣的还原性弱于SO2的现象是 ,写出有关离子方程式: 。
-
兴趣小组探究SO2气体还原Fe3+、I2,它们使用的药品和装置如图所示:
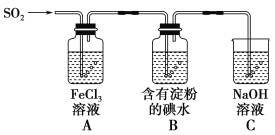
(1)SO2气体和Fe3+反应的氧化产物、还原产物分别是________、________
(2)下列实验方案适用于在实验室制取所需SO2的是________。
A.Na2SO3溶液与HNO3 B.Na2SO3固体与浓硫酸
C.固体硫在纯氧中燃烧 D.铜与浓H2SO4共热
(3)装置C的作用是__________________________________________________。
(4)装置B中反应的离子方程式_________________________________________________。
(5)在上述装置中通入过量的SO2,为了验证A中SO2与Fe3+发生了氧化还原反应,他们取A中的溶液,分成三份,并设计了如下实验:
方案①:往第一份试液中加入酸性KMnO4溶液,紫红色褪去。
方案②:往第二份试液中加入NaOH溶液,产生白色沉淀,并迅速转为灰绿,最后呈红褐色。
方案③:往第三份试液中加入用稀盐酸酸化的BaCl2,产生白色沉淀。
上述方案不合理的是方案_____,原因是__________________________________________________
-
某兴趣小组探究SO2气体还原Fe3+的反应,他们使用的药品和装置如下图所示,下列说法不合理的是( )
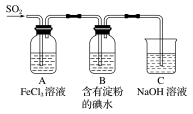
A.能表明I-的还原性弱 于SO2的现象是B中蓝色溶液褪色
于SO2的现象是B中蓝色溶液褪色
B.装置C的作用是吸收多余的SO2,防止污染空气
C.为了验证A中发生了氧化还原反应,加入用稀盐酸酸化的BaCl2,产生白色沉淀
D.为了验证A中发生了氧化还原反应,加入酸性KMnO4溶液,紫红色褪去
-
某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如下图所示。
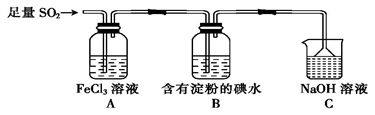
(1)装置C的作用是_____________________。
(2)①设计实验方案检验有Fe2+生成:_______________________。
②证明SO2气体还原I2的现象:_______________________。
(3)若要从A中所得溶液提取晶体,必须进行的实验操作步骤为蒸发、冷却结晶、过滤、自然干燥,在这一系列操作中没有用到的仪器有________(填字母)。
A.蒸发皿 B.试管夹 C.漏斗 D.烧杯 E.玻璃棒 F.坩埚
-
某兴趣小组探究SO2气体还原Fe3+,他们使用的药品和装置如图所示,下列说法合理的是
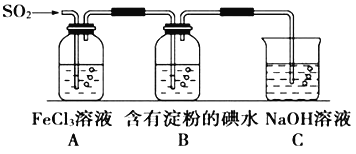
A. B中蓝色溶液褪色可以证明还原性:I->SO2
B. 实验完成后,检验A中是否含有Fe2+,可用酸性KMnO4溶液
C. 实验完成后,向A中加入用稀盐酸酸化的BaCl2溶液,产生白色沉淀
D. 装置C的作用是吸收SO2尾气,发生的反应是氧化还原反应
-
某校化学兴趣小组探究SO2与FeCl3溶液的反应,装置如下图所示。
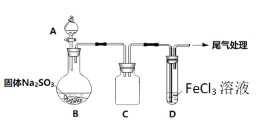
已知:
i.Fe(HSO3)2+离子为红棕色,它可以将Fe3+还原为Fe2+。
ii.生成Fe(HSO3)2+离子的反应为:Fe3+ +HSO ⇌Fe(HSO3)2+ 。
⇌Fe(HSO3)2+ 。
步骤一:实验准备:
如上图连接装置,并配制100mL 1.0 mol·L-1 FeCl3溶液(未用盐酸酸化),测其pH约为1,取少量装入试管D 中。
(1)配制100mL1.0 mol·L-1 FeCl3溶液用到的主要玻璃仪器为烧杯、玻璃棒、胶头滴管和______,装置C的作用为:________________。
(2)用离子方程式解释1.0 mol·L-1 FeCl3溶液(未用盐酸酸化)pH=1的原因:________
步骤二:预测实验
(3)该小组同学预测SO2与FeCl3溶液反应的现象为溶液由棕黄色变成浅绿色。
该小组同学预测的理论依据为:________________
步骤三:动手实验
(4)当SO2通入到FeCl3溶液至饱和时,同学们观察到的现象是溶液由棕黄色变成红棕色,将混合液放置12小时,溶液才变成浅绿色。
①SO2与FeCl3溶液反应生成了Fe(HSO3)2+离子的实验证据为:__________。证明浅绿色溶液中含有Fe2+的实验操作为:_____________ 。
②为了探究如何缩短红棕色变为浅绿色的时间,该小组同学进行了如下实验。
| 实验I | 往5mL1mol·L-1 FeCl3溶液中通入SO2气体,溶液立即变为红棕色。微热3 min,溶液颜色变为浅绿色。 |
| 实验II | 往5mL重新配制的1mol·L-1 FeCl3溶液(用浓盐酸酸化)中通入SO2气体,溶液立即变为红棕色。几分钟后,发现溶液颜色变成浅绿色。 |
综合上述实验探究过程,得出的结论为:____________。
步骤四:反思实验:
(5)在制备SO2的过程中,同学们发现,使用70%的硫酸比用98%的浓硫酸反应速率快,分析其中的原因是_________。
-
某兴趣小组欲在绿色环保的条件下探究大气污染物SO2的性质,设计如下图实验装置。请回答:

(1)B、C、D分别用于检验SO2的漂白性、还原性和氧化性,则B中所盛试剂为________; C中反应的离子方程式为________
(2)为了实现绿色环保的目标,某同学设计了上图A2的制取装置来代替A1装置,与A1装置相比,A2装置的优点是________
(3)试验中发现Na2SO3可能部分被氧化,现需测定Na2SO3的纯度:称取10.00g产品,配成100ml溶液,移取25.00ml溶液,用0.20mol/L酸性KMnO4溶液进行滴定,消耗KMnO4溶液20.00mL,产品中Na2SO3质量分数的计算表达式为________,计算结果为________。(保留两位小数)
-
某化学兴趣学习小组设计实验探究金属M与浓硫酸反应的气体产物。
【提出假设】假设1:气体产物只有SO2; 假设2:_____________;
【实验设计】为了探究金属M与浓硫酸反应产物,设计如图实验装置:一定量的浓硫酸与金属M反应.
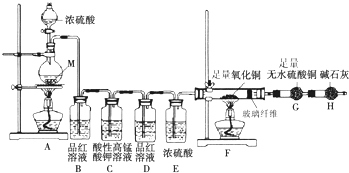
(1)检查上述装置气密性的一种方法是:关闭分液漏斗的活塞,在H装置后面连上一根导管,然后_____________,则证明装置的气密性良好。
(2)若B瓶里品红溶液褪色,E、F和G中都无明显现象.反应后硫酸盐中金属显+2价.写A中发生反应的化学方程式_____________;
(3)若假设2正确,则可观察到:F管中_____________;G干燥管里_____________;
【实验反思】为了进一步探究金属M成分和气体组分,进行如下实验:
称取11.2g金属M放入装置A中,加入一定量的浓硫酸,反应结束后,B瓶里品红溶液褪色,金属没有剩余,拆下G并称重,G增重0.9g。
(4)为了观察溶液颜色,实验完毕后,需要稀释烧瓶里溶液.稀释烧瓶里溶液的操作方法_______;
(5)将稀释后的溶液分装甲、乙试管,向甲试管里滴加KSCN溶液,溶液变红色;向乙试管里滴加酸性高锰酸钾溶液,振荡,溶液紫色褪去;所以可得到此条件下对金属M与浓硫酸反应的气体产物的探究假设 ________成立。
-
甲烷在加热条件下可还原氧化铜,气体产物除水蒸气外,还有碳的氧化物,某化学小组利用如图装置探究其反应产物。
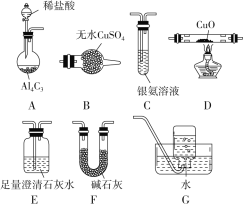
(查阅资料)
①CO能与银氨溶液反应:CO+2Ag(NH3)2++2OH-=2Ag↓+2NH4++CO32-+2NH3;
②Cu2O为红色,不与Ag+反应,发生反应:Cu2O+2H+=Cu2++Cu+H2O。
(1)装置A中反应的化学方程式为__________________________。
(2)按气流方向各装置从左到右的连接顺序为A→_____________________。
(3)实验中滴加稀盐酸的操作是_________________________。
(4)已知气体产物中含有CO,则装置C中可能观察到的现象是___________________________;装置F的作用为____________________。
(5)当反应结束后,装置D处试管中固体全部变为红色。
①设计实验证明红色固体中含有Cu2O:______;
②欲证明红色固体中是否含有Cu,甲同学设计如下实验:向少量红色固体中加入适量的0.1 mol/L AgNO3溶液,发现溶液变蓝,据此判断红色固体中含有Cu。乙同学认为该方案不合理,欲证明甲同学的结论,还需要增加对比实验,完成表中内容。
| 实验步骤(不要求写出具体的操作过程) | 预期现象与结论 |
| ________________________ | 若观察到溶液不变蓝,则证明红色固体中含有Cu |
-
某实验小组用如图所示装置进行实验以探究Fe3+、Cl2和SO2的氧化性强弱(夹持仪器已略)。
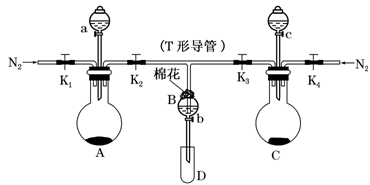
(1)按图连接好装置,检查装置的气密性后添加药品:向A装置的分液漏斗中加入浓盐酸,在圆底烧瓶中加入固体KMnO4;向B装置中加入10 mL FeCl2溶液,棉花浸润________溶液;在C装置的分液漏斗中加入70%的硫酸,向圆底烧瓶中加入固体Na2SO3。
(2)打开弹簧夹K1~K4,通入一段时间N2,再将T形导管插入B中,继续通入N2。通入一段时间N2的目的是__________________。
(3)关闭K1,K3,K4,打开活塞a 和K2,逐滴加入浓盐酸,A装置中发生反应的方程式为___________。
(4)当B中溶液变为棕黄色时,停止滴加浓盐酸,夹紧K2,打开活塞b,使约2 mL的溶液流入D试管中,分别取1 mL溶液滴入_______(填试剂名称)和铁氰化钾溶液可以证明其中含有Fe3+和Fe2+。此时B中发生反应的离子方程式为____________。
(5)打开K3和活塞c,逐滴加入70%的硫酸,当B中溶液颜色逐渐变为_____色,停止滴加70%的硫酸,夹紧K3,打开活塞b,使约2 mL的溶液流入D试管中,并检验其中的离子。此时B中发生反应的离子方程式为______________。
(6)结合实验现象判断Fe3+、Cl2、SO2氧化性由强到弱的顺序为___________。

方案③:往第二份试液加入用稀盐酸酸化的BaCl2,产生白色沉淀。








