-
(8分)氯化溴(BrCl)的化学性质类似于卤素单质,试回答下列问题:
(1)氯化溴的电子式是________,它是由________键形成的分子。
(2)氯化溴和水反应生成了一种三原子分子,该分子的电子式为________。
高二化学填空题简单题查看答案及解析
-
(8分)溴化碘(IBr)的化学性质类似于卤素单质,试回答下列问题:
(1)溴化碘的电子式是________,它是由________键形成的________
________分子。(填极性或非极性)
(2)溴化碘和水反应生成了一种三原子分子,该分子的电子式为________,
它的VSEPR模型是 ,分子构型是 。
高二化学填空题简单题查看答案及解析
-
溴化碘(IBr)的化学性质类似于卤素单质,试完成下列问题:
(1)溴化碘的电子式是 ,它是由 键形成的 分子.
(2)溴化碘和水反应生成了一种三原子分子,该分子的电子式为 .
高二化学填空题简单题查看答案及解析
-
卤素互化物与卤素单质性质相似。已知
(1,3—丁二烯)与氯气发生加成产物有三种:①
(1,2—加成)②
(1,4—加成)③
(完全加成)。据此推测
(异戊二烯)与卤素互化物BrCl的加成产物有几种(不考虑立体异构)( )
A.6种 B.10种 C.12种 D.14种
高二化学单选题困难题查看答案及解析
-
氯化溴(BrCl)结构和性质类似Br2 、 Cl2下列叙述正确的是
A BrCl是离子化合物 B . Br-Cl键长大于Cl-Cl键长
C. BrCl 和Br2中都存在极性键 D. BrCl和 Cl2都是非极性分子
高二化学选择题中等难度题查看答案及解析
-
在1981年才第一次制得卤族元素的第五个成员砹,根据卤素性质的变化规律,我们可以预料砹的下列性质不正确的是( )
A.砹单质在室温下的状态是固体,颜色比碘深,单质能溶于四氯化碳
B.砹原子得电子能力比碘强
C.AgAt的颜色比AgI 深,HAt的稳定性比HI弱
D.单质砹是卤素中弱氧化剂,而砹离子是卤族中的强还原剂
高二化学单选题中等难度题查看答案及解析
-
卤素的单质和化合物种类很多,我们可以利用所学物质结构与性质的相关知识去认识和理解它们。回答下列问题:
(1)溴原子的价层电子排布图为_______。根据下表提供的第一电离能数据,判断最有可能生成较稳定的单核阳离子的卤素原子是________(填元素符号)。
氟
氯
溴
碘
第一电离能/ (kJ·mol-1)
1 681
1 251
1 140
1 008
(2)氢氟酸在一定浓度的溶液中主要以二分子缔合[(HF)2]形式存在,使氟化氢分子缔合的相互作用是____________。碘在水中溶解度小,但在碘化钾溶液中明显增大,这是由于发生反应:I-+I2=I3-,CsICl2与KI3类似,受热易分解,倾向于生成晶格能更大的物质,试写出CsICl2受热分解的化学方程式:_________________________________。
(3)ClO2-中心氯原子的杂化轨道类型为________,与ClO2-具有相同立体构型和键合形式的物质的化学式为____________(写出一个即可)。
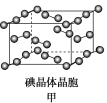
(4)如图甲为碘晶体晶胞结构,平均每个晶胞中有________个碘原子,碘晶体中碘分子的配位数为____________。
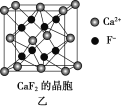
(5)已知NA为阿伏加德罗常数,CaF2晶体密度为ρ g·cm-3,其晶胞如图乙所示,两个最近Ca2+核间距离为a nm,则CaF2的相对分子质量可以表示为____________。
高二化学综合题中等难度题查看答案及解析
-
卤素单质及其化合物是物质世界不可缺少的组成部分。请利用所学物质结构与性质的相关知识回答下列问题:
(1)At原子的核外价电子排布式为______________________;I3+中心原子杂化方式为_______;ClO2-的空间构型为__________。基态氟原子核外电子有________种空间运动状态。
(2)已知高碘酸有两种结构,化学式分别为H5IO6(
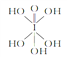 )和HIO4;前者为五元酸,后者为一元酸,请比较二者的酸性强弱:H5IO6 ______HIO4(填“>”、“=”或“<”).
)和HIO4;前者为五元酸,后者为一元酸,请比较二者的酸性强弱:H5IO6 ______HIO4(填“>”、“=”或“<”).(3)TiCl4熔点为-24℃,沸点为136.4℃。可溶于甲苯,固态TiCl4属于_________晶体。
(4)用锌还原TiCl4的盐酸溶液,可制得绿色配合物[TiCl(H2O)5]Cl2·H2O。1mol该配合物中含有σ键数目为__________。
(5)CaF2晶胞结构如下图
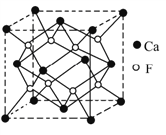
①晶体中距离最近的2个Ca2+(X)与一个F-(Y)形成的夹角(∠XYX)为___________。
②CaF2的摩尔质量为78g/mol,晶胞密度为ρg/cm3,阿伏加德罗常数为NA,则晶体中两个最近的Ca2+间中心距离为____________cm
高二化学综合题中等难度题查看答案及解析
-
溴化碘(IBr)的化学性质类似于卤素单质,能与大多数金属反应生成金属卤化物,和非金属反应生成相应的卤化物,与水反应的化学方程式为IBr+H2O====HBr+HIO,则下列关于IBr的叙述不正确的是
A.IBr是共价化合物
B.IBr在很多反应中是强氧化剂
C.IBr跟H2O反应时既不是氧化剂也不是还原剂
D.IBr跟NaOH溶液反应生成NaBrO、NaI和H2O
高二化学选择题中等难度题查看答案及解析
-
铁的单质及化合物在研究和生产中有多种用途。根据所学知识回答下列问题:
(1)Fe3+价电子排布式为______________,并解释Fe2+还原性强的原因_______________。
(2)类卤素离子SCN-是检验Fe3+的试剂之一,与SCN-互为等电子体的一种物质的分子式 为_____________。
(3)①已知 Fe3C 的晶胞结构中碳原子的配位数为6,与碳原子紧邻的铁原子组成的空间构型为____________________,铁原子的配位数是___________。
②铁的某种化合物结构简式如图1所示,组成上述化合物中的第二周期元素原子的电负性由大到小的顺序为_________________________,上述化合物中氮原子的杂化方式为_____________,在图1中用“→”标出Fe元素周围的配位键_____。
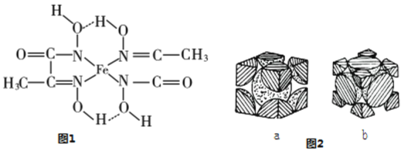
(4)铁单质的堆积方式有以下两种,其剖面图分别如图2 a、b 所示。其中属于面心立方最密堆积的是_______(填“a”或“b”),此晶体中原子的总体积占晶体体积的比例为____________________(用含圆周率π的代数式表示)。
高二化学综合题中等难度题查看答案及解析