20mL 0.1000 mol•L-1氨水用0.1000 mol•L-1的盐酸滴定,滴定曲线入右下图,下列说法正确的是
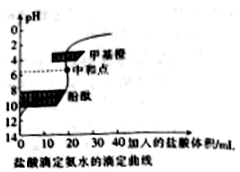
A. 该中和滴定适宜用酚酞作指示剂
B. 两者恰好中和时,溶液的pH=7
C. 达到滴定终点时,溶液中:c(H+)= c(OH-)+ c(NH3·H2O)
D. 当滴入盐酸达30mL时,溶液中c(NH4+)+c(H+)-)+c(Cl-)
高三化学选择题中等难度题
20mL 0.1000 mol•L-1氨水用0.1000 mol•L-1的盐酸滴定,滴定曲线入右下图,下列说法正确的是

A. 该中和滴定适宜用酚酞作指示剂
B. 两者恰好中和时,溶液的pH=7
C. 达到滴定终点时,溶液中:c(H+)= c(OH-)+ c(NH3·H2O)
D. 当滴入盐酸达30mL时,溶液中c(NH4+)+c(H+)-)+c(Cl-)
高三化学选择题中等难度题
20mL 0.1000 mol•L-1氨水用0.1000 mol•L-1的盐酸滴定,滴定曲线入右下图,下列说法正确的是

A. 该中和滴定适宜用酚酞作指示剂
B. 两者恰好中和时,溶液的pH=7
C. 达到滴定终点时,溶液中:c(H+)= c(OH-)+ c(NH3·H2O)
D. 当滴入盐酸达30mL时,溶液中c(NH4+)+c(H+)-)+c(Cl-)
高三化学选择题中等难度题查看答案及解析
25℃时,用0.1000mol·L-1的盐酸分别滴定20.00mL 0.1000mol·L-1氨水和20.00mL 0.1000mol·L-1 NaOH溶液,滴定曲线如图所示。下列说法不正确的是
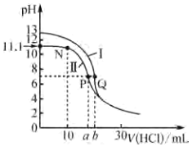
A.25℃,Kb(NH3·H2O)的数量级为10-5
B.N点处的溶液中:c(NH)>c(NH3·H2O)
C.曲线II滴定终点时所选的指示剂为酚酞
D.Q点所加盐酸的体积为b mL,则b=20
高三化学单选题简单题查看答案及解析
下图为常温下用0.1000molNaOH溶液滴定20.00mL 0.1000mol
盐酸和20.00mL 0.1000mol
醋酸的曲线。若以HA表示酸,下列判断和说法正确的是

A.上左图是滴定盐酸的曲线
B.E点时溶液中离子浓度为c()
c(
)
C.B点时,反应消耗溶液体积:V(NaOH)<V(HA)
D.当0mL<V(NaOH) <20.00mL时,两溶液中各离子浓度大小顺序一定均为c()>c(
)>c(
)>c(
)
高三化学选择题中等难度题查看答案及解析
室温下,用0.1000mol/L盐酸分别滴定20.00mL浓度均为0.1000mol/L氢氧化钠溶液和氨水,滴定过程中溶液pH随加入盐酸体积V[HCl(aq)]的变化关系如图所示。下列说法正确的是

A. Ⅰ表示是滴定氨水的曲线,V[HCl(aq)]=20mL时:c(Cl-)>c(NH4+)>c(H+)>c(OH-)
B. pH=7时,两种溶液中:c(Na+)=c(NH4+)
C. 滴定氢氧化钠溶液,V[HCl(aq)]>20mL时可能有c(Cl-)>c(Na+)>c(H+)>c(OH-)
D. 消定氨水时,当V[HCl(aq)]=10mL时,有2[c(OH-)-c(H+)]=c(NH4+)-c(NH3·H2O)
高三化学单选题困难题查看答案及解析
用0.1000mol/L的标准盐酸分别滴定20.00mL的0.1000mol/L氨水和20.00mL的0.1000mol/L氢氧化钠溶液的滴定曲线如图所示,横坐标为滴定百分数(滴定用量/总滴定用量),纵坐标为滴定过程中溶液pH,甲基红是一种酸碱指示剂,变色范围为4.4-6.2,下列有关滴定过程说法正确的是

A. 滴定氨水溶液当滴定分数为50%时,各离子浓度间存在关系:c(NH4+)+c(H+)=c(OH-)
B. 滴定分数为100%时,即为滴定过程中反应恰好完全的时刻
C. 从滴定曲线可以判断,使用甲基橙作为滴定过程中的指示剂准确性更佳
D. 滴定氨水溶液当滴定分数为150%时,所得溶液中离子浓度有大小关系c(Cl-)>c(H+)
高三化学选择题中等难度题查看答案及解析
下图为常温下用0.1000 mol·L-1 NaOH溶液滴定20.00 mL 0.1000 mol·L-1盐酸和20.00 mL 0.1000 mol·L-1醋酸的曲线。若以HA表示酸,下列判断和说法正确的是
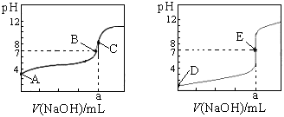
A.左图是滴定盐酸的曲线
B.E点时溶液中离子浓度为c(Na+) = c(A—)
C.B点时,反应消耗溶液体积:V(NaOH) <V(HA)
D.当0 mL< V(NaOH) < 20.00 mL时,对应溶液中各离子浓度大小顺序一定均为c(A-) >c(Na+)> c(H+) > c(OH-)
高三化学选择题困难题查看答案及解析
下图是用0.1000 mol·L-1 NaOH溶液滴定20.00 mL未知浓度盐酸(酚酞做指示剂)的滴定曲线。下列说法正确的是
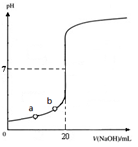
A.水电离出的氢离子浓度:a>b
B.盐酸的物质的量浓度为0.0100 mol·L-1
C.指示剂变色时,说明盐酸与NaOH恰好完全反应
D.当滴加NaOH溶液10.00 mL时,该混合液的pH= 1+lg3
高三化学选择题中等难度题查看答案及解析
25℃时,取浓度为0.1000 mol·L-1的氨水20.00 mL,用0.1000 mol·L-1盐酸滴定,过程中pH随滴加溶液的体积变化关系如图所示:
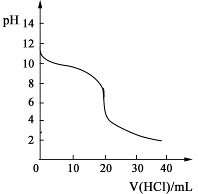
下列说法正确的是( )
A. 25℃时Kb (NH3·H2O) ≈10-5
B.滴定过程中水的电离程度一直保持增大趋势
C.为使终点现象更加明显可多加上几滴甲基橙
D.滴定终点时c(NH4+)=c(Cl-)> c(H+)=c(OH-)
高三化学选择题困难题查看答案及解析
用 0.1000 mol·L−1 NaOH 溶液分别滴定 20.00 mL 0.1000 mol·L−1 的盐酸和醋酸,滴定曲线如图所示,下列说法正确的是
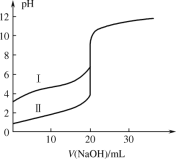
A.Ⅰ、Ⅱ分别表示盐酸和醋酸的滴定曲线
B.V(NaOH) = 10.00 mL 时,醋酸溶液中c(CH3COOH)<c(CH3COO−)
C.pH = 7 时,滴定盐酸消耗的 NaOH 溶液体积小于滴定醋酸消耗的 NaOH 溶液体积
D.V(NaOH) = 20.00 mL 时,两溶液中 c(CH3COO−)=c(Cl−)
高三化学单选题中等难度题查看答案及解析
25℃时,用0.1000 mol·L-1NaOH溶液分别滴定20.00ml 0.1000 mol·L-1的盐酸和醋酸,滴定曲线如图所示,下列说法正确的是( )
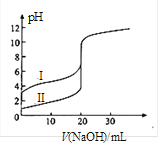
A. Ⅰ、Ⅱ分别表示盐酸和醋酸的滴定曲线
B. pH=7时,滴定盐酸和醋酸消耗NaOH溶液的体积相等
C. V(NaOH) =10.00mL时,醋酸溶液中c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
D. V(NaOH) =20.00mL时,两溶液中c(CH3COO-)>c(Cl-)
高三化学单选题中等难度题查看答案及解析