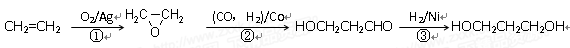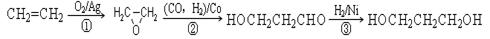-
(12分)利用焦炭或天然气制取廉价的CO和H2,再用于氨合成和有机合成是目前工业生产的重要途径。回答下列问题:
(1)甲烷在高温下与水蒸气反应的化学方程式为:CH4+H2O=CO+3H2。部分物质的燃烧热数据如下表:
| 物 质 | 燃烧热(kJ·mol-1) |
| H2(g) | -285.8 |
| CO(g) | -283.0 |
| CH4(g) | -890.3 |
已知1 mol H2O(g)转变为1 mol H2O(l)时放出44.0 kJ热量。写出CH4和水蒸气在高温下反应的热化学方程式________。
(2)500℃、50MPa时,在容积为V L的容器中加入1 mol N2、3 mol H2,,此时N2的转化率为a。则平衡时NH3的浓度为________。
(3)1,3―丙二醇是重要的化工原料,用乙烯合成1,3―丙二醇的路线如下:
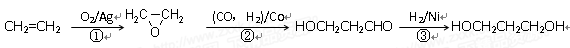
某化工厂已购得乙烯11.2 t,考虑到原料的充分利用,反应②、③所需的CO和H2可由以下两个反应获得:
C+H2O CO+H2 CH4+H2O
CO+H2 CH4+H2O CO+3H2
CO+3H2
假设在生产过程中,反应①、②、③中各有机物的转化率均为100%。且反应②中CO和H2、反应③中H2的转化率都为80%,计算至少需要焦炭________吨、甲烷________吨,
才能满足生产需要。
-
 利用焦炭或天然气制取廉价的CO和H2,再用于氨合成和有机合成是目前工业生产的重要途径。回答下列问题:
利用焦炭或天然气制取廉价的CO和H2,再用于氨合成和有机合成是目前工业生产的重要途径。回答下列问题:
(1)甲烷在高温下与水蒸气反应的化学方程式为:CH4+H2O CO+3H2。部分物质的燃烧热数据如下表:
| 物 质 | 燃烧热(kJ·mol-1) |
| H2(g) | -285.8 |
| CO(g) | -283.0 |
| CH4(g) | -890.3 |
已知1 mol H2O(g)转变为1 mol H2O(l)时放出44.0 kJ热量。写出CH4和水蒸气在高温下反应的热化学方程式。
(2)500℃、50MPa时,在容积为V L的容器中加入1 mol N2、3 molNH3,反应达平衡后测得平衡常数为K,此时CH4的转化率为a。则K和a的关系是K=。
(3)1,3―丙二醇是重要的化工原料,用乙烯合成1,3―丙二醇的路线如下:
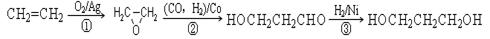
某化工厂已购得乙烯11.2 t,考虑到原料的充分利用,反应②、③所需的CO和H2可由以下两个反应获得:C+H2O CO+H2 CH4+H2O
CO+H2 CH4+H2O CO+3H2
CO+3H2
假设在生产过程中,反应①、②、③中各有机物的转化率均为100%。且反应②中CO和H2、反应③中H2的转化率都为80%,计算至少需要焦炭、甲烷各多少吨,才能满足生产需要?
-
利用焦炭或天然气制取廉价的CO和H2,再用于有机合成是目前工业生产的重要途径.回答下列问题:
(1)甲烷在高温下与水蒸气反应的化学方程式为:CH4+H2O═CO+3H2.部分物质的燃烧热数据如下表:
| 物 质 | 燃烧热 |
| H2(g) | -285.8 |
| CO(g) | -283.0 |
| CH4(g) | -890.3 |
已知1mol H2O (g)转变为1mol H2O(l)时放出44.0kJ热量.则CH4和水蒸气在高温下反应生成1mol H2的反应热为______.
(2)用CO和H2在一定条件下合成甲醇:CO+2H2⇌CH3OH.工业上采用稍高的压强(5MPa)和250℃,其可能原因是______.
| 反应温度/℃ | 平衡常数 | 反应温度/℃ | 平衡常数 |
| 667.30 | 200 | 1.909×10-2 |
| 100 | 12.92 | 300 | 2.42×10-4 |
(3)1,3-丙二醇是重要的化工原料,用乙烯合成1,3-丙二醇的路线如下:
CH2=CH2 HOCH2CH2CHO
HOCH2CH2CHO  HOCH2CH2CH2OH
HOCH2CH2CH2OH
某化工厂已购得乙烯11.2t,考虑到原料的充分利用,反应②、③所需的CO和H2可由以下两个反应获得:
C+H2O CO+H2 CH4+H2O
CO+H2 CH4+H2O  CO+3H2
CO+3H2
假设在生产过程中,反应①、②、③中各有机物的转化率均为100%.且反应②中CO和H2、反应③中H2的转化率都为80%,计算至少需要焦炭、甲烷各多少吨,才能满足生产需要?______.
-
利用焦炭或天然气制取廉价的CO和H2,再用于氨合成和有机合成是目前工业生产的重要途径.
(1)已知:CH4(g)+2O2 (g)=CO2 (g)+2H2O (l)△H=-890.3kJ•mol-1 ①
H2(g)+1/2O2 (g)=H2O (l)△H=-285.8kJ•mol-1 ②
CO(g)+1/2O2(g)=CO2(g)△H=-283.0kJ•mol-1 ③
H2O(g)=H2O(l)△H=-44.0kJ•mol-1 ④
反应CH4(g)+H2O(g) CO(g)+3H2(g),△H=________kJ•mol-1.标准状况下33.6L甲烷高温下与水蒸气完全反应生成CO和H2,反应过程中转移________mole-,放出________kJ热量.
CO(g)+3H2(g),△H=________kJ•mol-1.标准状况下33.6L甲烷高温下与水蒸气完全反应生成CO和H2,反应过程中转移________mole-,放出________kJ热量.
(2)一定条件下,在体积为5L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g)⇌CH3OH(g).不同温度时甲烷的物质的量随时间变化曲线如图所示.根据题意完成下列各题:
①反应达到平衡时,平衡常数表达式K=________,降低温度,K值________(填“增大”、“减小”或“不变”).
②在300℃,从反应开始到平衡,氢气的平均反应速率v(H2)=________.(用相关符号和数据表示)
③判断该可逆反应达到平衡状态的标志是________.(填字母)
a.CH3OH的生成速率与CO的消耗速率相等 b.容器中气体的压强不变
c.容器中混合气体的密度保持不变 d.CO百分含量保持不变
e.CO和CH3OH浓度相等
④欲提高H2的转化率,下列措施可行的是________.(填字母)
a.向容器中再充入Ar b.改变反应的催化剂
c.向容器中再充入CO d.升高温度.

-
氰化钠(NaCN)是重要的化工原料,常用于化学合成、冶金工业等。回答下列问题:
(1)下列标志中,应贴在装有氰化钠容器上的是 。

(2)写出NaCN的电子式 。
(3)可用纯碱、焦炭、氨气反应制取NaCN,写出反应的化学方程式,并用单线桥标明电子转移的方向和数目 。
(4)现代采金技术先以NaCN溶液在自然环境中浸取粉碎的含金(Au)矿石,得到Na[Au(CN)2](二氰合金酸钠)溶液,再用锌还原Na[ Au(CN)2]生成金。“浸取”反应的氧化剂是 ,消耗的锌与生成的金的物质的量之比为 。
(5)工业利用NaCN制备蓝色染料的流程如下:
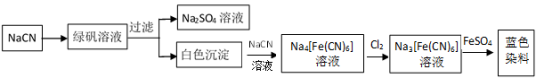
通入Cl2时发生反应的离子方程式为_ _,该蓝色染料的化学式为 。
-
氰化钠(NaCN)是重要的化工原料,常用于化学合成、冶金工业等.回答下列问题:
(1)可用纯碱、焦炭、氨气反应制取 NaCN,同时还有水生成,写出反应的化学方程式,并标明电子转移的方向和数目______________;
(2)现代采金技术先以NaCN溶液在自然环境中浸取粉碎的含金(Au)矿石,得到 Na[Au(CN)2](二氰合金酸钠)溶液,再用锌还原 Na[Au(CN)2]生成金,“浸取”反应的还原产物是______________;
(3)下图为用含NaCN的废水合成黄血盐(K4Fe(CN)6)的主要工艺流程如图:
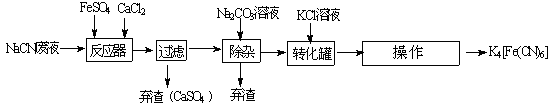
已知相同温度下溶解度:Na4Fe(CN)6>K4Fe(CN)6
① 实验室用NaCN固体配制NaCN溶液时,应先将其溶于______________溶液,再用蒸馏水稀释。
②在转化罐中发生反应的化学方程式为______________。
③加入碳酸钠溶液主要目的是______________。
④“操作”环节具体为______________。
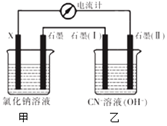
(4)CN -可以造成水体污染,某小组用如下方法对此污水进行处理如下图装置模拟电化学法处理CN -,有关结果见表.
| 实验序号 | 电极(X) | NaCl溶液浓度(mol/L) | 甲中石墨表面通人气体 | 电流计读数(A) |
| (1) | Fe | 0.l | 空气 | I |
| (2) | Al | 0.1 | 空气 | 1.5Ⅰ |
| (3) | Fe | 0.1 | 02 | 2Ⅰ |
| (4) | Al | 0.5 | 空气 | 1.6Ⅰ |
①若乙池中石墨(I)极产生无毒无害的物质,其电极反应式为___________;
②该实验表明电化学法处理CN -时,影响处理速率的因素有___________、___________(任答两点)
-
利用天然气制取合成气,然后用合成气合成多种有机物是目前部分有机物的重要来源。
I.甲烷制取合成气时,在同一容器中同时发生的主要反应是:
反应①: CH4(g)+H2O(g) CO(g)+3H2(g) △H =+206.3 kJ mol-l
CO(g)+3H2(g) △H =+206.3 kJ mol-l
反应②: CH4(g)+2O2(g) CO2(g)+2H2O(g) △H =-802.6 kJmol-l
CO2(g)+2H2O(g) △H =-802.6 kJmol-l
(1)下列有关合成气制取的说法中正确的是_____。
A.升温时反应①的正反应速率增大,逆反应速率减小,平衡正向移动
B.反应②因为反应物和生成物的计量数相等,所以△S=0
C.反应②放出的热可以提供反应①所需的热量
D.在恒温恒容容器中,气体密度保持不变时,反应达到化学平衡状态
(2)在制取合成气的初始阶段,反应②的反应速率大于反应①的反应速率,请用碰撞理论解释原因______。
(3)在某密闭容器中加入一定量的CH4、H2O,在温度为T1时发生反应①,t1时达到化学平衡状态,氢气浓度[c(H2)]随时间(t)的变化如图。控制其它条件不变,在温度为T2时(T2<T1)发生反应,在图中画出c(CO)变化曲线_____。
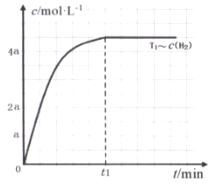
II.合成己烷时发生的反应是∶
主反应:反应③6CO(g)+13H2(g) C6H14(g)+6H2O(g) △H
C6H14(g)+6H2O(g) △H
副反应:反应④CO(g)+ H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
反应⑤2CO(g) CO2(g)+C(s)
CO2(g)+C(s)
反应③的平衡常数的对数(lgK)随温度(T/K)的变化如图1,在固定的氢碳比[m(H2)/m(CO)]条件下CO的平衡转化率[a(CO)]随温度变化的曲线如图2.
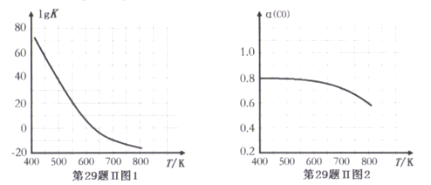
请回答∶
(1)反应③的△H______0 (填“>”“="或“<")
(2) 600K前随温度升高反应③的平衡转化率几乎不变,结合图1说明原因(副反应影响可忽略)_____。
(3)工业生产需要选择适合的条件提高综合效益,下列对工业合成已烷的说法中正确的是(______)
A.减少体系中的水蒸气,有利于提高生产效益
B.在体系中加入并保持一定量的二氧化碳有利于减少副反应的发生
C.在体系中加入并保持一定量的碳有利于工业合成已烷
D.工业生产中,选择的压强越高越有利于提高综合效益
-
氨气是一种重要的化工产品,在生产和科研中应用广泛,氢气是工业合成氨的原料之一,工业上制取氨气有下列两种途径:
途径一、用水和天然气作原料一步反应制得
途径二,用煤和水作原料经多步反应制得
请回答下列问题:
(1)途径一反应的还原产物是______。
(2)途径二中的一步反应为:
①上述反应达到平衡后,为提高CO的转化率,下列措施中正确的是______ 填写序号
填写序号 。
。
A.增大压强  降低温度
降低温度  增大
增大 的浓度
的浓度  使用催化剂
使用催化剂
②已知1000K时,上述反应的平衡常数 ,若要使CO的转化率超过
,若要使CO的转化率超过 ,则起始时
,则起始时 :
: 不低于______。
不低于______。
③在容积为2L的容器中发生上述反应,测得 与反应时间t的变化曲线Ⅰ如图1所示,若在
与反应时间t的变化曲线Ⅰ如图1所示,若在 时刻将容器的体积扩大至4L,请在答题卡图中绘出
时刻将容器的体积扩大至4L,请在答题卡图中绘出 与反应时间变化的曲线Ⅱ。____________
与反应时间变化的曲线Ⅱ。____________
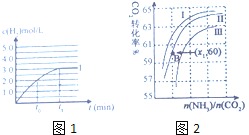
(3)目前常用氨气处理硝酸生产的工业尾气,在 左右且有催化剂存在的情况下,氨气能把
左右且有催化剂存在的情况下,氨气能把 还原成无色无毒气体,直接排入空气中,已知氢气的燃烧热为
还原成无色无毒气体,直接排入空气中,已知氢气的燃烧热为 ,
, ,
, 。试写出氨气与
。试写出氨气与 反应生成无毒气体和液态水的热化学方程式______。
反应生成无毒气体和液态水的热化学方程式______。
(4)工业上用氨和二氧化碳反应合成尿素,其反应为:CO2+2NH3=CO(NH2)2+H2O; 生成过程中,原料气常混有水蒸气,
生成过程中,原料气常混有水蒸气, 的转化率与氨碳比
的转化率与氨碳比 、水碳比
、水碳比 的变化关系如图2所示:
的变化关系如图2所示:
①曲线Ⅰ、Ⅱ、Ⅲ对应的水碳比最小的是______。
②若B点氨的转化率为 ,则
,则 ______。
______。
(5)某同学将 和
和 按物质的量之比2:1通入水中,充分反应所得溶液中
按物质的量之比2:1通入水中,充分反应所得溶液中 、
、 、
、 三种离子浓度由大到小的顺序是______
三种离子浓度由大到小的顺序是______ 已知:氨水、碳酸的电离平衡常数如表
已知:氨水、碳酸的电离平衡常数如表
-
(共10分)二甲醚是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用。工业上可利用焦炭与水蒸气在高温下的反应产物(水煤气)合成二甲醚。请回答下列问题:
(1)、制水煤气的主要化学反应方程式为: 。
(2)、煤的气化过程中产生的有害气体H2S用Na2CO3溶液吸收,生成两种酸式盐,该反应的化学方程式为: 。
(3)、利用水煤气合成二甲醚的三步反应如下:
① 2H2(g) CO(g)
CO(g) CH3OH(g)
CH3OH(g) 90.8 kJ
90.8 kJ
② 2CH3OH(g) CH3OCH3(g)
CH3OCH3(g) H2O(g)
H2O(g) 23.5 kJ
23.5 kJ
③ CO(g) H2O(g)
H2O(g) CO2(g)
CO2(g) H2(g)
H2(g) 41.3 kJ
41.3 kJ
总反应:3H2(g) 3CO(g)
3CO(g) CH3OCH3(g)
CH3OCH3(g) CO2(g)
CO2(g) Q,其中Q
Q,其中Q kJ;
kJ;
一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是
(填字母代号)。
a.低温高压 b.加入催化剂 c.减少CO2的浓度 d.增加CO的浓度
(4)、已知某温度下反应②2CH3OH(g) CH3OCH3(g)
CH3OCH3(g) H2O(g)在一密闭容器中进行到10min时恰好达平衡,测得各组分的浓度如下:
H2O(g)在一密闭容器中进行到10min时恰好达平衡,测得各组分的浓度如下:
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol·L ) ) | 0.44 | 0.6 | 0.6 |
比较此时正、逆反应速率数值(单位相同)的大小: (甲醇)
(甲醇)  (水)(填“>”、“<”或“=”)。
(水)(填“>”、“<”或“=”)。
反应开始时 (CH3OH)
(CH3OH) ________ ;
________ ;
该时间内的平均反应速率 (CH3OH)
(CH3OH) ;
;
该温度下反应的平衡常数值为 。(精确到0.01)
-
Ⅰ.CO和H2的混合气体俗称合成气,是一种重要的工业原料气,工业上利用天然气(主要成分为CH4)与水进行高温重整制备合成气。
(1)用甲烷与水蒸气制备合成气,每生成1mol合成气,需要供给51.5 kJ热量。该反应的热化学方程式为_____________________________________________________。
(2)在一定温度下,向体积为2L的密闭容器中充入0.40mol CH4和0.60mol H2O(g),发生反应: CH4(g) + H2O(g)  CO(g) + 3H2(g)。测得CH4和H2的物质的量浓度随时间变化如下表所示:
CO(g) + 3H2(g)。测得CH4和H2的物质的量浓度随时间变化如下表所示:
| 时间/min 物质的浓度(mol/L) | 0 | 1 | 2 | 3 | 4 |
| CH4 | 0.2 | 0.13 | 0.1 | 0.1 | 0.09 |
| H2 | 0 | 0.21 | 0.3 | 0.3 | 0.33 |
①该反应第一次达平衡时的平衡常数K=_______________。
②3min时改变的反应条件是__________________(只填一种条件的改变即可)。
(3)已知一定压强下,温度、投料比X[n(CH4)/n(H2O)]对该反应的影响如图所示。图1中的两条曲线所示投料比的关系X1 ______X2(填“=”、“>”或“<”)。
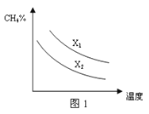
Ⅱ.(4)已知常温下HCOOH的电离常数为 ,则HCOO—的水解反应HCOO- + H2O
,则HCOO—的水解反应HCOO- + H2O  HCOOH + OH-的平衡常数K h =__________________。
HCOOH + OH-的平衡常数K h =__________________。
(5)常温下,将a mol/L的HCOOH溶液与a/2mol/L的NaOH溶液等体积混合后,溶液中各离子浓度由大到小的顺序是______________________________。
(6)常温下,在a mol/L的HCOOH溶液中加入等体积的bmol/L的NaOH溶液至溶液呈中性,此时溶液中HCOOH的物质的量浓度为______________________。