-
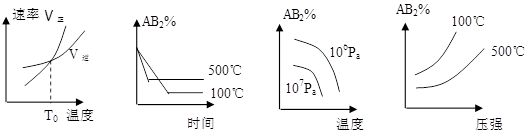
对于反应A2(g)+2B(g) 2AB2(g)(正反应为放热反应),下列各图所表示的变化符合勒夏特列原理的是
2AB2(g)(正反应为放热反应),下列各图所表示的变化符合勒夏特列原理的是
A. B. C. D.
-
对于反应A2(g)+2B2 (g)⇌2AB2(g)(正反应为放热反应),下列各图所表示的变化符合勒夏特列原理的是
A.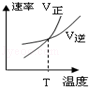 B.
B.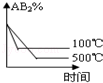 C.
C.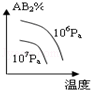 D.
D.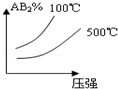
-
在1L密闭容器中,充入一定量的A发生反应:A(g)
 2B(g)(正反应为放热反应).当反应达到平衡后,改变影响平衡的一个条件,反应达到新的平衡.如图Ⅰ、Ⅱ两曲线分别表示整个反应过程中两种物质的浓度变化关系.下列说法正确的是( )
2B(g)(正反应为放热反应).当反应达到平衡后,改变影响平衡的一个条件,反应达到新的平衡.如图Ⅰ、Ⅱ两曲线分别表示整个反应过程中两种物质的浓度变化关系.下列说法正确的是( )
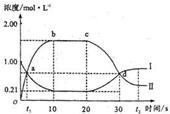
A.a点和d点分别表示两个不同的平衡状态
B.在a点,B的物质的量浓度为0.67mol/L
C.20s~t2s,表示降低温度使平衡移动的过程
D.0s~10s间,用B表示的反应速率为v(B)=1.58mol/
-
在1L密闭容器中,充入一定量的A发生反应:A(g)
 2B(g)(正反应为放热反应).当反应达到平衡后,改变影响平衡的一个条件,反应达到新的平衡.如图Ⅰ、Ⅱ两曲线分别表示整个反应过程中两种物质的浓度变化关系.下列说法正确的是( )
2B(g)(正反应为放热反应).当反应达到平衡后,改变影响平衡的一个条件,反应达到新的平衡.如图Ⅰ、Ⅱ两曲线分别表示整个反应过程中两种物质的浓度变化关系.下列说法正确的是( )
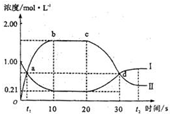
A.a点和d点分别表示两个不同的平衡状态
B.在a点,B的物质的量浓度为0.67mol/L
C.20s~t2s,表示降低温度使平衡移动的过程
D.0s~10s间,用B表示的反应速率为v(B)=1.58mol/
-
在1 L密闭容器中,充入一定量的A发生反应:A(g) 2B(g)(正反应为放热反应)。当反应达到平衡后,改变影响平衡的一个条件,反应达到新的平衡。下图Ⅰ、Ⅱ两曲线分别表示整个反应过程中两种物质的浓度变化关系。下列说法正确的是
2B(g)(正反应为放热反应)。当反应达到平衡后,改变影响平衡的一个条件,反应达到新的平衡。下图Ⅰ、Ⅱ两曲线分别表示整个反应过程中两种物质的浓度变化关系。下列说法正确的是
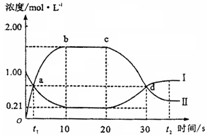
A.a点和d点分别表示两个不同的平衡状态
B.在a点,B的物质的量浓度为0.67 mol/L
C.20s~t2s,表示降低温度使平衡移动的过程
D.0s~10s间,用B表示的反应速率为 mol/(L·s)
mol/(L·s)
-
在1 L密闭容器中,充入一定量的A发生反应:A(g) 2B(g)(正反应为放热反应)。当反应达到平衡后,改变影响平衡的一个条件,反应达到新的平衡。右图Ⅰ、Ⅱ两曲线分别表示整个反应过程中两种物质的浓度变化关系。下列说法正确的是( )
2B(g)(正反应为放热反应)。当反应达到平衡后,改变影响平衡的一个条件,反应达到新的平衡。右图Ⅰ、Ⅱ两曲线分别表示整个反应过程中两种物质的浓度变化关系。下列说法正确的是( )
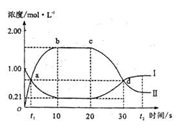
A.a点和d点分别表示两个不同的平衡状态
B.在a点,B的物质的量浓度为0.67 mol/L
C.20s~t2s,表示降低温度使平衡移动的过程
D.0s~10s间,用B表示的反应速率为 mol/(L·s)
mol/(L·s)
-
下列图象与文字描述正确的是( )
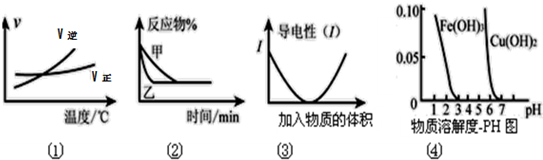
A.根据图①可判断对于“A2(g)+3B2(g)⇌2AB3(g)”:升温,化学反应平衡常数增大
B.图②表示压强对可逆反应2A(g)+2B(g)⇌3C(g)+D(s)的影响且P甲<P乙
C.图③可表示醋酸溶液中通入氨气至过量过程中溶液导电性的变化
D.根据图④,若除去CuSO4溶液中的Fe3+可采用向溶液中加入适量Cu(OH)2至溶液的pH在4左右即可
-
在体积不变的密闭容器中,在一定条件下发生下列反应:2A B(g)+C(s),达到平衡后,升高温度使容器内气体的密度增大,则下列叙述中正确的是( )
B(g)+C(s),达到平衡后,升高温度使容器内气体的密度增大,则下列叙述中正确的是( )
A. 若正反应为吸热反应,则A为非气体
B. 若正反应为放热反应,则A为非气体
C. 在平衡体系中加入少量的C,该平衡向逆反应方向移动
D. 改变压强对该平衡的移动无影响
-
化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题:
(1)一定温度下,在一个固定容积的密闭容器中,可逆反应 A(g)+2B(g)=4C (g)△H>0 达到平衡时,c(A)=2mol•L-1,c(B)=7mol•L-1,c(C)=4mol•L-1.试确定B的起始浓度c(B)的取值范围是______;若改变条件重新达到平衡后体系中C的质量分数增大,下列措施可行的是______.
A.增加C的物质的量 B.加压 C.升温 D.使用催化剂
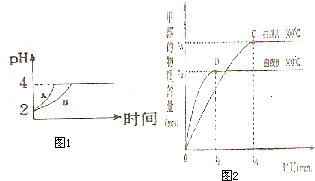
(2)常温下,取 pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图1所示.则图中表示醋酸溶液中pH变化曲线的是______ ( 填“A”或“B”). 设盐酸中加入的Zn质量为m1,醋酸溶液中加人的Zn质量为 m2. 则 m1______ m2 ( 选填“<”、“=”、“>”)
(3)在体积为3L的密闭容器中,CO与H2在一定条件下反应生成甲醇:CO(g)+2H2(g)→CH3OH(g).反应达到平衡时,平衡常数表达式K=______,升高温度,K值______(填“增大”、“减小”或“不变”).在500℃,从反应开始到平衡,氢气的平均反应速率v(H2)=______.
(4)难溶电解质在水溶液中存在着电离平衡.在常温下,溶液里各离子浓度以它们化学计量数为方次的乘积是一个常数,叫溶度积常数.例如:
Cu(OH)2(s)=Cu2+(aq)+2OH-(aq),Ksp=c(Cu2+)[c(OH-)]2=2×10-20
当溶液中各离子浓度方次的乘积大于溶度积时,则产生沉淀,反之固体溶解.若某CuSO4溶液里c( Cu2+)=0.02mol•L-1,如果生成Cu(OH)2沉淀,应调整溶液pH,使之大于______; 要使0.2mol•L-1的CuSO4 溶液中Cu2+沉淀较为完全 (使Cu2+浓度降至原来的千分之一)则应向溶液里加NaOH溶液,使溶液pH值为______.
(5)常温下,某纯碱(Na2CO3) 溶液中滴入酚酞,溶液呈红色.则该溶液呈______性.在分析该溶液遇酚酞呈红色原因时,甲同学认为是配制溶液所用的纯碱样品中混有NaOH 所致;乙同学认为是溶液中Na2CO3电离出的CO32-水解所致.请你设计一个简单的实验方案给甲和乙两位同学的说法以评判(包括操作、现象和结论)______.
-
合成氨工业对国民经济和社会发展具有重要的意义.对于密闭容器中的反应:N2(g)+3H2(g)
 2NH3(g)(正反应为放热反应),673K、30MPa下,n(NH3)和n(H2)随时间 t变化的关系如图所示.下列叙述中,正确的是( )
2NH3(g)(正反应为放热反应),673K、30MPa下,n(NH3)和n(H2)随时间 t变化的关系如图所示.下列叙述中,正确的是( )
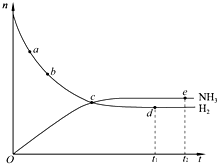
A.点c处正反应速率和逆反应速率相等
B.点a的正反应速率比点b的大
C.点d(t1时刻)和点e(t2时刻)处n(N2)不同
D.在t2时刻,正反应速率大于逆反应速率
2AB2(g)(正反应为放热反应),下列各图所表示的变化符合勒夏特列原理的是

2AB2(g)(正反应为放热反应),下列各图所表示的变化符合勒夏特列原理的是

2AB2(g)(正反应为放热反应),下列各图所表示的变化符合勒夏特列原理的是

 B.
B. C.
C. D.
D.


2B(g)(正反应为放热反应)。当反应达到平衡后,改变影响平衡的一个条件,反应达到新的平衡。下图Ⅰ、Ⅱ两曲线分别表示整个反应过程中两种物质的浓度变化关系。下列说法正确的是

mol/(L·s)
2B(g)(正反应为放热反应)。当反应达到平衡后,改变影响平衡的一个条件,反应达到新的平衡。右图Ⅰ、Ⅱ两曲线分别表示整个反应过程中两种物质的浓度变化关系。下列说法正确的是( )

mol/(L·s)

B(g)+C(s),达到平衡后,升高温度使容器内气体的密度增大,则下列叙述中正确的是( )

