-
(8分)我国对中药中重金属元素和有毒元素的含量等各项指标检查是非常严格的。下面是分析实验室对中草药中可能的残余有毒元素As的检验方法和步骤(As在中草药中主要以As2O3的形式存在):
① 取1000g中草药样品进行前期处理制得待测溶液,此时样品中可能含有的As元素将转化为H3AsO3;
② 将待测溶液转移到250mL锥形瓶中,并加入2-3滴0.2%的淀粉溶液;
③ 用0.001mol/L标准碘溶液滴定待测溶液至终点,消耗20.00mL标准I2溶液,发生的反应为:H3AsO3+ I2+ H2O→H3AsO4+ I-+ H+(未配平)
试回答下列问题:
(1)简述如何对中草药样品进行前期处理制得待测溶液? ________。
(2)配平离子反应方程式:__H3AsO3+__I2+__H2O— __H3AsO4+__I-+__H+
(3)如何判断滴定到达终点?________。
(4)我国《药用植物及制剂进出口绿色行业标准》中规定:绿色中药的砷含量不能超过
2.000mg/kg,试计算该草药样品中砷含量为________mg/kg,则该草药样品________(填
“合格”或“不合格”)。
高三化学填空题中等难度题查看答案及解析
-
我国中医药已有数千年历史,其独特的疗效使得经深加工的中药产品正逐步进入国际市场,但国外在进口中药时对中药的重金属元素和有毒元素的含量等各项指标检查是非常严格的,因此把好出口中药的质量关是非常重要的。以下介绍了分析实验室对中草药中可能的残余有毒元素As的检验方法和步骤(As在中草药中主要以As2O3的形式存在):
①取1000g中草药样品进行前期处理制得待测溶液,此时样品中可能含有的As元素将转化为H3AsO3;
②将待测溶液转移入250mL锥形瓶中,并加入2-3滴0.2%的淀粉溶液;
③用标准碘溶液滴定待测溶液至终点,消耗20.25mL标准I2溶液,其间发生反应:
H3AsO3+ I2+ H2O→H3AsO4+ I-+ H+(未配平)
试回答下列问题:
(1)简述如何对少量的中草药样品进行前期处理制得待测溶液?
。
(2)配平离子反应方程式:__H3AsO3+__I2+__H2O— __H3AsO4+__I-+__H+
(3)0.2%的淀粉溶液的作用是________,如何判断滴定到达终点?________。
(4)题中所用标准碘溶液并非将碘单质直接溶解于蒸馏水中制得,而是由0.1070g纯KIO3、过量的KI以及酸混合,并将其准确稀释到1000 mL而制得,请用一个离子反应方程式说明标准碘溶液的形成过程。
(5)我国《药用植物及制剂进出口绿色行业标准》中限定:绿色中药的砷含量不超过2.000mg/kg,试计算说明该中草药样品是否合格?(不需计算过程)计算可知该样品砷含量约为________mg/kg,故该草药样品(填“合格”或“不合格”)。
高三化学填空题中等难度题查看答案及解析
-
“砒霜”是我国古代一味重要的中药,其中含有一定量的砷元素,但同时它也具有剧毒.下列关于砷的说法不正确的是( )
A.水体的砷污染,会使水生生物体内砷含量超标,对人体造成危害
B.砷化氢的稳定性比溴化氢的弱,Mg3As2可以发生水解反应生成白色沉淀物质
C.砒霜可以用于癌症治疗,但服用过多可使人致命
D.砷、汞等都属重金属元素,对环境会造成污染高三化学选择题中等难度题查看答案及解析
-
【化学选修3:物质结构与性质】
元素周期表中第四周期的金属元素在生产和科研中有非常重要的使用价值。
(1)测定土壤中铁的含量时需先将三价铁还原为二价铁,再采用邻啡罗啉作显色剂,用比色法测定,若土壤中含有高氯酸盐时会对测定有干扰.相关的反应如下:
4FeCl3+2NH2OH•HCl→4FeCl2+N2O↑+6HCl+H2O
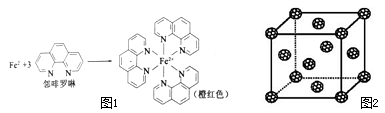
①Fe2+在基态时,核外电子排布式_________________________;
①羟胺中(NH2OH)采用SP3杂化的原子有___________________;
③Fe2+与邻啡罗啉形成的配合物中,配位数为__________;
(2)向硫酸铜溶液中加入过量氨水,然后加入适量乙醇,溶液中析出深蓝色的[Cu(NH3)4]SO4晶体,该晶体中含有的化学键类型是_______________;
(3)往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+,已知NF3与NH3的空间构型都是三角锥形,但NF3 不易与Cu2+形成配离子,其原因是___________________;
(4)配合物Ni(CO)4常温下呈液态,易溶于CCl4、苯等有机溶剂.固态Ni(CO)4属于______ _____晶体;
(5)如果把晶胞顶点与最近三个面心所围成的空隙叫做四面体空隙,第四周期电负性最小的原子可作为容体掺入C60 晶体的空隙中,形成具有良好的超导性的掺杂C60 化合物.现把C60抽象成质点,该晶体的晶胞结构如图2所示,若每个四面体空隙填入一个原子,则全部填满C60 晶体的四面体空隙后,所形成的掺杂C60 化合物的化学式为
高三化学填空题极难题查看答案及解析
-
最近,食品安全问题引起广泛关注。下列做法正确的是( )
A.用硫黄熏制白净的粉丝
B.用福尔马林保鲜海产品
C.用三聚氰胺作食品添加剂,以提高食品检测中的蛋白质含量指标
D.腌制食品中严格控制NaNO2的用量
高三化学选择题简单题查看答案及解析
-
重金属离子有毒性. 实验室有甲和乙两种废液, 均有一定的毒性, 经过化验甲废液呈碱性, 主要有毒离子为Ba2+, 如果将甲和乙两废液按照一定比例混合, 毒性明显降低, 乙废液中可能含有的离子是
A.Cu2+和SO42- B.Cu2+和Cl- C.K+和SO42- D.Ag+和NO3-
高三化学选择题中等难度题查看答案及解析
-
补铁剂中铁元素的含量是质检部门衡量其质量的重要指标,实验主要包括如下步骤:
①配制0.01mol•L-1、0.008mol•L-1等一系列浓度的[Fe(SCN)6]3-(红色)标准比色液
②样品处理
③准确量取一定体积的待测液于比色管中,加入稍过量的KSCN溶液,并稀释到10mL
④比色,直到与选取的标准颜色一致或相近即可.
试回答下列问题:
(1)配制25mL0.01mol•L-1标准溶液,需要的玻璃仪器有:烧杯、玻璃棒、量筒,还需要:________,若配制过程中定容时俯视刻度会使配制的浓度________(填偏大、偏小、不影响).
(2)步骤②脱色过程包括加入:________(填:脱有机色素的吸附剂名称)→搅拌煮沸→冷却→________(填操作).
(3)比色法确定待测液的浓度的原理是________
(4)已知有关离子的还原性顺序为I->Fe2+>SCN->Br->Cl-,则步骤②中Ⅲ可选择的氧化剂有________a.碘水 b.溴水 c.氯水 d.通入(SCN)2;写出加入上述某一氧化剂时涉及到的离子反应方程式:________
(5)若其补铁剂是由乳酸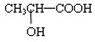 与铁粉作用生成的,请写出上述步骤②反应Ⅰ的化学方程式:________.
与铁粉作用生成的,请写出上述步骤②反应Ⅰ的化学方程式:________. 高三化学填空题中等难度题查看答案及解析
-
(8分)镁是海水中含量较多的金属元素,单质镁、镁合金以及镁的化合物在科学研究和工业生产中用途非常广泛.
(1)Mg2Ni是一种储氢合金,已知:
Mg(s)+H2(g)===MgH2(s) ΔH1== -74.5kJ/mol
Mg2Ni(s)+2H2(g)===Mg2NiH4(s) ΔH2== -64.4kJ/mol
Mg2Ni(s)+2MgH2(s)===2Mg(s)+Mg2NiH4(s) ΔH3
则ΔH3== kJ/mol
(2)工业上可用电解熔融的无水氯化镁获得镁.其中氯化镁晶体脱水是关键的工艺之一.一种正在试验的氯化镁晶体脱水的方法是:先将MgCl2•6H2O转化为MgCl2•NH4Cl•nNH3,然后在700℃脱氨得到无水氯化镁,脱氨反应的化学方程式为 ;用惰性电极电解熔融氯化镁,阴极的电极反应式为 。
(3)储氢材料Mg(AlH4)2在110℃﹣200℃的反应为:Mg(AlH4)2===MgH2+2Al+3H2↑,每生成27gAl转移电子的物质的量为 。
高三化学填空题中等难度题查看答案及解析
-
中药的煎制直接关系到其疗效。下列中草药煎制步骤中,属于过滤操作的是
A.冷水浸泡
B.加热煎制
C.箅渣取液
D.灌装保存




A. A B. B C. C D. D
高三化学选择题中等难度题查看答案及解析
-
补铁剂中铁元素的含量是质检部门衡量其质量的重要指标,实验主要包括如下步骤:
①配制0.01mol/L、0.008mol/L等一系列浓度的[Fe(SCN)6]3-(红色)标准比色液
②样品处理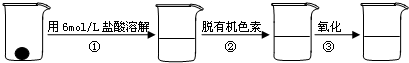
③准确量取一定体积的待测液于溶液中(比色管),加入稍过量的KSCN溶液,并稀释到10mL.
④比色,直到与选取的标准颜色一致或相近即可.
试回答下列问题:
①配制100mL0.01mol/L溶液,需要的玻璃仪器有:烧杯、玻璃棒、量筒,还需要:________、________.
②步骤②脱色过程包括加入:________(填:脱有机色素的吸附剂名称)→搅拌煮沸→冷却→________(填操作).
③比色法确定待测液的浓度其原理是________.
④若其补铁剂是由乳酸()与铁粉作用生成的,请写出该反应的化学方程式:________.
高三化学填空题中等难度题查看答案及解析