-
[化学一选修3:物质结构与性质](15分)
一水硫酸四氨合铜(II)(化学式为 是一种重要的染料及农药中间体。某学习小组以孔雀石(主要成分为Cu2(OH)2CO3,含少量Fe2O3和SO2杂质)为原料制备该物质的流程如下:
是一种重要的染料及农药中间体。某学习小组以孔雀石(主要成分为Cu2(OH)2CO3,含少量Fe2O3和SO2杂质)为原料制备该物质的流程如下:
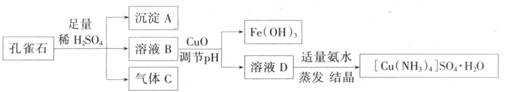
请回答:
(1) 沉淀A的晶体中最小环上的原子个数为______,气体C分子中 键和
键和 键的个数比为______
键的个数比为______
(2) 溶液D的溶质阴离子的空间构型为______,其中心原子的杂化轨道类型为______
(3) MgO的熔点高于CuO的原因为____________
(4) 画出一水硫酸四氨合铜(II)中配离子 的配位键____________。
的配位键____________。
(5)湿法炼铜就是利用溶液D制得铜单质,铜单质晶体中原子的堆积方式如图甲所示, 其晶胞如图乙所示,原子之间相互位置关系的平面图如图丙所示。
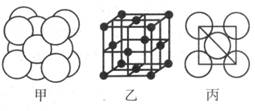
①铜单质晶体中原子的堆积方式为____________,晶胞中Cu原子的配位数为______
②若Cu原子半径为acm,则Cu单质晶体的密度为______g/cm3(只列出计算式,阿伏加德罗常数的值为NA)。
-
(15分)一水硫酸四氨合铜(Ⅱ)的化学式为[Cu(NH3)4]SO4·H2O是一种重要的染料及农药中间体。某学习小组在实验室以氧化铜为主要原料合成该物质,设计的合成路线为:
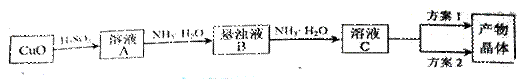
相关信息如下:
①[Cu(NH3)4]SO4·H2O在溶液中存在以下电离(解离)过程:
 [Cu(NH3)4]SO4·H2O=[Cu(NH3)4]2++
[Cu(NH3)4]SO4·H2O=[Cu(NH3)4]2++ +H2O
+H2O
[Cu(NH3)4]2+ Cu2++4NH3
②(NH4)2SO4在水中可溶,在乙醇中难溶。
③[Cu(NH3)4]SO4·H2O在乙醇·水混合溶剂中的溶解度随乙醇体积分数的变化曲线示意图如下:
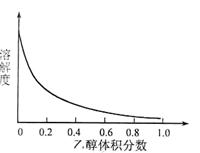
请根据以下信息回答下列问题: 图3
(1)方案1的实验步骤为:
a. 加热蒸发 b. 冷却结晶 c. 抽滤 d. 洗涤 e. 干燥
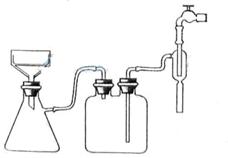
①步骤1的抽滤装置如图3所示,该装置中的错误之处是________;抽滤完毕或中途停止抽滤时,应先________,然后________。
②该方案存在明显缺陷,因为得到的产物晶体中往往含有________杂质,产生该杂质的原因是________。
(2)方案2的实验步骤为:
a. 向溶液C中加入适量________,b.________,c. 洗涤,d. 干燥
①请在上述内填写合适的试剂或操作名称。
②下列选项中,最适合作为步骤c的洗涤液是________。
A. 乙醇 B. 蒸馏水 C. 乙醇和水的混合液 D. 饱和硫酸钠溶液
③步骤d不宜采用加热干燥的方法,可能的原因是________。
-
一水硫酸四氨合铜(Ⅱ)的化学式为[Cu(NH3)4]SO4•H2O是一种重要的染料及农药中间体.某学习小组在实验室以氧化铜为主要原料合成该物质,设计的合成路线为:
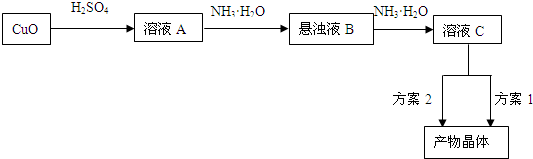
相关信息如下以下电离(解离)过程:
[Cu(NH3)4]SO4•H2O=[Cu(NH3)4]2++SO42-+H2O
[Cu(NH3)4]2+ Cu2++4NH3
Cu2++4NH3
②(NH4)2SO4在水中可溶,在乙醇中难溶.
③[Cu(NH3)4]SO4•H2O在乙醇•水混合溶剂中的溶解度随乙醇体积分数的变化曲线示意图如下: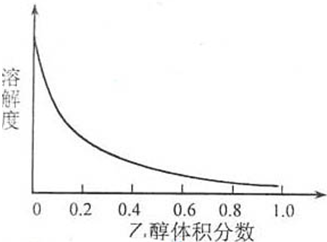
请根据以下信息回答下列问题:
(1)方案1的实验步骤为:
a.加热蒸发 b.冷却结晶 c.抽滤 d.洗涤 e.干燥
①步骤1的抽滤装置如下图所示,该装置中的错误之处是______;抽滤完毕或中途停止抽滤时,应先______,然后______.
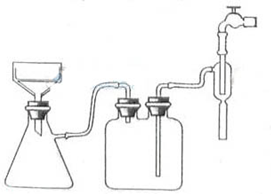
②该方案存在明显缺陷,因为得到的产物晶体中往往含有______杂质,产生该杂质的原因是______.
(2)方案2的实验步骤为:
a.向溶液C加入适量______b.______c.洗涤,d.干燥
①请在上述内填写合适的试剂或操作名称.
②下列选项中,最适合作为步骤c的洗涤液是______.
A.乙醇 B.蒸馏水 C.乙醇和水的混合液 D.饱和硫酸钠溶液
③步骤d不宜采用加热干燥的方法,可能的原因是______.
-
一水硫酸四氨合铜晶体[Cu(NH3)4SO4·H2O,相对分子质量为246]是一种重要的染料及农药中间体。常温下该物质可溶于水,难溶于乙醇。某化学兴趣小组通过以下实验制备一水硫酸四氨合铜晶体并测定其纯度。回答相关问题:
I.实验室制取CuSO4溶液
方案i:铜与浓硫酸加热制备。
方案ii:将铜粉在空气中充分加热至完全变黑,再加稀硫酸即可得到硫酸铜溶液。
(1)请写出方案i反应的化学方程式____,其缺点是____(写1点)。
(2)实际生产中方案ii常常有紫红色固体未反应,猜想原因可能是____。
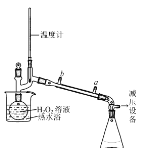
(3)基于此,实验进行了改进,其中一种方案是在硫酸和铜的反应容器中滴加H2O2溶液,观察到的现象是____(写1点)。H2O2的沸点为150.2℃。为加快反应需要提高H2O2溶液的浓度,可通过下图将H2O2稀溶液浓缩,冷水入口是____(填a或b),增加减压设备的目的是____。
II.一水硫酸四氨合铜晶体的制备
(4)硫酸铜溶液含有一定的硫酸,呈酸性,加入适量NH3·H2O调节溶液pH,产生浅蓝色沉淀,已知其成分为Cu2(OH)2SO4,试写出生成此沉淀的离子反应方程式__________。
(5)继续滴加NH3·H2O,会转化成深蓝色溶液。从深蓝色溶液中析出深蓝色晶体的简便实验是滴加____________。
III.产品纯度的测定
(6)精确称取mg晶体,加适量水溶解,然后逐滴加入足量NaOH溶液,通入水蒸气将氨全部蒸出,用V1mL0.200mol·L-1的盐酸完全吸收。以甲基橙作指示剂,用0.200mol·L-1NaOH标准溶液滴定过剩的HCl,到终点时消耗V2mLNaOH溶液。产品纯度的表达式为______。
-
一水硫酸四氨合铜晶体[Cu(NH3)4SO4·H2O,相对分子质量为246]是一种重要的染料及农药中间体。常温下该物质可溶于水,难溶于乙醇。某化学兴趣小组通过以下实验制备一水硫酸四氨合铜晶体并测定其纯度。回答相关问题:
I.实验室制取CuSO4溶液
方案i:铜与浓硫酸加热制备。
方案ii:将铜粉在空气中充分加热至完全变黑,再加稀硫酸即可得到硫酸铜溶液。
(1)请写出方案i反应的化学方程式________________________________________,此方法硫酸的利用率较低的原因是___________________________(写1点)。
(2)实际生产中方案ii常常有紫红色固体未反应,猜想原因可能是___________。
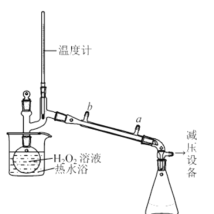
(3)某同学对实验ii进行了改进,其中一种方案是在硫酸和铜的反应容器中滴加H2O2溶液,观察到的现象是_____________________________________。H2O2的沸点为150.2℃。为加快反应需要提高H2O2溶液的浓度,可通过如图将H2O2稀溶液浓缩,增加减压设备的目的除了加快蒸馏速度,还有可能是________________________。
II.一水硫酸四氨合铜晶体的制备
(4)硫酸铜溶液含有一定的硫酸,呈酸性,加入适量NH3·H2O调节溶液pH,产生浅蓝色沉淀,已知其成分为Cu2(OH)2SO4,试写出生成此沉淀的离子反应方程式_______________________。
(5)继续滴加NH3·H2O,会转化成深蓝色溶液。向深蓝色溶液中加入乙醇可析出深蓝色晶体,滴加乙醇的作用可能是________________
A.乙醇可以作还原剂
B.乙醇可以降低该晶体在该溶液中的溶解度
C.乙醇可以作萃取剂
Ⅲ.产品纯度的测定
(6)精确称取mg晶体,加适量水溶解,然后逐滴加入足量NaOH溶液,通入水蒸气将氨全部蒸出,用V1mL0.200mol·L-1的盐酸完全吸收。以甲基橙作指示剂,用0.200mol·L-1NaOH标准溶液滴定过剩的HCl,到终点时消耗V2mLNaOH溶液。产品纯度的表达式为____________。
-
[化学一选修3:物质结构与性质](15分)
氮、磷、砷是同族元素,该族元素单质及其化合物在农药、化肥等方面有重要应用。回答下列问题:
(1)基态砷原子的电子排布式为 。
(2)K3[Fe(CN)6]晶体中Fe3+与CN一之间化学键类型为 键,与CN一互为等电子体的化合物分子式为 。
(3)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾污染,光化学烟雾中含有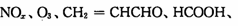
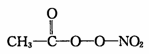 (PAN)等二次污染物。
(PAN)等二次污染物。
N2O结构式可表示为N=N=O,N2O中中心氮原子的杂化轨道类型为 ,1 mol PAN中含σ键数目为 。
测定大气中PM2.5的浓度方法之一是 一射线吸收法,
一射线吸收法, 一射线放射源可用85 Kr。Kr晶体为面心立方晶体,若晶体中与每个Kr原子相紧邻的Kr原子有m个,晶胞中含Kr原子为n个,则
一射线放射源可用85 Kr。Kr晶体为面心立方晶体,若晶体中与每个Kr原子相紧邻的Kr原子有m个,晶胞中含Kr原子为n个,则 = (填数字)。已知Kr晶体的密度为
= (填数字)。已知Kr晶体的密度为 g/cm3 ,摩尔质量为Mg/ mol,阿伏伽德罗常数用NA表示,列式表示Kr晶胞参数a= nm
g/cm3 ,摩尔质量为Mg/ mol,阿伏伽德罗常数用NA表示,列式表示Kr晶胞参数a= nm
-
一水硫酸四氨合铜(Ⅱ)([Cu(NH3)4]SO4·H2O)是一种重要的染料及农药中间体。请回答下列相关问题:
(1)Cu的核外电子排布式为 。
(2)N的L层中有 对成对电子;N 立体构型是 ,其中心原子的杂化方式为 。
立体构型是 ,其中心原子的杂化方式为 。
(3)氨水溶液中存在多种氢键,任表示出其中两种 ;
(4)[Cu(NH3)4]SO4·H2O中呈深蓝色的离子是 ,该微粒中的“电子对给予一接受键”属于 键;
(5)Cu的一种氯化物晶胞结构如图所示,该氯化物的化学式 。
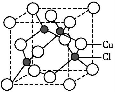
-
一水硫酸四氨合铜(Ⅱ)([Cu(NH3)4]SO4•H2O]是一种重要的染料及农药中间体.请回答下列相关问题:
(1)Cu的核外电子排布式为______.
(2)N的L层中有______对成对电子; 立体构型是______,其中心原子的杂化方式为______.
立体构型是______,其中心原子的杂化方式为______.
(3)氨水溶液中存在多种氢键,任表示出其中两种______;
(4)[Cu(NH3)4]SO4•H2O中呈深蓝色的离子是______,该微粒中的“电子对给予一接受键”属于______键(填“σ”或“π”);
(5)Cu的一种氯化物晶胞结构如图所示,该氯化物的化学式是______.
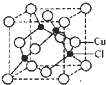
-
(15分)【化学——选修有机化学基础】呋喃酚是合成农药的重要中间体,其合成路线如下:
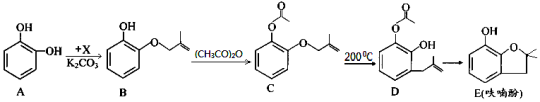
(1)A物质核磁共振氢谱共有 个峰,B→C的反应类型是 。
(2)已知X的分子式为C4H7C1,写出A→B的化学方程式: 。
(3)Y是X的同分异构体,分子中无支链且不含甲基,则Y的名称(系统命名)是 。
(4)下列有关化合物C、D的说法正确的是 。
①可用氯化铁溶液鉴别C和D ②C和D含有的官能团完全相同
③C和D互为同分异构体 ④C和D均能使溴水褪色
(5)E的同分异构体很多,写出两种符合下列条件的芳香族同分异构体的结构简
式: 、 。
①环上的一氯代物只有一种
②含有酯基
③能发生银镜反应
-
硫酸是一种重要的工业原料,广泛应用于炼油、冶金、染料等工业中。硫酸性质是中学化学学习的重点。
请回答下列问题:
(1)写出中学化学中利用物质与浓硫酸共热产生不同类别的两种气体的名称:___、___。
(2)浓硫酸脱水性实验教材中如下操作:取20g蔗糖置200mL烧杯中,加2mL水,搅拌均匀。再加入20mL98%的浓硫酸,迅速搅拌,静置。实验中,生产大量含SO2、CO2等混合气体。写出产生该混合气体的化学方程式:___。
(3)有学生改进了浓硫酸的脱水性实验(装置如图):
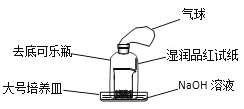
实验准备就绪后,加入浓硫酸,迅速搅拌后用去底可乐瓶罩上,观察现象。除看到烧杯中白色蔗糖颜色变深,体积膨胀,有气体产生外,还可看到哪些现象?___。
(4)图中,仪器a、b的名称分别是___、___;其中,仪器b常用于操作___(填一种物质提纯操作)。
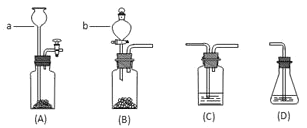
(5)有学生为了确定浓硫酸使蔗糖脱水过程中产生SO2、CO2气体,请选用上述装置(可重复使用)设计实验,将它们的编号填入方框,并将装置内所放的化学药品填入括号内___。
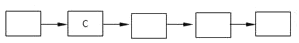
(浓硫酸,蔗糖)________________________。
是一种重要的染料及农药中间体。某学习小组以孔雀石(主要成分为Cu2(OH)2CO3,含少量Fe2O3和SO2杂质)为原料制备该物质的流程如下:

键和
键的个数比为______
的配位键____________。









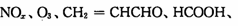
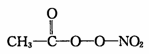 (PAN)等二次污染物。
(PAN)等二次污染物。




