-
向2L的密闭容器中充入7.6mol NO和3.8mol O2,发生如下反应:
①2NO(g)+O2 (g) 2NO2(g)
2NO2(g)
②2NO2(g) N2O4(g)
N2O4(g)
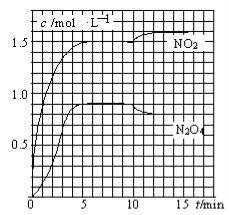
测得NO2和N2O4的浓度变化如图所示,0~10min维持容器温度为T1℃,10min后升高并维持容器的温度为T2℃。下列说法正确的是
A.前5min反应的平均速率v(N2O4)=0.18mol·(L·min)-1
B.T1℃时反应②的化学平衡常数K=0.6
C.反应①、②均为吸热反应
D.若起始时向该容器中充入3.6mol NO2和2.0mol N2O4,T1℃达到平衡时,N2O4的转化率为10%
-
向2L的密闭容器中充入7.6mol NO和3.8mol O2,发生如下反应:
①2NO(g)+O2(g) 2NO2(g)
2NO2(g)
②2NO2(g) N2O4(g)
N2O4(g)
测得NO2和N2O4的浓度变化如图所示,0~10min维持容器温度为T1℃,10min后升高并维持容器的温度为T2℃。下列说法正确的是
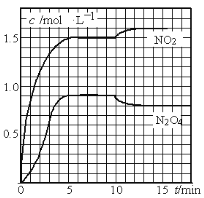
A. 前5min的平均反应速率v(N2O4)=0.18mol·L-1·s-1
B. T1℃时反应②的化学平衡常数K=0.6
C. 反应①、②均为吸热反应
D. 若起始时向该容器中充入3.6mol NO2和2.0mol N2O4,T1℃达到平衡时,N2O4的转化率为10%
-
向2L的密闭容器中充入7.6mol NO和3.8mol O2,发生如下反应:
①2NO(g)+O2(g) 2NO2(g)
2NO2(g)
②2NO2(g) N2O4(g)
N2O4(g)
测得NO2和N2O4的浓度变化如图所示,0~10min维持容器温度为T1℃,10min后升高并维持容器的温度为T2℃。
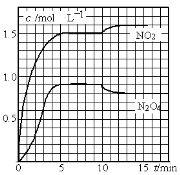
下列说法正确的是
A.前5min反应的平均速率v(N2O4)=0.18mol·L-1·s-1
B.T1℃时反应②的化学平衡常数K=0.6
C.反应①、②均为吸热反应
D.若起始时向该容器中充入3.6mol NO2和2. 0mol N2O4,T1℃达到平衡时,N2O4的转化率为10%
-
温度为T1时,在三个容积均为1L的恒容密闭容器中仅发生反应:2NO2(g) 2NO(g)+O2(g)相关数据如下表所示。下列说法错误的是( )
2NO(g)+O2(g)相关数据如下表所示。下列说法错误的是( )
| 容器 编号 | 物质的起始浓度 (mol·L-1) | 物质的平衡浓度 (mol·L-1) |
| c(NO2) | c(NO) | c(O2) | c(O2) |
| Ⅰ | 0.6 | 0 | 0 | 0.2 |
| Ⅱ | 0.3 | 0.5 | 0.2 | |
| Ⅲ | 0 | 0.5 | 0.35 | |
A.容器Ⅰ中发生反应的平衡常数为0.8 B.容器Ⅱ中发生反应的起始阶段有v正>v逆
C.达到平衡时,容器Ⅲ中 >1 D.达到平衡时,容器Ⅰ与容器Ⅲ中的总压强之比为16∶17
>1 D.达到平衡时,容器Ⅰ与容器Ⅲ中的总压强之比为16∶17
-
某温度下,三个容积均为2.0 L恒容密闭容器中发生反应2NO(g)+2CO(g) N2(g)+2CO2(g),各容器中起始物质的量浓度与反应温度如下表所示:
N2(g)+2CO2(g),各容器中起始物质的量浓度与反应温度如下表所示:
| 容器 | 温度/℃ | 起始物质的量浓度/(mol·L-1) |
| NO(g) | CO(g) | N2 | CO2 |
| 甲 | T1 | 0.10 | 0.10 | 0 | 0 |
| 乙 | T2 | 0 | 0 | 0.10 | 0.20 |
| 丙 | T2 | 0.10 | 0.10 | 0 | 0 |
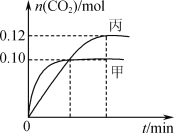
反应过程中甲、丙容器中CO2的物质的量随间变化关系如图所示。下列说法正确的是
A.该反应的正反应为放热反应,平衡常数K(T1)<K(T2)
B.达到平衡时,乙容器中的压强一定大于甲容器的2倍
C.乙容器中反应达到平衡时,N2的转化率大于40%
D.丙容器中反应达到平衡后,再充入0.10 mol NO和0.10 mol CO2,此时v(正)>v(逆)
-
(11分)某条件下,在2L密闭容器中发生如下反应:2NO2(g) 2NO(g)+O2(g) △H>0。在三种不同条件下进行,其中NO、O2的起始浓度都为0 mol/L,实验Ⅰ、Ⅱ反应温度相同,NO2的浓度(mol·L-1)随时间(min)的变化如图所示。请回答下列问题:
2NO(g)+O2(g) △H>0。在三种不同条件下进行,其中NO、O2的起始浓度都为0 mol/L,实验Ⅰ、Ⅱ反应温度相同,NO2的浓度(mol·L-1)随时间(min)的变化如图所示。请回答下列问题:
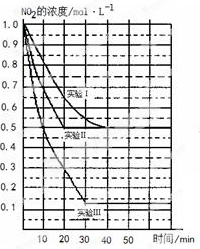
(1)请在图中标上对应的反应温度(800℃或850℃)。实验Ⅱ隐含的反应条件是_______________________。
(2)写出该反应的平衡常数表达式:K=______________。
(3)若实验Ⅰ中达平衡后,再向密闭容器中通入1mol NO2与1mol NO混合气体(保持温度不变),则平衡将 _________(填“正向移动”或“逆向移动”或“不移动”)
_________(填“正向移动”或“逆向移动”或“不移动”)(4)一定条件下NO2与SO2可发生反应,其方程式为:
NO2(g)+SO2(g) SO3(g)+NO(g) △H>0,将NO2与SO2以体积比
SO3(g)+NO(g) △H>0,将NO2与SO2以体积比 置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是________ ________。
置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是________ ________。
A、体系压强保持不变 B、混合气体颜色保持不变
C、SO3和NO的体积比保持不变 D、混合气体的平均相对分子质量保持不变
(5)若改变条件,使平衡常数变大,该反应________ ________。
A、一定向正反应方向移动 B、在平衡移动时,正反应速率先增大后减小
C、一定向逆反应方向移动 D、在平衡移动时,逆反应速率先增大后减小
-
(12分)某条件下,在2L密闭容器中发生如下反应:2NO2(g) 2NO(g)+O2(g) △H>0。在三种不同条件下进行,其中NO、O2的起始浓度都为0 mol/L,实验Ⅰ、Ⅱ反应温度相同,NO2的浓度(mol·L-1)随时间(min)的变化如图所示。
2NO(g)+O2(g) △H>0。在三种不同条件下进行,其中NO、O2的起始浓度都为0 mol/L,实验Ⅰ、Ⅱ反应温度相同,NO2的浓度(mol·L-1)随时间(min)的变化如图所示。
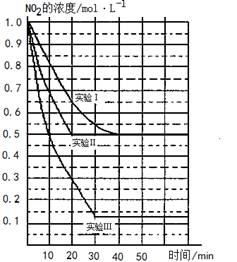
请回答下列问题:
(1)请在图中标上对应的反应温度(800℃或850℃)。实验Ⅱ隐含的反应条件是_______________________。
(2)写出该反应的平衡常数表达式:K=______________。
(3)若实验Ⅰ中达平衡后,再向密闭容器中通入1mol NO2与1mol NO混合气体(保持温度不变),则平衡将_________(填“正向移动”或“逆向移动”或“不移动”)
(4)一定条件下NO2与SO2可发生反应,其方程式为:
NO2(g)+SO2(g) SO3(g)+NO(g) △H>0,将NO2与SO2以体积比
SO3(g)+NO(g) △H>0,将NO2与SO2以体积比 置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是________ ________。
置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是________ ________。
A、体系压强保持不变 B、混合气体颜色保持不变
C、SO3和NO的体积比保持不变 D、混合气体的平均相对分子质量保持不变
(5)若改变条件,使平衡常数变大,该反应________ ________。
A、一定向正反应方向移动 B、在平衡移动时,正反应速率先增大后减小
C、一定向逆反应方向移动 D、在平衡移动时,逆反应速率先增大后减小
-
在800℃时,在2L密闭容器中将一定量的NO和O2混合发生反应2NO+O2⇌2NO2,n(NO)随时间的变化如下表:
| 时间/s | | 10 | 20 | 30 | 40 | 50 |
| n(NO)/mol | 0.2 | 0.1 | 0.08 | 0.07 | 0.07 | 0.07 |
请回答下列问题:
(1)用O2表示从0~20s内该反应的速率为________;达到平衡时NO的转化率为________.
(2)若升温到850℃,平衡后n(NO)=n(NO2),则该反应是________热反应(填:“吸”、“放”)
(3)下列能说明该反应已达到平衡的是________.
A.容器内压强不变 B.容器内气体密度不变
C.n(NO)=n(NO2) D.容器内气体颜色不变
E.容器内混合气体的平均分子量不变 F.v(NO2)=2v(O2)
(4)若改变某一条件,达新平衡时n(NO)=0.06mol,下列说法正确的是________.
A.平衡一定正向移动
B.可能是向容器中加入了一定量的NO气体
C.NO的转化率一定增大
D.可能是缩小了容器的体积
(5)假设在一定条件下0.2molNO气体与氧气反应,达到平衡时测得放出热量akJ,此时NO转化率为80%,写出在此条件下该反应的热化学方程式________.
-
一定温度下,向aL密闭容器中加入2mol NO2(g),发生如下反应:2NO2 2NO+O2,此反应达到平衡状态的标志是
A.混合气体的密度不再变化
B.混合气体的颜色变浅
C.混合气体中NO2、NO、O2的物质的量之比为2:2:1
D.单位时间内生成2n mol NO同时生成2n mol NO2
-
(15分)在100℃时,将0.40mol的二氧化氮气体充入2L抽空的密闭容器中,发生反应:
2NO2 N2O4。每隔一定时间就对该容器内的物质进行分析,得到如下表数据:
N2O4。每隔一定时间就对该容器内的物质进行分析,得到如下表数据:
| 时间/s | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
(1)在上述条件下,从反应开始直至20 s时,二氧化氮的平均反应速率为__________
mol/(L·s)。
(2)若在相同情况下最初向该容器充入的是四氧化二氮气体,要达到上述同样的平衡状态,四氧化二氮的起始浓度是_________mol/L。假设在80s时达到平衡,请在如图中画出该条
件下N2O4和NO2的浓度随时间变化的曲线。
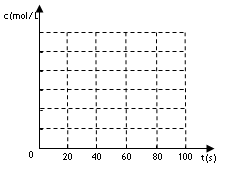
(3)上述(2)达到平衡后四氧化二氮的转化率为_________,混合气体的平均摩尔质量
为___________。
(4)达到平衡后,如向该密闭容器中再充入0.32molHe气,并把容器体积扩大为4L,则平衡将________(填“向左移动”、“向右移动”或“不移动”)。

2NO2(g)
N2O4(g)





