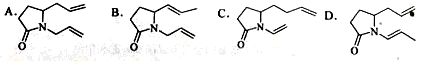-
中科院大连化学物理研究所的“煤基甲醇制取低碳烯烃技术(简称DMTO)”荣获2014年度国家技术发明一等奖。DMTO技术主要包括煤的气化、液化、烯烃化三个阶段,相关反应的热化学方程式如下:
(i)煤气化制合成气:C(s)+H2O(g) CO(g)+H2(g)
CO(g)+H2(g)
(ii)煤液化制甲醇:CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
(iii)甲醇制取低碳烯烃:2CH3OH(g) C2H4(g)+2H2O(g) ΔH= -11.72kJ·mol-1……(a)
C2H4(g)+2H2O(g) ΔH= -11.72kJ·mol-1……(a)
3CH3OH(g) C3H6(g)+3H2O(g) ΔH= -30.98kJ·mol-1……(b)
C3H6(g)+3H2O(g) ΔH= -30.98kJ·mol-1……(b)
回答下列问题:
(1)已知:C(s)+CO2(g)=2CO(g) ΔH= +172.5kJ·mol-1,
CO(g)+H2O(g)=CO2(g)+H2(g) ΔH= -41.0kJ·mol-1
反应(i)能自发进行的条件是 (填“高温”、“低温”或“任何温度”)。
(2)反应(ii)中以氢碳[n(H2)∶n(CO)]投料比为2制取甲醇,温度、压强与CO的平衡转化率关系如下图1。
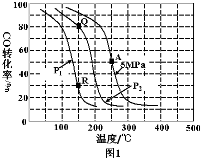
①对于气体参与的反应,表示平衡常数Kp时用气体组分(B)的平衡压强p(B)代替该气体物质的量浓度c(B),则A点时反应(ii)的Kp= (保留两位有效数字,分压=总压×物质的量分数)。
②比较P1 P2,Kp(Q) Kp(R)(填“大于”、“小于”或“等于”)。
③工业上常以铜基催化剂,压强5MPa,温度275℃下发生反应(ii),CO转化率可达到40%左右。为提高CO转化率除了可以适当改变反应温度和压强外,还可以采取的措施有 (写出2个)。
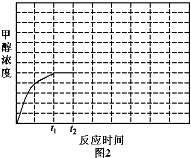
④若反应(ii)在恒容密闭容器内进行,T1温度下甲醇浓度随时间变化曲线如图2所示;不改变其他条件,假定t2时刻迅速降温到T2,t3时刻体系重新达到平衡。试在图中画出t2时刻后甲醇浓度随时间变化趋势图(在图中标出t3)。
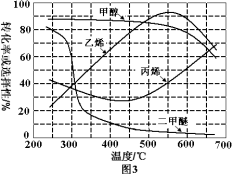
(3)烯烃化阶段:在常压和某催化剂作用下,甲醇的平衡转化率及乙烯、丙烯等物质的选择性(指除了水蒸气以外的产物中乙烯、丙烯等物质的物质的量分数)与反应温度之间的关系如图3。为尽可能多地获得乙烯,控制反应温度为550℃的理由是 。
-
(14分)在2014年国家科学技术奖励大会上,甲醇制取低碳烯烃技术(DMTO)获国家技术发明奖一等奖。DMTO主要包括煤的气化、液化、烯烃化三个阶段。
(1)煤的气化:用化学方程式表示出煤的气化的主要反应________________________:
(2)煤的液化:下表中有些反应是煤液化过程中的反应:

①a__________0(填“>”、“<”、“=”),c与a、b之间的定量关系为__________。
②K3=__________,若反应③是在容积为2 L的密闭容器巾进行(500℃)的,测得某一时刻体系内 物质的量分别为6 mol、2 mol、10 mol、10 mol,则此时CH3OH的生成速率(填“>”、“<”、“=”) CH3OH的消耗速率。
物质的量分别为6 mol、2 mol、10 mol、10 mol,则此时CH3OH的生成速率(填“>”、“<”、“=”) CH3OH的消耗速率。
(3)烯烃化阶段:如图l是某工厂烯烃化阶段产物中乙烯、丙烯的选择性与温度、压强之间的关系(选择性:指生成某物质的百分比,图中I、Ⅱ表示乙烯,Ⅲ表示丙烯)。

①为尽可能多地获得乙烯,控制的生产条件为__________。
②一定温度下某密闭容器中存在反应,  。在压强为P1时,产物水的物质的量与时间的关系如图2所示,若t0 时刻,测得甲醇的体积分数为10%,此时甲醇乙烯化的转化率为_________(保留三位有效数字),若在t1 时刻将容器容积快速扩大到原来的2倍,请在图中绘制出此变化发生后至反应达到新平衡时水的物质的量与时问的关系图。
。在压强为P1时,产物水的物质的量与时间的关系如图2所示,若t0 时刻,测得甲醇的体积分数为10%,此时甲醇乙烯化的转化率为_________(保留三位有效数字),若在t1 时刻将容器容积快速扩大到原来的2倍,请在图中绘制出此变化发生后至反应达到新平衡时水的物质的量与时问的关系图。
-
在2014年国家科学技术奖励大会上,甲醇制取低碳烯烃技术 获国家技术发明奖一等奖。DMTO主要包括煤的气化、液化、烯烃化三个阶段。
获国家技术发明奖一等奖。DMTO主要包括煤的气化、液化、烯烃化三个阶段。
(1)煤的气化:用化学方程式表示出煤的气化的主要反应 ______ :
(2)煤的液化:下表中有些反应是煤液化过程中的反应:
① ______
______  填“
填“ ”、“
”、“ ”、“
”、“ ”
” ,c与a、b之间的定量关系为 ______ 。
,c与a、b之间的定量关系为 ______ 。
② ______ ,若反应
______ ,若反应 是在容积为2L的密闭容器巾进行
是在容积为2L的密闭容器巾进行 的,测得某一时刻体系内
的,测得某一时刻体系内 、
、 、
、 、
、 物质的量分别为6mol、2mol、10mol、10mol,则此时
物质的量分别为6mol、2mol、10mol、10mol,则此时 的生成速率 ______
的生成速率 ______  填“
填“ ”、“
”、“ ”、“
”、“ ”
”
 的消耗速率。
的消耗速率。
(3)烯烃化阶段:如图l是某工厂烯烃化阶段产物中乙烯、丙烯的选择性与温度、压强之间的关系 选择性:指生成某物质的百分比,图中I、Ⅱ表示乙烯,Ⅲ表示丙烯
选择性:指生成某物质的百分比,图中I、Ⅱ表示乙烯,Ⅲ表示丙烯 。
。

①为尽可能多地获得乙烯,控制的生产条件为 ______ 。
②一定温度下某密闭容器中存在反应, 在压强为
在压强为 时,产物水的物质的量与时间的关系如图2所示,若
时,产物水的物质的量与时间的关系如图2所示,若 时刻,测得甲醇的体积分数为
时刻,测得甲醇的体积分数为 ,此时甲醇乙烯化的转化率为 ______
,此时甲醇乙烯化的转化率为 ______  保留三位有效数字
保留三位有效数字 ,若在
,若在 时刻将容器容积快速扩大到原来的2倍,请在图中绘制出此变化发生后至反应达到新平衡时水的物质的量与时问间关系图______________
时刻将容器容积快速扩大到原来的2倍,请在图中绘制出此变化发生后至反应达到新平衡时水的物质的量与时问间关系图______________
-
我国化学家在“铁基(氟掺杂镨氧铁砷化合物)高温超导”材料研究上取得了重要成果,该研究项目荣获2013年度“国家自然科学奖”一等奖。
(1)基态Fe2+的核外电子排布式为_________________。
(2)氟、氧、砷三种元素中电负性值由大到小的顺序是__________(用相应的元素符号填空)。
(3)Fe(SCN)3溶液中加人NH4F,发生如下反应:Fe(SCN)3+6NH4F=(NH4)3FeF6+3NH4SCN。
①(NH4)3FeF6存在的微粒间作用力除共价键外还有_________(选填序号,下同)。
a.配位键 b.氢键 c.金属键 d.离子键
②已知SCN一中各原子最外层均满足8电子稳定结构,则C原子的杂化方式为_____________,该原子团中 键与
键与 个数的比值为___________________。
个数的比值为___________________。
(4)FeCl3晶体易溶于水、乙醇,用酒精灯加热即可气化,而FeF3晶体熔点高于1000℃,试解释两种化合物熔点差异较大的原因:_______________________________。
(5)氮、磷、砷虽为同主族元素,但其化合物的结构与性质是多样化的。
①该族氢化物RH3(NH3、PH3、AsH3)的某种性质随R的核电荷数的变化趋势如右图所示,则Y轴可表示的氢化物(RH3)性质可能有________。
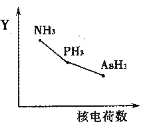
a.稳定性 b.沸点 c.R—H键能 d.分子间作用力
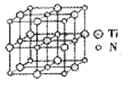
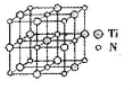
②碳氮化钛化合物在汽车制造和航空航天等领域有广泛的应用,其结构是用碳原子取代氮化钛晶胞(结构如图)顶点的氮原子,据此分析,这种碳氮化钛化台物的化学式为______。
-
我国化学家在“铁基(氟掺杂镨氧铁砷化合物)高温超导”材料研究上取得了重要成果,该研究项目荣获2013年度“国家自然科学奖”一等奖。
(1)基态Fe2+的核外电子排布式为_________________。
(2)氟、氧、砷三种元素中电负性值由大到小的顺序是__________(用相应的元素符号填空)。
(3)Fe(SCN)3溶液中加人NH4F,发生如下反应:Fe(SCN)3+6NH4F=(NH4)3FeF6+3NH4SCN。
①(NH4)3FeF6存在的微粒间作用力除共价键外还有_________(选填序号,下同)。
a.配位键 b.氢键 c.金属键 d.离子键
②已知SCN一中各原子最外层均满足8电子稳定结构,则C原子的杂化方式为_____________,该原子团中 键与
键与 个数的比值为___________________。
个数的比值为___________________。
(4)FeCl3晶体易溶于水、乙醇,用酒精灯加热即可气化,而FeF3晶体熔点高于1000℃,试解释两种化合物熔点差异较大的原因:_______________________________。
(5)氮、磷、砷虽为同主族元素,但其化合物的结构与性质是多样化的。
①该族氢化物RH3(NH3、PH3、AsH3)的某种性质随R的核电荷数的变化趋势如右图所示,则Y轴可表示的氢化物(RH3)性质可能有________。

a.稳定性 b.沸点 c.R—H键能 d.分子间作用力
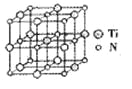
②碳氮化钛化合物在汽车制造和航空航天等领域有广泛的应用,其结构是用碳原子取代氮化钛晶胞(结构如图)顶点的氮原子,据此分析,这种碳氮化钛化台物的化学式为______。
-
我国化学家在“铁基(氟掺杂镨氧铁砷化合物)高温超导”材料研究上取得了重要成果,该研究项目荣获2013年度“国家自然科学奖”一等奖。
(1)基态Fe2+的核外电子排布式为_________________。
(2)氟、氧、砷三种元素中电负性值由大到小的顺序是__________(用相应的元素符号填空)。
(3)Fe(SCN)3溶液中加人NH4F,发生如下反应:Fe(SCN)3+6NH4F=(NH4)3FeF6+3NH4SCN。
①(NH4)3FeF6存在的微粒间作用力除共价键外还有_________(选填序号,下同)。
a.配位键 b.氢键 c.金属键 d.离子键
②已知SCN一中各原子最外层均满足8电子稳定结构,则C原子的杂化方式为_____________,该原子团中 键与
键与 个数的比值为___________________。
个数的比值为___________________。
(4)FeCl3晶体易溶于水、乙醇,用酒精灯加热即可气化,而FeF3晶体熔点高于1000oC,试解释两种化合物熔点差异较大的原因:_______________________________。
(5)氮、磷、砷虽为同主族元素,但其化合物的结构与性质是多样化的。
①该族氢化物RH3(NH3、PH3、AsH3)的某种性质随R的核电荷数的变化趋势如右图所示,则Y轴可表示的氢化物(RH3)性质可能有________。
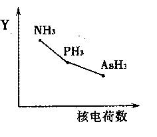
a.稳定性 b.沸点 c.R—H键能 d.分子间作用力
②碳氮化钛化合物在汽车制造和航空航天等领域有广泛的应用,其结构是用碳原子取代氮化钛晶胞(结构如图)顶点的氮原子,据此分析,这种碳氮化钛化台物的化学式为______。
-
CO2的资源化利用一直是化学家们关注的重要课题,中科院大连化学物理研究所设计了一种新型多功能复合催化剂,成功地实现了CO2直接加氢制取高辛烷值汽油: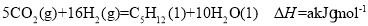 (反应①),该研究成果被评价为“CO2催化转化领域的突破性进展”。
(反应①),该研究成果被评价为“CO2催化转化领域的突破性进展”。
(1)已知氢气的燃烧热为 ,若要利用
,若要利用 的燃烧热求a的值,则还需要知道一个反应的
的燃烧热求a的值,则还需要知道一个反应的 ,该反应是________________________________。反应①在一定条件下具有自发性,则a_______________0(填“>”或“<”)。
,该反应是________________________________。反应①在一定条件下具有自发性,则a_______________0(填“>”或“<”)。
(2)向某密闭容器中按一定投料比充入 、
、 ,控制条件使其发生反应:
,控制条件使其发生反应: 。测得
。测得 的平衡转化率与温度、压强之间的关系如图1所示:
的平衡转化率与温度、压强之间的关系如图1所示:
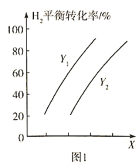
则X表示______________, ___________
___________ (填“>”或“<”)。欲提高
(填“>”或“<”)。欲提高 的平衡转化率并提高单位时间内
的平衡转化率并提高单位时间内 的产量,可采取的措施是______________________(填两种)。
的产量,可采取的措施是______________________(填两种)。
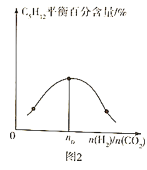
(3)控制一定温度、催化剂,按不同投料比 将反应物通入到某密闭容器中,测得平衡时
将反应物通入到某密闭容器中,测得平衡时 的百分含量与投料比之间的关系如图2所示,则
的百分含量与投料比之间的关系如图2所示,则 ____________。
____________。
(4)在钌-铑双金属催化剂的作用下,CH3OH、CO2、H2可高效地转化为乙酸,反应方程式为 。一定温度下,向某刚性容器中通入等物质的量的三种原料气,测得体系中的总压强与时间的关系如下表所示:
。一定温度下,向某刚性容器中通入等物质的量的三种原料气,测得体系中的总压强与时间的关系如下表所示:
| t/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| p/kPa | 3 | 2.7 | 2.5 | 2.35 | 2.26 | 2.2 | 2.2 |
则反应开始到达到平衡的过程中, ______________
______________ ______________
______________ 。
。
(5)碳捕捉技术的发展也有利于CO2在资源应用方面得到充分利用。常温下,若某次用NaOH溶液捕捉空气中的CO2所得溶液的pH=10,并测得溶液中 ,则
,则 _____________
_____________ 。
。
-
中科院大连化学物理研究所设计了一种新型Na-Fe3O4/HZSM-5多功能复合催化剂,成功实现了CO2直接加氢制取高辛烷值汽油,该研究成果被评价为“CO2催化转化领域的突破性进展”。
(1)已知:2H2(g)+O2(g)=2H2O(l) ΔH=-571.6kJ·mol-1
C8H18(l)+ O2(g)=8CO2(g)+9H2O(l) ΔH=-5518kJ·mol-1
O2(g)=8CO2(g)+9H2O(l) ΔH=-5518kJ·mol-1
则8CO2(g)+25H2(g)=C8H18(l)+16H2O(l) ΔH=___kJ·mol-1。
(2)氨硼烷(NH3BH3)是储氢量最高的材料之一,氨硼烷还可作燃料电池,其工作原理如图1所示。氨硼烷电池工作时正极的电极反应式为__________。
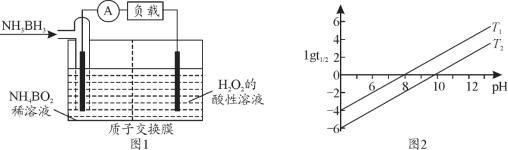
(3)常见含硼的化合物有NaBH4、NaBO2,已知NaBH4溶于水生成NaBO2、H2,写出其化学方程式_______。 为NaBH4反应的半衰期(反应一半所需要的时间,单位为min)。lgt1/2随pH和温度的变化如图2所示,则T1______T2(填“>”或“<”)。
为NaBH4反应的半衰期(反应一半所需要的时间,单位为min)。lgt1/2随pH和温度的变化如图2所示,则T1______T2(填“>”或“<”)。
(4)燃油汽车尾气含有大量的NO,在活化后的V2O5催化作用下,氨气将NO还原成N2的一种反应历程如图3所示。
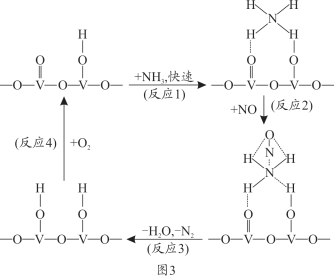
根据图写出总反应的化学方程式_______________。
-
中科院大连化学物理研究所设计了一种新型Na-Fe3O4/HZSM-5多功能复合催化剂,成功实现了CO2直接加氢制取高辛烷值汽油,该研究成果被评价为“CO2催化转化领域的突破性进展”。
(1)已知:2H2(g)+O2(g)=2H2O(l) ΔH=-571.6kJ·mol-1
C8H18(l)+ O2(g)=8CO2(g)+9H2O(l) ΔH=-5518kJ·mol-1
O2(g)=8CO2(g)+9H2O(l) ΔH=-5518kJ·mol-1
则8CO2(g)+25H2(g)=C8H18(l)+16H2O(l) ΔH=___kJ·mol-1。
(2)氨硼烷(NH3BH3)是储氢量最高的材料之一,氨硼烷还可作燃料电池,其工作原理如图1所示。氨硼烷电池工作时正极的电极反应式为__________。

(3)常见含硼的化合物有NaBH4、NaBO2,已知NaBH4溶于水生成NaBO2、H2,写出其化学方程式_______。 为NaBH4反应的半衰期(反应一半所需要的时间,单位为min)。lgt1/2随pH和温度的变化如图2所示,则T1______T2(填“>”或“<”)。
为NaBH4反应的半衰期(反应一半所需要的时间,单位为min)。lgt1/2随pH和温度的变化如图2所示,则T1______T2(填“>”或“<”)。
(4)燃油汽车尾气含有大量的NO,在活化后的V2O5催化作用下,氨气将NO还原成N2的一种反应历程如图3所示。
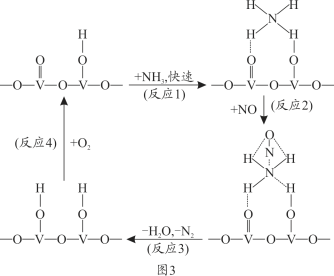
根据图写出总反应的化学方程式_______________。
-
三位科学家因在烯烃复分解反应研究中的杰出贡献而荣获2005年度诺贝尔化学奖,烯烃复分解反应可示意如下:
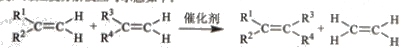
下列化合物中,经过烯烃复分解反应可以生成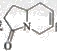 的是
的是
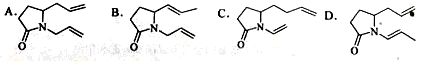
CO(g)+H2(g)
CH3OH(g)
C2H4(g)+2H2O(g) ΔH= -11.72kJ·mol-1……(a)
C3H6(g)+3H2O(g) ΔH= -30.98kJ·mol-1……(b)




 物质的量分别为6 mol、2 mol、10 mol、10 mol,则此时CH3OH的生成速率(填“>”、“<”、“=”) CH3OH的消耗速率。
物质的量分别为6 mol、2 mol、10 mol、10 mol,则此时CH3OH的生成速率(填“>”、“<”、“=”) CH3OH的消耗速率。
 。在压强为P1时,产物水的物质的量与时间的关系如图2所示,若t0 时刻,测得甲醇的体积分数为10%,此时甲醇乙烯化的转化率为_________(保留三位有效数字),若在t1 时刻将容器容积快速扩大到原来的2倍,请在图中绘制出此变化发生后至反应达到新平衡时水的物质的量与时问的关系图。
。在压强为P1时,产物水的物质的量与时间的关系如图2所示,若t0 时刻,测得甲醇的体积分数为10%,此时甲醇乙烯化的转化率为_________(保留三位有效数字),若在t1 时刻将容器容积快速扩大到原来的2倍,请在图中绘制出此变化发生后至反应达到新平衡时水的物质的量与时问的关系图。







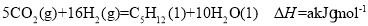 (反应①),该研究成果被评价为“CO2催化转化领域的突破性进展”。
(反应①),该研究成果被评价为“CO2催化转化领域的突破性进展”。





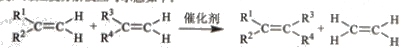
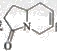 的是
的是