-
联氨(N2H4)是一种无色的可燃液体。请回答下列问题:
(1)联氨是火箭的重要燃料。已知:
(a) N2H4(l)的燃烧热ΔH1 = –624.0 kJ·mol–1
(b)  ΔH2 = –66.4 kJ·mol–1
ΔH2 = –66.4 kJ·mol–1
(c)  ΔH3 = –28.6 kJ·mol–1
ΔH3 = –28.6 kJ·mol–1
写出N2H4(l)在N2O4(g)中燃烧生成氮气和液态水的热化学方程式________________。
(2)N2H4能使锅炉内壁的铁锈(主要成分为Fe2O3·xH2O)变成磁性氧化铁,从而可减缓锅炉锈蚀。反应过程中每生成0.1 mol磁性氧化铁,转移的电子数为_________________。
(3)联氨-空气燃料电池的电解质为KOH溶液。写出该电池放电时负极的反应式________。
(4)联氨的制备方法有多种,尿素法是其中之一。在KMnO4的催化作用下,尿素CO(NH2)2和NaClO、NaOH溶液反应生成联氨、水和两种钠盐,写出该反应的化学方程式_________________。
-
(6分)联氨(N2H4)是一种无色可燃的弱碱性液体,是液体大推力火箭常用的高能燃料。
⑴已知联分子中的N原子最外层满足8电子相对稳定结构,则下列说法正确的是
A.联氨(N2H4)结构与C2H4相似,存在N=N双键
B.一分子联氨中含有的电子对数目为5
C.联氨中的N原子的杂化类型为sp3杂化
D.联氨能与HCl发生化合反应生成N2H6Cl2
⑵联氨可以采用尿素[CO(NH2)2]为原料制取,方法是在高锰酸钾催化剂存在下,尿素和次氯酸钠、氢氧化钠溶液反应生成联氨、另外两种正盐和水,写出其反应的化学方程式________;
⑶火箭推进器中分别装有联氨和过氧化氢,当它们混合时即产生气体,并放出大量热。 已知:12.8 g液态联氨与足量过氧化氢反应生成氮气和水蒸气,放出256.65 kJ的热量,写出该反应的热化学方程式 。
-
(16分)(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料.已知在100 kPa时,32.0 g N2H4在氧气中完全燃烧生成氮气,放出热量624 kJ(25℃),N2H4完全燃烧的热化学方程式是______________.
(2)肼—空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液.肼—空气燃料电池放电时,正极的电极反应式是________________.负极的电极反应式是________________.
(3)下图是一个电化学过程示意图.

①锌片上发生的电极反应式是_______________.
②假设使用肼—空气燃料电池作为本过程中的电源,铜片的质量变化128 g,则肼—空气燃料电池理论上消耗标准状况下的空气________ L(假设空气中氧气体积含量为20%).
(4)传统制备肼的方法,是用NaClO氧化NH3制得肼的稀溶液.该反应的离子方程式是_____________.
-
Ⅰ.肼(N2H4)又称联氨,常温时是一种可燃性液体,可用作火箭燃料。
(1)已知在25℃、101kPa时,16g N2H4在氧气中完全燃烧生成氮气,放出312kJ的热量,则N2H4完全燃烧的热化学方程式是_______________。
Ⅱ.如图所示,某研究性学习小组利用上述燃烧原理设计一个肼(N2H4)—空气燃料电池(如图甲)并探究某些工业原理,其中乙装置中X为阳离子交换膜(即只允许阳离子通过)。
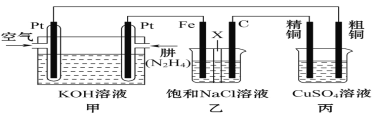
根据要求回答相关问题:
(2)甲装置中通入_________气体的一极为正极,负极的电极反应式为__________。
(3)乙装置中石墨电极为______极,其电极反应式为___________;可以用______________检验该反应产物,电解一段时间后,乙池中的溶液呈__________性。
(4)图中用丙装置模拟工业中的_____________________原理,如果电解后丙装置精铜质量增加3.2g,则理论上甲装置中肼消耗质量为____________g。
(5)如果将丙中的粗铜电极换为Pt电极,则丙中总化学方程式为_______________。
-
肼(N2H4)又称联氨,是一种可燃性液体,可用作火箭燃料。
(1)已知在101 kPa时,32.0 g N2H4在氧气中完全燃烧生成氮气和水,放出热量624 kJ(25 ℃时),N2H4完全燃烧的热化学方程式是__________________________________。
(2)肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼-空气燃料电池放电时,正极的反应式是___________________________;负极的反应式是____________________________。
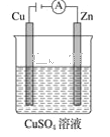
(3)下图是一个电化学过程示意图。
①锌片上发生的电极反应式是_________________________________________________。
②假设使用肼-空气燃料电池作为本过程中的电源,铜片的质量变化为128 g,则肼-空气燃料电池理论上消耗标准状况下的空气______L(假设空气中氧气体积分数为20%)。
(4)有同学想把Ba(OH)2·8H2O晶体与NH4Cl晶体的反应设计成原电池,你认为是否可行?________(填“是”或“否”)
-
(15分)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。
(1)已知在25℃,101kPa时,16.0g N2H4在氧气中完全燃烧生成氮气,放出热量312kJ,N2H4完全燃烧反应的热化学方程式是 ________。
肼—空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼—空气燃料电池放电时,负极的电极反应式是:________。电池工作一段时间后,电解质溶液的pH将(填“增大”、“减小”、“不变”)。
(2)右图是一个电化学装置示意图。用肼——空气燃料电池做此装置的电源。如果A是铂电极,B是石墨电极,C是500mL足量的饱和氯化钠溶液,当两极共产生1.12L气体时,溶液的pH为 ,
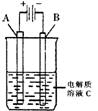
则肼-空气燃料电池理论上消耗的空气L(气体体积在标准状况下测定,假设空气中氧气体积分数为20%)
(3)肼易溶于水,它是与氨类似的弱碱,用电离方程式表示肼的水溶液显碱性的原因________。
(4)常温下将0.2mol/L HCl溶液与0.2mol/L N2H4·H2O溶液等体积混合(忽略混合后溶液体积的变化),若测得混合溶液的pH=6,则混合溶液中由水电离出的c(H+)________0.1
mol/L HCl溶液中由水电离出的c(H+)(填“大于”、“小于”、或“等于”)。
(5)已知:在相同条件下N2H4·H2O的电离程度大于N2H5C1的水解程度。常温下,若将0.2
mol/L N2H4·H2O溶液与0.1mol/L HCl溶液等体积混合,则溶液中N2H+5、Cl-、OH-、H+
离子浓度由大到小的顺序为。
-
(10分)(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在101kPa时,16.0gN2H4在氧气中完全燃烧生成氮气,放出热量312kJ(25℃时),写出表示N2H4燃烧热的热化学方程式________ 。
(2)甲烷----氧气燃料电池以20%~30%的KOH溶液为电解质溶液。
正极的电极反应式是。
负极的电极反应式是________ 。
(3)右图是一个电化学过程示意图。
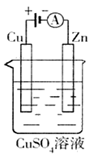
①锌片上发生的电极反应是________ 。
②假设使用肼—空气燃料电池作为本过程中的电源,铜片的质量变化128g,则肼一空气燃料电池理论上消耗标标准状况下的空气________ L(假设空气中氧气体积含量为20%)
-
(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在101kPa时,32.0g N2H4在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),N2H4完全燃烧反应的热化学方程式是__________________________________。
(2)肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼-空气燃料电池放电时:正极的电极反应式是_______________________;负极的电极反应式是___________________________;总反应方程式是______________。
(3)传统制备肼的方法,是以NaClO氧化NH3,制得肼的稀溶液。该反应的离子方程式是____。
-
(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在101kPa时,32.0g N2H4 在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),N2H4完全燃烧反应的热化学方程式是__________________________________。
(2)肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20% ~30%的KOH溶液。肼-空气燃料电池放电时:
正极的电极反应式是__________________________________________;
负极的电极反应式是__________________________________________;
(3)传统制备肼的方法,是以NaClO氧化NH3,制得肼的稀溶液。该反应的离子方程式为_____________________________________________________________________
-
(8分)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在25℃,101kPa时,32.0gN2H4在氧气中完全燃烧生成氮气,放出热量624kJ
(1)写出该状态下N2H4完全燃烧反应的热化学方程式
________ 。
(2)肼—空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼—空气燃料电池放电时:正极的电极反应式是
________ 。
( 3)下图是一个电化学过程示意图。
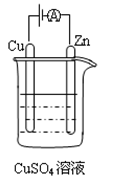
① 锌片上发生的电极反应式是________。
② 假设使用肼—空气燃料电池作为本过程中的电源,铜片的质量变化128g,则肼一空气燃料电池理论上需要标准状况下的空气
________ L(假设空气中氧气体积含量为20%)
ΔH2 = –66.4 kJ·mol–1
ΔH3 = –28.6 kJ·mol–1




