-
下表是NaCl和CsCl的熔沸点的比较。
NaCl
CsCl
熔点
801 ℃
645 ℃
沸点
1 413 ℃
1 290 ℃
(1)同为离子晶体,为什么NaCl的熔沸点比CsCl的高?请从影响离子键强弱的因素入手进行分析。
(2)实验证明,干燥的NaCl晶体不导电,熔融的NaCl或NaCl溶液却可以导电,你能说明其中的原因吗?
高三化学简答题中等难度题查看答案及解析
-
下表给出几种氯化物的熔点和沸点(*表示在2.5×1.01×105 Pa下测定):
NaCl
MgCl2
AlCl3
SiCl4
熔点(℃)
801
714
190*
―68
沸点(℃)
1465
1418
180
57
下列有关叙述,不正确的是
A.AlCl3在加热时升华
B.SiCl4晶体属于分子晶体
C.1500℃时NaCl存在气态分子
D.AlCl3晶体是典型的离子晶体
高三化学选择题简单题查看答案及解析
-
下表给出几种氯化物的熔点和沸点(*表示在2.5×1.01×105 Pa下测定):
NaCl
MgCl2
AlCl3
SiCl4
熔点(℃)
801
714
190*
―68
沸点(℃)
1465
1418
180
57
下列有关叙述,不正确的是
A.AlCl3在加热时升华 B.SiCl4晶体属于分子晶体
C.1500℃时NaCl存在气态分子 D.AlCl3晶体是典型的离子晶体
高三化学选择题简单题查看答案及解析
-
下列有关离子晶体的数据大小比较不正确的是( )
A. 熔点:NaF>MgF2>AlF3
B. 晶格能:NaF>NaCl>NaBr
C. 阴离子的配位数:CsCl>NaCl>CaF2
D. 硬度:MgO>CaO>BaO
高三化学选择题中等难度题查看答案及解析
-
下列数据是对应物质的熔点:
物质
Na2O
NaCl
AIF3
A1C13
BCl3
A12O3
CO2
SiO2
熔点
920
801
1291
190
-107
2073
-57
1723
由以上数据做出的下列判断,其中错误的是
A.铝的化合物的晶体中有的是离子晶体
B.表中只有BCl3和干冰是分子晶体
C.同族元素的氧化物可形成不同类型的晶体
D.不同族元素的氧化物可形成相同类型的晶体
高三化学选择题简单题查看答案及解析
-
下表数据是对应物质的熔点:
编号
①
②
③
④
⑤
⑥
⑦
⑧
物质
Na2O
NaCl
AlF3
AlCl3
BCl3
Al2O3
CO2
SiO2
熔点℃
920
801
1291
160
-107
2072
-57
1723
(1)上述涉及原子中最活泼非金属原子核外电子排布式是________________;某阴离子的轨道表示式为
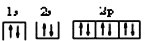 ,其核外电子占有的轨道总数是_____个,有______种能量不同的电子,有_____种不同运动状态的电子。
,其核外电子占有的轨道总数是_____个,有______种能量不同的电子,有_____种不同运动状态的电子。(2)物质①的电子式:____________,⑦的结构式:_______________。
(3)④溶于水溶液呈酸性,用离子方程式表示其原因_______________________________;若把其溶液加热蒸干并灼烧,得到的固体是_______________。
(4)不能用于比较Na与Al金属性相对强弱的事实是_________________。
A.最高价氧化物对应水化物的碱性 B.Na最外层1个电子而Al 最外层3个电子
C.单质与H2O反应的难易程度 D.比较同浓度NaCl和AlCl3的pH值
(5)⑧比⑦熔点高出很多,其理由是:_____________________________;①和②都属于离子晶体,但①比②的熔点高,请解释原因____________________________。
高三化学综合题中等难度题查看答案及解析
-
现有几种物质的熔点数据如下表:
A组 B组 C组 D组
金刚石:3550 ℃ Li:181 ℃ HF:-83 ℃ NaCl:801 ℃
硅晶体:1410 ℃ Na:98 ℃ HCl:-115 ℃ KCl:776 ℃
硼晶体:2300 ℃ K:64 ℃ HBr:-89 ℃ RbCl:718 ℃
二氧化硅1723 ℃ Rb:39 ℃ Hi:-51 ℃ CsCl:645 ℃
据此完成下列问题:
(1)A组属于__________晶体,其熔化时克服的粒子间的作用力是__________。
(2)B组晶体共同的物理性质是__________(填序号)。
①有金属光泽 ②导电性 ③导热性 ④延展性
(3)C组中HF熔点反常是由于____________________。
(4)D组晶体可能具有的性质是__________(填序号)。
①硬度小 ②水溶液能导电 ③固体能导电 ④熔融状态能导电
(5)XY晶体的单元结构如下图所示,晶体中距离最近的X+与Y-的核间距离为a cm,已知阿伏加德罗常数为Na mol-1,其密度为ρ g·cm-3,则XY的摩尔质量可表示为 __________
g·mol-1。

高三化学填空题中等难度题查看答案及解析
-
下列各晶体熔沸点高低的比较,正确的是( )
A.硅>金刚石>石英砂
B.CsCl>KCl>NaCl
C.SiO2>CO2>Hg
D.H2O>NH3>H2高三化学选择题中等难度题查看答案及解析
-
下列数据是对应物质的熔点(℃):
BCl3
Al2O3
Na2O
NaCl
AlF3
AlCl3
干冰
SiO2
-107
2 073
920
801
1 291
190
-57
1 723
据此做出的下列判断中错误的是( )
A.铝的化合物的晶体中有的是离子晶体
B.表中只有BCl3和干冰是分子晶体
C.同族元素的氧化物可形成不同类型的晶体
D.不同族元素的氧化物可形成相同类型的晶体
高三化学选择题中等难度题查看答案及解析
-
(6分)(1)下列数据是对应物质的熔点(℃)
NaCl
Na2O
AlF3
AlCl3
BCl3
Al2O3
CO2
SiO2
801
920
1291
190
-109
2073
-57
1723
据此作出的下列判断中,错误的是________
A、铝的化合物晶体中有离子晶体
B、表中只有BCl3、干冰是分子晶体
C、同族元素的氧化物可形成不同类型的晶体
D、不同族元素的氧化物可形成不同类型的晶体
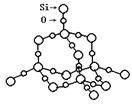
(2)SiO2晶体结构片断如图所示。SiO2晶体中Si和Si-O键的比例为_____________。
通常人们把拆开1mol 某化学键所吸收的能量看成该化学键的键能。
化学键
Si-O
Si-Si
O=O
键能/ KJ·mol-1
460
176
498
Si(s)+O2(g)
SiO2(s),该反应的反应热△H = ___________
高三化学填空题简单题查看答案及解析