-
C、N、S元素都是生命体的重要组成元素,它们在自然界的平衡已受到较大的破坏.C、N、S元素在地球大气圈、岩石圈、水系、生物圈等的循环过程中会产生的物质是①HNO3 ②CO2 ③糖类 ④CH4 ⑤SO2 ( )
A.①②③④⑤ B.②③⑤ C.②③④ D.②
高一化学选择题简单题查看答案及解析
-
C、N、S元素都是生命体的重要组成元素,它们在自然界的平衡已受到较大的破坏。C、N、S元素在地球大气圈、岩石圈、水系、生物圈的循环过程中会产生的物质是
①HNO3 ②CO2 ③糖类 ④CH4
A. ② B. ②③ C. ②③④ D. ①②③④
高一化学选择题简单题查看答案及解析
-
在人类社会的发展进程中,金属起着重要的作用。下列说法正确的是
A.地球上绝大多数金属元素是以游离态存在于自然界中的
B.在化学反应中,金属容易失去电子,是还原剂
C.多数合金的熔点高于组成它的成分的金属的熔点
D.硅单质是良好的半导体,所以它是金属元素
高一化学选择题中等难度题查看答案及解析
-
硅是在人类文明发展过程中起了重要作用的元素。下列有关硅的说法正确的是( )
A. 硅是构成矿物和岩石的主要元素,硅在地壳中的含量在所有的元素中居第一位
B. 硅在自然界中有单质存在
C. 光纤通信是以光作为信息的载体,光导纤维的主要成分是SiO2
D. 硅单质的性质十分稳定,不能和任何物质发生反应
高一化学单选题简单题查看答案及解析
-
下面叙述中,正确的是( )
A.硅是构成矿物和岩石的主要元素,硅在地壳中的含量在所有的元素中居第一位
B.水泥是重要的硅酸盐产品,以纯碱、石灰石、二氧化硅为原料
C.硅的化学性质不活泼,在自然界中可以以游离态存在
D.硅是一种亲氧元素,在自然界中它总是与氧相互化合
高一化学选择题中等难度题查看答案及解析
-
下面有关硅的叙述中,正确的是
A.二氧化硅在电子工业中,是最重要的半导体材料
B.硅是构成矿物和岩石的主要元素,硅在地壳中的含量在所有的元素中居第一位
C.硅的化学性质不活泼,在自然界中可以以游离态存在
D.光导纤维是以二氧化硅为主要原料制成的
高一化学选择题中等难度题查看答案及解析
-
如图是自然界中N、S两种元素的循环过程:根据如图内容,判断下列说法正确的是( )
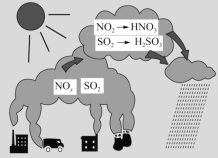
A.图示过程表示了地球臭氧层的破坏过程
B.图中涉及的氧化物均为酸性氧化物
C.机动车尾气含有氮的氧化产物
D.图示中描述的过程所涉及的反应均为氧化还原反应
高一化学单选题简单题查看答案及解析
-
四种短周期元素A、B、C、D的性质或结构信息如下:
信息:①原子半径:A>B>C>D ②四种元素之间形成的某三种分子的比例模型及部分性质如下:
甲:
是地球上最常见的物质之一,是所有生命体生存的重要资源,约占人体体重的三分之二。
乙:
无色,无气味并且易燃。是常见的一种基础能源。
丙:
有强氧化性的弱酸,可以用于消毒杀菌。
请根据上述信息回答下列问题。
(1)B元素在元素周期表中的位置为________________,请写出BC2分子的电子式:_______________。
(2)A所在周期中,E元素的单质还原性最强,F元素的某些盐类常用作净水剂。E单质与甲反应有化合物X生成。请写出以下两个反应的离子方程式:
①A元素的单质与物质甲发生反应:_____________________________________。
②F、C两种元素组成的化合物Y可作为高温结构陶瓷材料,X与Y两种化合物在溶液中发生反应:______________________________________________________。
(3)物质丁的元素组成和甲相同,丁分子具有18电子结构。向盛有一定浓度丁溶液的试管中,逐滴加入硫酸酸化的硫酸亚铁溶液。滴加过程中的现象为:
①试管中溶液变成深棕黄色,发生反应的离子方程式为 ;
②开始有少量气泡出现(经验证是氧气),片刻后反应变得剧烈,继续滴加溶液,静置一段时间,试管底部出现红褐色沉淀。请回答“片刻后反应变得剧烈”的原因是a b
高一化学填空题简单题查看答案及解析
-
四种短周期元素A、B、C、D的性质或结构信息如下:
信息:①原子半径:A>B>C>D ②四种元素之间形成的某三种分子的比例模型及部分性质如下:
甲:
是地球上最常见的物质之一,是所有生命体生存的重要资源,约占人体体重的三分之二。
乙:
无色,无气味并且易燃。是常见的一种基础能源。
丙:
有强氧化性的弱酸,可以用于消毒杀菌。
请根据上述信息回答下列问题。
(1)B元素在元素周期表中的位置为________________,请写出BC2分子的电子式:_______________。
(2)A所在周期中,E元素的单质还原性最强,F元素的某些盐类常用作净水剂。E单质与甲反应有化合物X生成。请写出以下两个反应的离子方程式:
①A元素的单质与物质甲发生反应:_____________________________________。
②F、C两种元素组成的化合物Y可作为高温结构陶瓷材料,X与Y两种化合物在溶液中发生反应:______________________________________________________。
(3)物质丁的元素组成和甲相同,丁分子具有18电子结构。向盛有一定浓度丁溶液的试管中,逐滴加入硫酸酸化的硫酸亚铁溶液。滴加过程中的现象为:
①试管中溶液变成深棕黄色,发生反应的离子方程式为 ;
②开始有少量气泡出现(经验证是氧气),片刻后反应变得剧烈,继续滴加溶液,静置一段时间,试管底部出现红褐色沉淀。请回答“片刻后反应变得剧烈”的原因是a b
高一化学填空题简单题查看答案及解析
-
硅和氮均是自然界含量丰富的元素,其单质及其化合物在环境、能源及材料科学中有着重要影响和广泛应用.试回答下列问题:
(1) 向大气中排放NOx可能导致的环境问题有________.(答两点)已知足量NaOH溶液能完全吸收NO2生成氮的两种含氧酸盐(氮为+3、+5价).试写出该反应的离子方程式________ .
(2) 光导纤维的作用,让人们的生活更加丰富精彩,________是制备光导纤维的基本原料.
(3) 氮化硅陶瓷是一种新型无机非金属材料,其化学式为________, 可由硅粉(用Al2O3和Y2O3作助剂)在氮气中高温烧结而成,氮气在反应中既是反应物,同时又起了
________作用.由于使用的硅粉表面含二氧化硅,在反应中需加入碳粉.在烧结过程中,二氧化硅、碳、氮气以物质的量之比3∶6∶2反应生成两 种化合物,该反应的化学方程式为________.
(4) 硅燃烧放出大量热量,“硅能源”有望成为二十一世纪的新能源.与“氢能源”比较“硅能源”具有________等更加优越的特点,从而得到全球的关注和期待.
高一化学填空题简单题查看答案及解析