-
某矿抽出的废液中含有大量的K+、Cl-、Br-,还有少量的Ca2+、Mg2+、SO 。某研究性学习小组获取这种废液来制取较纯净的氯化钾晶体及液溴(Br2),他们设计了如下流程:
。某研究性学习小组获取这种废液来制取较纯净的氯化钾晶体及液溴(Br2),他们设计了如下流程:
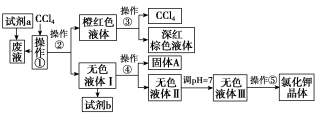
可供试剂a、b的选择试剂:饱和Na2CO3溶液、饱和K2CO3溶液、KOH溶液、BaCl2溶液、Ba(NO3)2溶液、H2O2溶液、稀盐酸。(已知:2Br-+2H++H2O2=Br2+2H2O)
请根据以上流程,回答相关问题:
(1)试剂a应该选用_________________。
(2)操作①、②、③、④、⑤的名称是______________________________(填字母)。
A.萃取、过滤、分液、过滤、蒸发 B.萃取、分液、蒸馏、过滤、蒸发
C.分液、萃取、过滤、过滤、蒸发 D.萃取、分液、分液、过滤、蒸 发
发
(3)除去无色液体Ⅰ中的Ca2+、Mg2+、SO ,选出b所代表的试剂,按滴加顺序依次是______________(填化学式)。
,选出b所代表的试剂,按滴加顺序依次是______________(填化学式)。
(4)调节pH的作用是________________,操作方法是_________________。
(5)操作⑤中用到的瓷质仪器的名称是__________________。
-
某废液中含有大量的K+、Cl-、Br-,还有少量的Ca2+、Mg2+、SO42-。某研究性学习小组利用这种废液来制取较纯净的氯化钾晶体及液溴(Br2),设计了如下流程图:
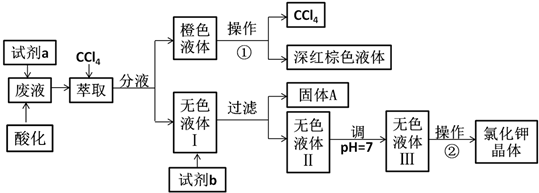
可供选择的试剂:①饱和Na2CO3溶液;②饱和K2CO3溶液;③KOH溶液;④BaCl2溶液;⑤Ba(NO3)2溶液;⑥H2O2溶液;⑦KMnO4溶液(H+);⑧稀盐酸。
请根据流程图,回答相关问题:
(1)试剂a应该选用______(填试剂编号),反应的离子方程式为____________。
(2)萃取操作中,可以选的试剂还可以是_________。
A. 裂化汽油 B.乙醇 C.苯 D.直馏汽油
(3)除去无色液体Ⅰ中的Ca2+、Mg2+、SO42-,选出试剂b(试剂b代表一组试剂)所代表的试剂,按滴加顺序依次是__________。(填试剂序号)
(4)调节pH的作用是___________________________________。
(5)操作①的名称是_____,操作②中用到的硅酸盐仪器除酒精灯、玻璃棒外还有________。
-
某废液中含有大量的K+、Cl-、Br-,还有少量的Ca2+、Mg2+、SO42ˉ。某研究性学习小组利用这种废液来制取较纯净的氯化钾晶体及液溴(Br2),设计了如图所示的流程图:
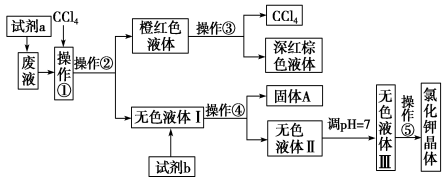
可供试剂a、试剂b(试剂b代表一组试剂)选择的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、KOH溶液、BaCl2溶液、Ba(NO3)2溶液、H2O2溶液、酸性KMnO4溶液、稀盐酸。
请根据流程图,回答相关问题:
(1) 操作①②③④⑤的名称是_____________
①_______②________③________④________⑤________
(2) 除去无色液体Ⅰ中的Ca2+、Mg2+、SO42ˉ, 选出试剂b所代表的试剂,按滴加顺序依次是________________(填化学式)。
选出试剂b所代表的试剂,按滴加顺序依次是________________(填化学式)。
(3)调节pH的目的是____________________,操作方法是_______________________。
(4)操作⑤中用到的瓷质仪器名称是 。
-
某工厂排放的废液中含有大量的K+、Cl-、Br-,还有少量的Ca2+、Mg2+、SO42-。某研究性小组利用这种废液来制取较纯净的氯化钾晶体及液溴,他们设计了如下的流程(提示:图中试剂a的作用是将Br-转化为Br2)

试剂b需要从以下试剂中选择:饱和Na2CO3溶液、饱和K2CO3溶液、KOH溶液、BaCl2溶液、Ba(NO3)2溶液、稀盐酸
(1)操作①②③④⑤的名称是________(填序号)。
A. 萃取、过滤、分液、过滤、蒸发结晶
B. 萃取、分液、蒸馏、过滤、蒸发结晶
C. 分液、萃取、过滤、过滤、蒸发结晶
D. 萃取、分液、分液、过滤、蒸发结晶
(2)除去无色液体Ⅰ中的Ca2+、Mg2+、SO42-,选出试剂b(试剂b代表一组试剂)所代表的试剂,按滴加顺序依次是_____________________________________________________________。
(3)调节pH=7的作用是________________________________________,所用的试剂是___________(填名称)
(4)操作⑤中用到的瓷质仪器名称是________________
-
某厂排放的废液中含有大量的K+、Cl-、Br-,还含有少量的Ca2+、Mg2+、SO42-.某研究性学习小组拟取这种工业废水来制取较纯净的氯化钾晶体及液溴,他们设计了如下的流程:(已知:若用实际参加反应的离子表示化学反应,则溶液中可能发生如下反应:
H2O2+2Br- =H2O+Br2;10Br-+2MnO4-+16H+ =2Mn2++5Br2+8H2O)
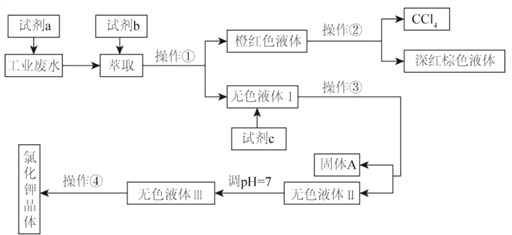
可供试剂a、b、c选择的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、KOH溶液、BaCl2溶液、Ba(NO3)2 溶液、苯、CCl4、H2O2溶液、KMnO4(H+)溶液.
根据以上流程回答相关问题:
⑴试剂a、b分别是_________、___________.
⑵操作①②③④的名称是__________(填字母代号)
a. 过滤、分液、过滤、蒸发结晶
b. 分液、蒸馏、过滤、蒸发结晶
c. 分液、过滤、过滤、蒸发结晶
d. 分液、分液、过滤、蒸发结晶
⑶除去无色液体Ⅰ中的 Ca2+、 Mg2+、 SO42-,选出 c 所代表的试剂,按滴加顺序依次是_________(只填化学式).
⑷调节 pH 的作用是___________________________________.
-
某研究性学习小组拟从盐卤液(含Na+、Cl-、Mg2+、Ca2+、I-、SO42-),来制取较纯净的氯化钠晶体及单质碘(I2),他们设计了如下实验:
第一步:提取碘
(1)在盐卤液中通入Cl2可使I-氧化为碘单质(I2),反应的离子方程式为_______________
(2)要将此反应后的溶液中的碘单质分离出来,先加入一种试剂可以得到一种紫红色液体,这种试剂是___________(填字母编号)
A.盐酸 B.四氯化碳 C.氢氧化钠溶液 D.酒精
该分离方法称为___________。
(3)要从紫红色液体中再分离出单质碘,还需要采取下图的分离操作,该分离方法称为___________。(填分离操作名称)
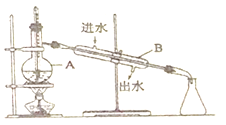
①指出图中的两处明显错误_________________;___________________。
②写出仪器名称:A_____________,B________________。
第二步:粗盐提纯
(4)提取碘后,溶液中主要含有Na+、Cl-、Ca2+、Mg2+、SO42-,为了得到纯净的NaCl,然后在下列操作中选取必要的步骤和正确的操作顺序______________(有多少选多少)
①过滤②加过量NaOH溶液③加适量盐酸④加过量Na2CO3溶液⑤加过量BaCl2溶液
-
某研究性学习小组利用软锰矿浆(主要成分是MnO2)吸收工业废气中的SO2,并制备硫酸锰的生产流程如下(浸出液的pH<2,其中除含Mn2+外,还含有少量Fe2+、Al3+、Ca2+等金属离子):
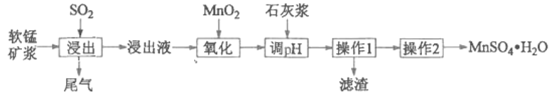
“操作1”的滤液通过阳离子吸附剂除去Ca2+。金属离子形成氢氧化物沉淀时的pH见下表:
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 7.6 | 9.7 |
| Fe3+ | 2.7 | 3.7 |
| Al3+ | 3.8 | 4.7 |
| Mn2+ | 8.3 | 9.8 |
(1)浸出过程中被氧化的物质的化学式为____________。
(2)氧化过程中主要反应的离子方程式为_____________
(3)在氧化后的液体中加入石灰浆调节pH, pH 的范围是__________。
(4)操作2包括蒸发浓缩、__________、 过滤、 洗涤、干燥等操作。
(5)为测定所得MnSO4·H2O的纯度,准确称取上述样品1.720 g加入适量H2SO4和NH4NO3溶液,加热使Mn2+全部氧化成Mn3+后,配成200 mL溶液。取20.00 mL该溶液,向其中逐滴加入0.0500 mol·L-1的FeSO4溶液,发生如下反应: Fe2+ +Mn3+=== Fe3+ + Mn2+当反应恰好完全进行时,共消耗FeSO4溶液19.50 mL。计算MnSO4·H2O的纯度(写出计算过程,结果保留四位有效数字)__
-
某研究性学习小组同学用含有少量泥沙、CaCl2、MgCl2、Na2SO4的粗盐制取纯净的NaCl,实验前他们设计了如图方案(框图)
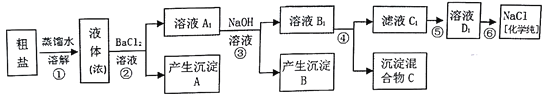
(1)请写出操作第④步所加试剂名称及第②步操作名称:
④_____________________,②___________________________。
(2)写出第⑤步操作中可能发生反应的离子方程式:____________________。
(3)如何检验第②步操作中硫酸根离子已完全除尽:_____________________。
(4)你认为该设计里哪些步骤调换后不影响实验结果:___________________。
-
某化学研究性学习小组为确定一化工废液的成分,进行了如下实验操作:向少量样品废液中加入过量盐酸时有白色沉淀生成。过滤后,向滤液中加入过量氨水使溶液呈碱性时,有白色沉淀生成,过滤后,向滤液中加入小苏打溶液,又有白色沉淀生成。则该化学成分是( )
A.AlO2―、Ba2+、Mg2+ B.Ag+、Ca2+、Al3+
C.Ag+、Mg2+、Na+ D.AlO2―、Na+、Ba2+
-
现代工业常以氯化钠为原料制备纯碱,部分工艺流程如图:
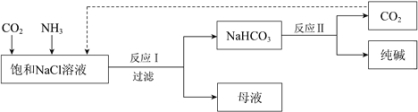
(1)工业生产中,反应I的化学方程式是______。
(2)海水中含有大量的NaCl,以及少量的Ca2+、Mg2+、SO42−等离子。
①为得到纯净的饱和NaCl溶液,进行了如下操作。请补全操作步骤:
a.向浓缩后的海水中加入过量的氢氧化钠溶液后,过滤;
b.向滤液中_______,过滤;
c.向滤液中_______,过滤;
d.向滤液中加入足量的稀盐酸;
e.加热煮沸一段时间,得到饱和NaCl溶液。
②步骤c中反应的离子方程式有____。
(3)反应II的化学方程式是______。
(4)制得的纯碱中含有少量NaCl。取5.5g纯碱样品加入足量稀硫酸,得到标准状况下1120mLCO2。则样品中纯碱的质量分数是______%(保留1位小数)。
。某研究性学习小组获取这种废液来制取较纯净的氯化钾晶体及液溴(Br2),他们设计了如下流程:

发
,选出b所代表的试剂,按滴加顺序依次是______________(填化学式)。







