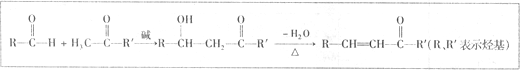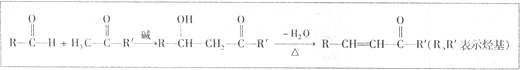-
一氧化碳是一种用途广泛的化工基础原料。有机物加氢反应中镍是常用的催化剂。但H2中一般含有微量CO会使催化剂镍中毒,在反应过程中消除CO的理想做法是投入少量SO2,为弄清该方法对催化剂的影响,查得资料如下:
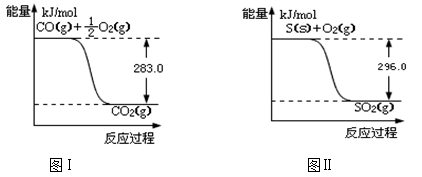
回答下列问题:
(1)SO2(g) + 2CO(g)  S(s) + 2CO2(g) △H = ;该反应的平衡常数的表达式是 。
S(s) + 2CO2(g) △H = ;该反应的平衡常数的表达式是 。
(2)工业上用一氧化碳制取氢气的反应为:CO(g)+H2O(g)  CO2(g)+H2(g),已知420℃时,该反应的化学平衡常数K=9。如果反应开始时,在2L的密闭容器中充入CO和H2O的物质的量都是0.60mol,5min末达到平衡,则此时CO的转化率为 ,H2的平均生成速率为 mol·L-1·min-1。
CO2(g)+H2(g),已知420℃时,该反应的化学平衡常数K=9。如果反应开始时,在2L的密闭容器中充入CO和H2O的物质的量都是0.60mol,5min末达到平衡,则此时CO的转化率为 ,H2的平均生成速率为 mol·L-1·min-1。
(3)为减少雾霾、降低大气中有害气体含量,研究机动车尾气中CO、NO及CxHy的排放量意义重大。机动车尾气污染物的含量与空/燃比(空气与燃油气的体积比)的变化关系如图所示。
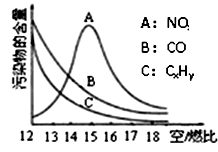
已知:N2与O2生成NO的反应是吸热反应。请解释:
①随空/燃比增大,CO和CxHy的含量减少的原因是 。
②当空/燃比达到15后,NO减少的原因可能是 。
(4)一定条件下H2与CO合成CH3OH,CH3OH再转化成为CH3OCH3,转化的热化学反应方程式如下:2CH3OH(g)  CH3OCH3(g)+H2O(g) ΔH=-24.5 kJ·mol-1
CH3OCH3(g)+H2O(g) ΔH=-24.5 kJ·mol-1
在250℃、压强不变的密闭容器中,加入2mol的CH3OH,一段时间后上述反应达平衡,体系放出热量11 kJ;若同一条件下加入0.2mol CH3OCH3和0.2mol H2O,一段时间后上述反应达平衡,体系的热效应为 .
-
一氧化碳是一种用途广泛的化工基础原料。有机物加氢反应中镍是常用的催化剂。但H2中一般含有微量CO会使催化剂镍中毒,在反应过程中消除CO的理想做法是投入少量SO2,为弄清该方法对催化剂的影响,查得资料如下:
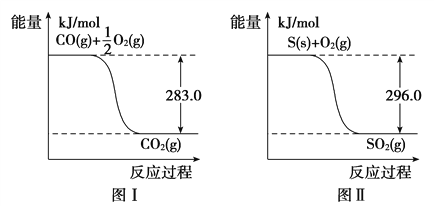
则:(1)① 不用通入O2氧化的方法除去CO的原因是 ______________________________。
②SO2(g)+2CO(g)===S(s)+2CO2(g) ΔH=________。
(2)工业上用一氧化碳制取氢气的反应为:CO(g)+H2O(g)  CO2(g)+H2(g),已知420 ℃时,该反应的化学平衡常数K=9。如果反应开始时,在2 L的密闭容器中充入CO和H2O的物质的量都是0.60 mol,5 min末达到平衡,则此时CO的转化率为________,H2的平均生成速率为________ mol·L-1·min-1。
CO2(g)+H2(g),已知420 ℃时,该反应的化学平衡常数K=9。如果反应开始时,在2 L的密闭容器中充入CO和H2O的物质的量都是0.60 mol,5 min末达到平衡,则此时CO的转化率为________,H2的平均生成速率为________ mol·L-1·min-1。
(3)为减少雾霾、降低大气中有害气体含量, 研究机动车尾气中CO、NOx及CxHy的排放量意义重大。机动车尾气污染物的含量与空/燃比 (空气与燃油气的体积比)的变化关系示意图如图所示:
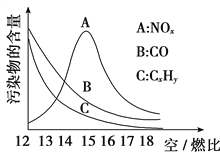
①随空/燃比增大,CO和CxHy的含量减少的原因是_____________________________。
②当空/燃比达到15后,NOx减少的原因可能是____________________________________________。
-
煤的气化主要生成CO、H2等,其中CO、H2是用途相当广泛的化工基础原料。但煤的气化获得的化工原料气中常含有少量羰基硫(COS),能引起催化剂中毒、大气污染等。
(1)COS的电子式为_____________________。
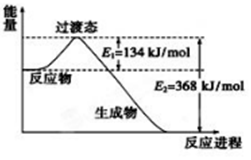
(2)下图是1molCO和lmolNO2反应生成两种气态氧化物过程屮能量变化示意图。已知14克CO参加反应时转移电子数为NA。写出该反应的热化学方程式_______________________。
(3)在某一恒温、恒容的密闭容器中发生以下反应:Ni(S)+4CO(g) 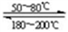 Ni(CO)4(g)。下列说法正确的是__________。
Ni(CO)4(g)。下列说法正确的是__________。
A.该反应的反应热△H<0
B.增加Ni的量可提高CO的转化率,Ni的转化率降低
C.反应达到平衡后,充入CO再次达到平衡时,CO的浓度增大
D.当v正[Ni(CO)4]=4v逆(CO)时或容器中混合气体密度不变时,都可说明反应已达化学平衝状态
(4)工业上采用CO与H2反应合成甲醇,反应如下CO(g)+2H2(g) CH3OH(g)。在T℃时,将2molCO和amolH2充入2L的恒容密闭容器中充分反应,l0min后反应达到平衡。已知v(CH3OH)=0.05mol•L-1•min-1,且CO和H2的转化率相等。
CH3OH(g)。在T℃时,将2molCO和amolH2充入2L的恒容密闭容器中充分反应,l0min后反应达到平衡。已知v(CH3OH)=0.05mol•L-1•min-1,且CO和H2的转化率相等。
①H2的转化率为_________________,反应未开始时的容器内气体压强P1与反应达平衡时压强P2的比值为__________________。
②以甲醇燃料电池为电源,熔融盐电解法制取硅烷原理如图。阳极的电极反应式为_______________。

(5)甲醇可制备二甲醚:2CH3OH(g) CH3OCH3(g)+ H2O(g),K =1 (300℃测定)。
CH3OCH3(g)+ H2O(g),K =1 (300℃测定)。
①在300℃时,测得n(CH3OCH3)=2n(CH3OH),此时反应的v正__________v逆(填“〉”、“〈”或“=”〉,你的分析理由是___________________。
②二甲醚催化重整制氢的反应过程,主要包括以下几个反应(以下数据为25℃、1.01×l05Pa测定):
Ⅰ:CH3OCH3(g)+H2O(1) 2CH3OH(1)△H>0
2CH3OH(1)△H>0
Ⅱ:CH3OH(1)+H2O(1) CO2(g)+3H2(g)△H>0
CO2(g)+3H2(g)△H>0
Ⅲ:CO(g)+H2O(1) CO2(g)+H2(g)△H<0
CO2(g)+H2(g)△H<0
Ⅳ:CH3OH(l) CO(g)-2H2(g)△H>0
CO(g)-2H2(g)△H>0
工业生产中测得不同温度下各组分体积分数及二甲醚转化率的关系如下图所示,

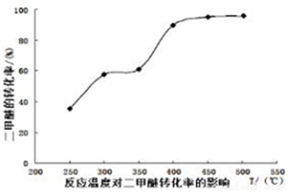
你认为反应控制的最佳温度应为__________。
A. 300〜350℃ B. 350〜40℃ C. 400〜450℃ D. 450〜500℃
-
硫的化合物在化工生产、污水处理等领域应用广泛。
Ⅰ.羰基硫(O=C=S)广泛存在于以煤为原料制备的各种化工原料气中,能引起催化剂中毒、大气污染等。羰基硫的水解和氢解是两种常用的脱硫方法,其反应式分别为:
a.水解反应:COS(g)+H2O(g) H2S(g)+CO2(g) △H1=-35 kJ/mol
H2S(g)+CO2(g) △H1=-35 kJ/mol
b.氢解反应:COS(g)+H2(g) H2S(g)+CO(g) △H2
H2S(g)+CO(g) △H2
已知:CO(g)+H2O(g) H2(g)+CO2(g) △H3=-42kJ/mol
H2(g)+CO2(g) △H3=-42kJ/mol
(1)完成上述氢解反应的热化学方程式:______。
(2)一定条件下,密闭容器中发生反应 a,其中 COS(g)的平衡转化 率(α)与温度(T)的关系如图所示。则 A、B、C 三点对应的状态中,v(COS)=v(H2S)的是______(填字母)。

(3)反应 b 的正、逆反应的平衡常数(K)与温度(T)的关系如图所示,其中表示正反应的平衡常数(K 正)的是______(填“A”或“B”)。
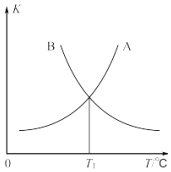
(4)T1℃时,向容积为 10L 的恒容密闭容器中充入2mol COS(g)和2mol H2(g),发生反应 b,则:COS的平衡转化率为______。
Ⅱ.矿石冶炼与含硫化合物有关。
(5)将冰铜矿(主要为Cu2S和FeS相熔合而成)加熔剂(石英砂)在1200℃左右吹入空气 进行吹炼:Cu2S被氧化为Cu2O,生成的Cu2O与Cu2S反应,生成含Cu量约为98.5%的粗铜,该过程中发生反应的化学方程式分别是:___________;___________。
(6)废气中的SO2可用NaOH溶液吸收,吸收SO2后的碱性溶液还可用于Cl2的尾气处理,吸收Cl2后的溶液仍呈强碱性。
①吸收Cl2后的溶液中一定存在的阴离子有OH-、______。
②吸收Cl2后的溶液中可能存在SO32-,取该溶液于试管中,滴加黄色的溴水,得到无色溶液。此实验不能证明溶液中含有SO32-,理由是___________。
-
羰基硫(O=C=S)广泛存在于以煤为原料制备的各种化工原料气中,能引起催化剂中毒、化学产品质量下降和大气污染等。羰基硫的氢解和水解反应是两种常用的脱硫方法,其反应式分别为:
①氢解反应:COS(g)+H2(g) H2S(g)+CO(g) ΔH1=+7 kJ·mol-1
H2S(g)+CO(g) ΔH1=+7 kJ·mol-1
②水解反应:COS(g)+H2O(g) H2S(g)+CO2(g) ΔH2=-35 kJ·mol-1
H2S(g)+CO2(g) ΔH2=-35 kJ·mol-1
请回答下列问题:
(1)已知热化学方程式:CO(g)+H2O(g) H2(g)+CO2(g) ΔH3,则ΔH3 =_______。
H2(g)+CO2(g) ΔH3,则ΔH3 =_______。
(2)水解反应达到平衡后,若减小容器的体积,则逆反应速率_______________(填“增大”、“减小”或“不变”,下同),COS的转化率_______________。
(3)COS氢解反应的平衡常数K与温度T具有如下的关系式 (a、b均为常数)
(a、b均为常数)
①如图能表示COS的氢解反应的直线为____________。
②一定条件下,催化剂Ⅰ和Ⅱ对COS氢解反应的催化作用如下:
| 达到平衡所需时间/min | a 的数值 | b的数值 |
| 催化剂Ⅰ | t | a1 | b1 |
| 催化剂Ⅱ | 2t | a2 | b2 |
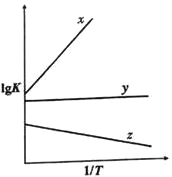
则a1_______________a2 (填“>”、“<”、“=”)。
(4)某温度下,维持体系体积恒定,物质的量分别为m、n的COS蒸气和H2发生氢解反应。已知COS的平衡转化率为α,则在该温度下反应的平衡常数K=________(用m、n、α等符号表示)。
-
羰基硫(O=C=S)广泛存在于以煤为原料制备的各种化工原料气中,能引起催化剂中毒、化学产品质量下降和大气污染等。羰基硫的氢解和水解反应是两种常用的脱硫方法,其反应式分别为:
①氢解反应:COS(g)+H2(g) H2S(g)+CO(g) ΔH1=+7 kJ·mol-1
H2S(g)+CO(g) ΔH1=+7 kJ·mol-1
②水解反应:COS(g)+H2O(g) H2S(g)+CO2(g) ΔH2=-35 kJ·mol-1
H2S(g)+CO2(g) ΔH2=-35 kJ·mol-1
请回答下列问题:
(1)已知热化学方程式:CO(g)+H2O(g) H2(g)+CO2(g) ΔH3,则ΔH3 =_______。
H2(g)+CO2(g) ΔH3,则ΔH3 =_______。
(2)水解反应达到平衡后,若减小容器的体积,则逆反应速率_______________(填“增大”、“减小”或“不变”,下同),COS的转化率_______________。
(3)COS氢解反应的平衡常数K与温度T具有如下的关系式 (a、b均为常数)
(a、b均为常数)
①如图能表示COS的氢解反应的直线为____________。
②一定条件下,催化剂Ⅰ和Ⅱ对COS氢解反应的催化作用如下:
| 达到平衡所需时间/min | a 的数值 | b的数值 |
| 催化剂Ⅰ | t | a1 | b1 |
| 催化剂Ⅱ | 2t | a2 | b2 |
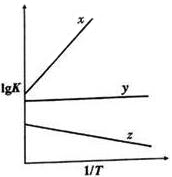
则a1_______________a2 (填“>”、“<”、“=”)。
(4)某温度下,维持体系体积恒定,物质的量分别为m、n的COS蒸气和H2发生氢解反应。已知COS的平衡转化率为α,则在该温度下反应的平衡常数K=________(用m、n、α等符号表示)。
-
(10分)一氧化碳是一种用途相当广泛的化工基础原料。
(1)利用下列反应可以将粗镍转化为纯度达99.9%的高纯镍: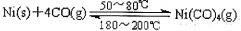 ,则该反应的△ H 0(选填“>”或“<”)。
,则该反应的△ H 0(选填“>”或“<”)。
(2)在高温下一氧化碳可将二氧化硫还原为单质硫。已知:
C(s)+O2(g)=CO2(g) △ H 1=-393.5kJ·mol-1
CO2(g)+C(s) =2CO(g) △ H 2=+172.5kJ·mol-1
S(s)+O2(g) =SO2(g) △ H 3=-296.0kJ·mol-1
请写出CO除SO2的热化学方程式 。
(3)工业上用一氧化碳制取氢气的反应为:CO(g)+H2O(g) CO2(g)+H2(g),已知420℃时,该反应的化学平衡常数为9.0。如果反应开始时,在2L的密闭容器中充入CO 和H2O的物质的量都是0.60mol,5min末达到平衡,则此时CO的转化率为 。
CO2(g)+H2(g),已知420℃时,该反应的化学平衡常数为9.0。如果反应开始时,在2L的密闭容器中充入CO 和H2O的物质的量都是0.60mol,5min末达到平衡,则此时CO的转化率为 。
(4)下图是一种新型燃料电池,它以CO为燃料,一定比例的Li2CO3和Na2CO3熔融混合物为电解质,图2是粗铜精炼的装置图,现用燃料电池为电源进行粗铜的精炼实验。回答下列问题:
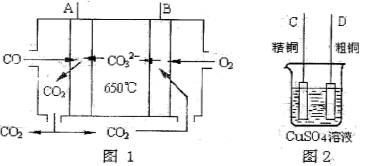
①写出A极发生的电极反应式 。
②要用燃料电池为电源进行粗铜的精炼实验,则B极应该与 极(填“C”或“D”)相连。
③当消耗标准状况下2.24LCO时,C电极的质量变化为 。
-
碱式碳酸铜[CuCO3·Cu(OH)2]是一种用途广泛的化工原料,可用于作有机催化剂、颜料制造、原油贮存时脱碱等。用废杂铜(主要成分为Cu,还含有少量杂质Fe)制取碱式碳酸铜的工艺流程如图所示。
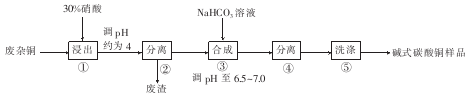
(1)步骤①浸出时,硝酸浓度不易过大,其原因是____。
(2)步骤②分离前需将溶液pH调节在4左右,其目的是 ,所得废渣的主要成分为____________。
(3)步骤③合成时,采用将NaHCO3溶液迅速投入Cu(NO3)2溶液中,其主要原因是 ;合成时发生反应的化学方程式为____________。
(4)本实验中两次用到固液分离,本实验中最适合固液分离的设备是____________。
(5)步骤⑤洗涤主要除去的杂质离子是 。
(6)准确称取所得产品m g,放入碘量瓶中,加入2 g KI及5 ml3 mol/L稀硫酸(两试剂均过量)摇匀并静置10 min(2Cu2++4I-=2CuI↓+I2),再加入2 mL淀粉溶液,用c mol/L的Na2S2O3标准溶液滴定(I2+2S2O32-=2I-+S4O62-),到滴定终点时消耗Na2S2O3标准溶液V mL,则样品中铜元素的质量分数为________。
-
有机物OPP是用途十分广泛的有机化工产品,广泛应用于杀菌防腐、印染助剂、表面活性剂、稳定剂和阻燃剂等领域.以烃A为原料可合成OPP:
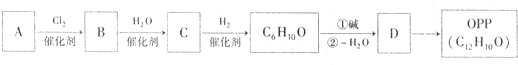
已知醛或酮在碱催化下可发生如下反应: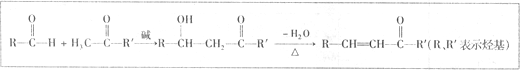
(1)①烃A是无色、带有特殊气味的液体.经实验测定,烃A中碳元素和氢元素的质量比为mc:mB=12:1.烃A的结构简式为______.
②(填操作名称)______是分离,提纯液态有机物的常用方法,烃A就是用该方法从煤焦油中得到的基本化工原料.
(2)烃A生成有机物B的反应类型为______.
(3)①有机物C能与NaOH反应,反应的化学方程式为______.
②有机物C与浓溴水反应生成白色沉淀,可用于有机物C的定性检验和定量测定,反应的化学方程式为______.
(4)有机物C6H10O的红外光谱图显示分子中含有C=O键,但是C6H10O不能发生银镜反应.C6H10O的结构简式为______.
(5)有机物D的结构简式为______.
(6)有机物D在钯催化剂催化下进行脱氢反应得到OPP,OPP的红外光谱图显示分子中有O-H键和苯环.OPP的一种同分异构体E和OPP具有相同的基团,其核磁共振氢谱有6个峰,峰面积之比为1:2:2:2:2:1,有机物E的结构简式为______.
-
有机物OPP是用途十分广泛的有机化工产品,广泛应用于杀菌防腐、印染助剂、表面活性剂、稳定剂和阻燃剂等领域.以烃A为原料可合成OPP:
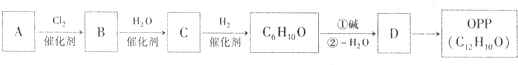
已知醛或酮在碱催化下可发生如下反应: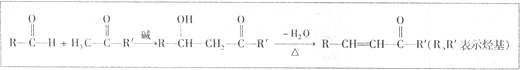
(1)①烃A是无色、带有特殊气味的液体.经实验测定,烃A中碳元素和氢元素的质量比为mc:mB=12:1.烃A的结构简式为______.
②(填操作名称)______是分离,提纯液态有机物的常用方法,烃A就是用该方法从煤焦油中得到的基本化工原料.
(2)烃A生成有机物B的反应类型为______.
(3)①有机物C能与NaOH反应,反应的化学方程式为______.
②有机物C与浓溴水反应生成白色沉淀,可用于有机物C的定性检验和定量测定,反应的化学方程式为______.
(4)有机物C6H10O的红外光谱图显示分子中含有C=O键,但是C6H10O不能发生银镜反应.C6H10O的结构简式为______.
(5)有机物D的结构简式为______.
(6)有机物D在钯催化剂催化下进行脱氢反应得到OPP,OPP的红外光谱图显示分子中有O-H键和苯环.OPP的一种同分异构体E和OPP具有相同的基团,其核磁共振氢谱有6个峰,峰面积之比为1:2:2:2:2:1,有机物E的结构简式为______.

S(s) + 2CO2(g) △H = ;该反应的平衡常数的表达式是 。
CO2(g)+H2(g),已知420℃时,该反应的化学平衡常数K=9。如果反应开始时,在2L的密闭容器中充入CO和H2O的物质的量都是0.60mol,5min末达到平衡,则此时CO的转化率为 ,H2的平均生成速率为 mol·L-1·min-1。

CH3OCH3(g)+H2O(g) ΔH=-24.5 kJ·mol-1



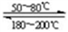 Ni(CO)4(g)。下列说法正确的是__________。
Ni(CO)4(g)。下列说法正确的是__________。





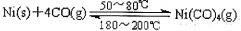 ,则该反应的△ H
,则该反应的△ H