-
铝酸钙(mCaO·nAl2O3)是一系列由氧化钙和氧化铝在高温下烧结而成的无机化合物,被应用于水泥和灭火材料中,工业上用石灰石(主要成分为CaCO3和MgCO3)和铝土矿(主要成分是Al2O3、Fe2O3、SiO2等)制备铝酸钙的流程如图:
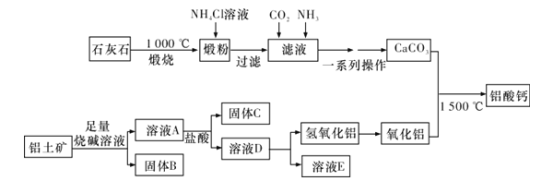
回答下列问题:
(1)固体B的主要成分是__(填化学式);一系列操作包括过滤、洗涤、干燥,洗涤过程应如何操作?__。
(2)向滤液中通入CO2和NH3的顺序为__,其理由是__。
(3)溶液D转化为Al(OH)3;离子方程式是__。
(4)常温下,用适量的NH4Cl溶液浸取煅粉后,若要保持滤液中c(Mg2+)小于5×10-6mol·L-1,则溶液的pH应大于__[已知:Mg(OH)2的K=5×10-12]。
(5)假设上述过程每一步均完全反应,最终得到的铝酸钙(3CaO·7Al2O3)的质量刚好等于原铝土矿的质量,该铝土矿中Al的质量分数为__(计算结果保留三位有效数字)。
-
二氧化硫是硫的重要化合物,在生产、生活中有广泛应用。探究二氧化硫的制取和性质都有着非常重要的意义。
(1)工业上用黄铁矿(FeS2,其中S元素为-1价)在高温下和氧气反应制备SO2:

该反应中被氧化的元素是__________(填元素符号)。当该反应转移5.50mol电子时,生成的二氧化硫在标准状况下的体积为________L。
(2)①实验室可用70%的浓硫酸和亚硫酸钠反应制取二氧化硫,如果能控制反应速度,下图中可选用的发生装置是_______(填写字母)。
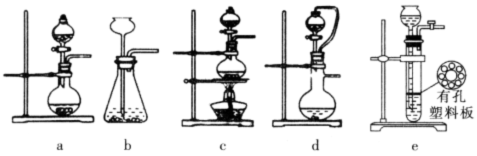
②若用硫酸和亚硫酸钠反应制取3.36L(标准状况)二氧化硫,如果已有4.0%亚硫酸钠(质量分数)被氧化成硫酸钠,则至少需称取该亚硫酸钠_______g(保留一位小数)。
(3)某化学兴趣小组设计用如图装置验证二氧化硫的化学性质。
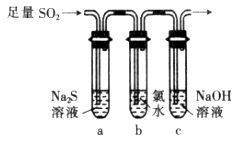
①能说明二氧化硫具有氧化性的实验现象为___________________________。
②为验证二氧化硫的还原性,充分反应后,取试管b中的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液加入品红溶液,红色褪去
方案Ⅱ:向第二份溶液加入BaCl2溶液,产生白色沉淀
方案Ⅲ:向第三份溶液中加入AgNO3溶液,有白色沉淀生成
上述方案中合理的是________(填“Ⅰ”、“Ⅱ”或“Ⅲ”);试管b中发生反应的离子方程式为______________。
-
将SiCl4与过量的液氨反应可生成化合物Si(NH2)4。将该化合物在无氧条件下高温灼烧,可得到氮化硅(Si3N4)固体,氧化硅是一种新型的耐高温、耐磨材料,在工业上有广泛的应用。则氮化硅所属的晶体类型是( )
A. 原子晶体 B. 分子晶体 C. 离子晶体 D. 金属晶体
-
硅单质及其化合物应用范围很广。
(1)制备硅半导体材料必须先得到高纯硅,工业上可以按如下步骤制备纯硅:
Ⅰ.高温下用碳还原二氧化硅制得粗硅
Ⅱ.粗硅与干燥的氯气在450 ℃~500 ℃ 反应制得SiCl4
Ⅲ. SiCl4液体经精馏提纯后与过量H2在1100 ℃~1200 ℃ 反应制得纯硅
已知SiCl4沸点为57.6 ℃,能与H2O强烈反应。1 mol H2与SiCl4气体完全反应吸收的热量为120.2 kJ。请回答下列问题:
① 第Ⅰ步制备粗硅的化学反应方程式为________,第Ⅲ步反应的热化学方程式是________。
②整个制备纯硅过程必须严格控制无水无氧。SiCl4在潮湿的空气中因水解而产生白色烟雾,其生成物是________;H2还原SiCl4过程中若混O2,可能引起的后果是________。
(2)二氧化硅大量用于生产玻璃。工业上用SiO2、Na2CO3和CaCO3共283 kg在高温下完全反应时放出CO2 44 kg,生产出的玻璃可用化学式Na2SiO3·CaSiO3·xSiO2表示,则其中x=。
-
下列说法不正确的是
A.工业上,在高温熔融、隔绝空气的条件下,利用钠单质和钛、钽等金属的氧化物发生置换反应,来制备钛、钽等稀有金属材料
B.铁的化合物应用十分广泛,氯化铁、硫酸亚铁是优良的净水剂
C.铜丝在氯气中燃烧,产生大量棕色的烟,实验结束后在集气瓶中加入少量水,盖上玻片后充分振荡,棕色消失,得到绿色溶液,再加水稀释,最终得到蓝色溶液
D.工业上锌可用湿法冶炼——电解 ZnSO4 溶液制备 Zn
-
某氮铝化合物X具有耐高温、抗冲击、导热性好等优良性质,广泛用于陶瓷工业等领域。
(1)基态氮原子的核外电子排布式为 。
(2)与N互为等电子体的离子有 (任写一种)。
(3)工业上用氧化铝与氮气和碳在一定条件下反应生成X和CO,X的晶体结构如图所示,其化学式为 ,工业制备X的化学方程式为______________________。
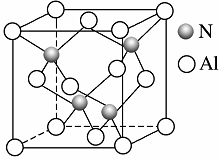
(4)X晶体中包含的化学键类型为________(填字母)。
A.共价键 B.配位键 C.离子键 D.金属键
X晶体中氮原子的杂化类型为________杂化。
(5)已知氮化硼与X晶体类型相同,且氮化硼的熔点比X高,可能的原因是
。
(6)若X的密度为ρ g·cm-3,则晶体中最近的两个Al原子的距离为 cm。(阿伏加德罗常数的值用NA表示)
-
下列说法正确的是
A. 泡沫灭火器中的Al2(SO4)3溶液贮存在钢筒内
B. 乙醇和双氧水都可用于消毒,二者消毒原理相同
C. 太阳能电池板的材料是二氧化硅
D. 工业生产玻璃、水泥漂白粉,均需要用石灰石作原料
-
铝的单质及其化合物在生产、生活、科研等领城应用广泛。
Ⅰ、工业上用铝土矿(主要成分为Al2O3,还含有Fe2O3、FeO、SiO2)制备铝的某种化合物的工艺流程如下:
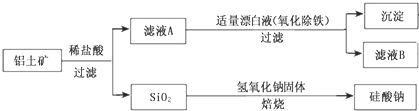
(1)加入盐酸时,氧化铝发生反应的离子方程式为______
(2)在滤液A中加入漂白液,目的是氧化除铁,所得滤液B显酸性。该过程中涉及某氧化还原反应如下,请完成:Fe2++___ClO-+ ________________________ ________________________═ Fe(OH)3↓+ Cl-+__________
Ⅱ、明矾在日常生活、生产中也占有一席之地。
(3)明矾是净水明星,用离子方程式表示其净水原理_____________________________。
(4)向0.02mol的明矾溶液中逐滴加入150mL0.2mol/LBa(OH)2溶液, 生成沉淀的质量为 _____克。
-
下列对应关系或事实的解释正确的是( )
A.NH4Cl水解呈酸性,不能用来当做肥料使用
B.氧化镁的熔点高,可用于制作耐高温的材料
C.氯碱工业中的“碱”指的是Na2CO3
D.水泥、玻璃等硅酸盐材料指的是以二氧化硅为原料生产的材料
-
下列叙述正确的是( )
A.合成氨工业、硫酸工业中均用到吸收塔这一设备
B.玻璃、水泥的工业生产中均用到纯碱和石灰石作为原料
C.光缆在信息产业中有广泛应用,制造光缆的主要材料是二氧化硅
D.绿色化学的核心思想是利用绿色植物治理环境污染




