-
工业上常用天然气作为制备甲醇CH3OH的原料。已知:
①CH4(g)+O2(g)⇌CO(g)+H2(g)+H2O(g)△H=-321.5kJ/mol
②CH4(g)+H2O(g)⇌CO(g)+3H2(g)△H=+250.3kJ/mol
③CO(g)+2H2(g)⇌CH3OH(g)△H=-90kJ/mol
(1)CH4(g)与O2(g)反应生成CH3OH(g)的热化学方程式为______。
(2)向VL恒容密闭容器中充入a mol CO与2a molH2,在不同压强下合成甲醇。CO的平衡转化率与温度、压强的关系如图所示:
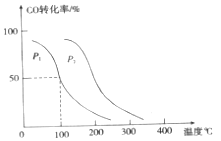
①压强P1______P2(填“<”、“>”或“=”)
②在100℃、P1压强时,平衡常数为______(用含a,V的代数式表示)。
(3)甲醇燃料电池往往采用KOH(或NaOH)浓溶液作电解质溶液,电极采用多孔石墨棒,两个电极上分别通入甲醇和氧气。通入氧气的电极为:通入甲醇的电极上发生的电极反应为:______。用此燃料电池电解某浓度氯化钠溶液,电解一段时间后,收集到标准状况下氢气3.36L,此时燃料电池所消耗的CH3OH的质量为:______。
(4)常温下,0.1mol/L NaHCO3溶液的pH大于8,则溶液中C(H2CO3)______ C(CO32-)(填“<”、“>”或“=”)。
-
(6分)工业上常用天然气作为制备CH3OH的原料。已知:
①CH4(g)+O2(g) CO(g)+H2(g)+H2O(g) △H=-321.5 kJ/mol
CO(g)+H2(g)+H2O(g) △H=-321.5 kJ/mol
②CH4(g)+ H2O(g)  CO(g)+3H2(g) △H=+250.3 kJ/mol
CO(g)+3H2(g) △H=+250.3 kJ/mol
③CO(g)+2H2(g)  CH3OH(g) △H=-90.0 kJ/mol
CH3OH(g) △H=-90.0 kJ/mol
(1)CH4(g)与O2(g)反应生成CH3OH(g)的热化学方程式为_____________。
(2)向V L恒容密闭容器中充入a mol CO与2a mol H2,在不同压强下合成甲醇。CO 的平衡转化率与温度、压强的关系如下图所示:

①压强P1____P2(填“<”、“>”或“=”)
②在100℃、P1压强时,平衡常数为________(用含a、V的代数式表示)。
-
甲醇被称为2l世纪的新型燃料,工业上通过下列反应①和②,用CH4和H2O为原料来制备甲醇。
① CH4(g)+H2O(g)  CO(g)+3H2(g) △H1
CO(g)+3H2(g) △H1
② CO(g)+2H2(g)  CH3OH(g) △H2
CH3OH(g) △H2
将0.20mol CH4和0.30 mol H2O(g)通入容积为10L的密闭容器中,在一定条件下发生反应①,达到平衡时,CH4的转化率与温度、压强的关系如右图。
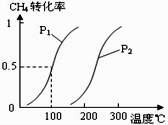
(1)已知在P1、100℃时达到平衡所需的时间为5min,则用CH4表示的平均反应速率为______。
(2)反应①的△H1____0,图中的P1______P2(填“<”、“=”或“>”)。
(3)在压强为0.1MPa条件下,将一定量CO与H2的混合气体在催化剂作用下能自发反应生成甲醇,则反应②的△H2____0,△S____0(填“<”、“=”或“>”)。
(4)根据题中给出的数据,计算反应①在100℃时的平衡常数值____________(写出计算过程及结果)
-
甲醇被称为2l世纪的新型燃料,工业上通过下列反应①和反应②,用CH4和H2O为原料来制备甲醇(CH3OH).
①CH4(g)+H2O(g) CO(g)+3H2(g)△H1
②CO(g)+2H2(g) CH3OH(g)△H2
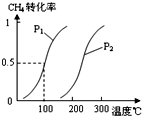
将0.20mol CH4和0.30mol H2O(g)通入容积为10L的密闭容器中,在一定条件下发生①反应,达到平衡时,CH4的转化率与温度、压强的关系如图.
(1)温度不变,缩小体积,增大压强,①的反应速率________(填“增大”、“减小”或“不变”),平衡向________方向移动.
(2)反应①的△H1________0(填“<”、“=”或“>”).
(3)如果反应①达到平衡时所用的时间为2min,求CH4的反应速率及化学平衡常数的值.(写出计算过程).
(4)在100℃压强为0.1MPa条件下,将a mol CO与 3a mol H2的混合气体在催化剂作用下进行②反应,生成甲醇.为了寻找合成甲醇的温度和压强的适宜条件,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中.请在下表空格中填入剩余的实验条件数据.
| 实验编号 | T(℃) | n (CO)/n(H2) | P(MPa) |
| I | 150 |  | 0.1 |
| II | | | 5 |
| III | 350 | | 5 |
-
甲醇被称为2l世纪的新型燃料,工业上通过下列反应①和②,用CH4和H2O为原料来制备甲醇。
① CH4(g)+H2O(g)  CO(g)+3H2(g) ΔH1
CO(g)+3H2(g) ΔH1
② CO(g)+2 H2(g)
H2(g)  CH3OH(g) ΔH2
CH3OH(g) ΔH2
将0.20mol CH4(g)和0.30 mol H2O(g)通入容积为10L的密闭容器中,在一定条件下发生反应①,达到平衡时,CH4的转化率与温度、压强的关系如图。
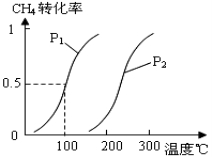
(1)温度不变,缩小体积,增大压强,①的反应速率 ______(填“增大”、“减小”或“不变”),平衡向 ___方向移动。
(2)温度升高,反应①的ΔH1 0(填“<”、“=”或“>”),其平衡常数表达式为K= ,100℃时的平衡常数值是 ______。
(3)在压强为0.1 MPa条件下, 将a mol CO与 3 a mol H2的混合气体在催化剂作用下进行反应②生成甲醇。为了寻找合成甲醇的温度和压强的适宜条件,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。请在下表空格中填入剩余的实验条件数据。
| 实验编号 | T(℃) | n (CO)/n(H2) | P(MPa) |
| I | 150 | 1/3 | 0.1 |
| II | | | 5 |
| III | 350 | | 5 |
-
二甲醚(CH3OCH3)和甲醇(CH3OH)被称为21世纪的新型燃料.以CH4和H2O为原料制备二甲醚和甲醇的工业流程如图1:

请填空:
(1)在一定条件下,反应室1中发生反应:
CH4(g)+H2O(g)⇌CO(g)+3H2(g)△H>0.
在其它条件不变的情况下降低温度,逆反应速率将______ (填“增大”、“减小”或“不变”).将1.0molCH4和2.0molH2O通入反应室1(假设容积为10L),1min末有0.1molCO生成,则1min内反应的平均速率v(H2)=______mol•L-1•min-1.
(2)在压强为0.1MPa条件下,反应室3(容积为2L)中0.2molCO与0.4molH2在催化剂作用下反应生成甲醇:CO(g)+2H2(g)⇌CH3OH(g),CO的平衡转化率与温度、压强的关系如图二所示,则:
①P1______P2 (填“<”、“>”或“=”).
②在P1压强下,100℃时,反应CO(g)+2H2(g)⇌CH3OH(g)的平衡常数K的值为______若温度不变,再加入1.0molCO后重新达到平衡,则CO的转化率______(填“增大”、“不变”或“减小”)
③在其它条件不变的情况下,反应室3再增加0.2molCO与0.4molH2,达到新平衡时,CO的转化率______(填“增大”、“不变”或“减小”)
-
(2013秋•兰山区期中)二甲醚(CH3OCH3)和甲醇(CH3OH)被称为21世纪的新型燃料.以CH4和H2O为原料制备二甲醚和甲醇的工业流程如下:
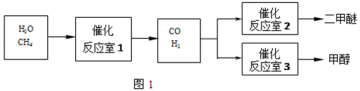
请填空:
(1)一定条件下,反应室1中发生反应CH4(g)+H2O(g)═CO(g)+3H2(g)△H>0.其它条件不变,只降低温度,逆反应速率将 (填“增大”、“减小”或“不变”).
(2)图1中反应室3(容积可变的密闭容器)中0.2mol CO与0.4mol H2在催化剂作用下发生可逆反应生成甲醇:CO(g)+2H2(g) CH3OH(g),CO的平衡转化率与温度、压强的关系如图2所示,则:
CH3OH(g),CO的平衡转化率与温度、压强的关系如图2所示,则:

①P1 P2 (填“<”、“>”或“=”).
②在压强P1下,100℃时反应达到化学平衡,反应室3的容积变为2L,此时CO平衡常为 , 若温度不变,再加入1.0mol CO后重新达到平衡,CO的平衡转化率 (填“增大”、“不变”或“减小”).
③保持容积为2L不变,温度100℃不变,向反应室3中再通入0.2mol CO与0.4mol H2,CO的平衡转化率 (填“增大”、“不变”或“减小”).
-
(6分)甲醇(CH3OH)和二甲醚(CH3OCH3)被称为21世纪的新型燃料。以CH4和H2O为原料制备甲醇和二甲醚的工业流程如下:
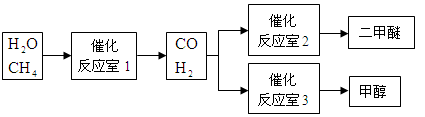
根据要求回答下列问题:
(1)“反应室1”在一定条件下反应的化学方程式为 。
(2)水煤气合成二甲醚的三步反应如下:
①2H2(g)+CO(g) CH3OH(g) ΔH= -90.8kJ·mol-1
CH3OH(g) ΔH= -90.8kJ·mol-1
②2CH3OH(g) CH3OCH3(g)+H2O(g) ΔH= -23.5kJ·mol-1
CH3OCH3(g)+H2O(g) ΔH= -23.5kJ·mol-1
③CO(g)+H2O(g) CO2(g)+H2(g) ΔH= -41.3kJ·mol-1
CO2(g)+H2(g) ΔH= -41.3kJ·mol-1
完成热化学反应方程式:3H2(g)+3CO(g) CH3OCH3(g)+CO2(g);ΔH= 。
CH3OCH3(g)+CO2(g);ΔH= 。
-
(6分)甲醇(CH3OH)和二甲醚(CH3OCH3)被称为21世纪的新型燃料。以CH4和H2O为原料制备甲醇和二甲醚的工业流程如下:
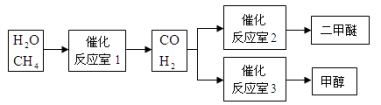
根据要求回答下列问题:
(1)“反应室1”在一定条件下反应的化学方程式为 。
(2)水煤气合成二甲醚的三步反应如下:
①2H2(g)+CO(g) CH3OH(g) ΔH = -90.8kJ·mol-1
CH3OH(g) ΔH = -90.8kJ·mol-1
②2CH3OH(g) CH3OCH3(g)+H2O(g) ΔH = -23.5kJ·mol-1
CH3OCH3(g)+H2O(g) ΔH = -23.5kJ·mol-1
③CO(g)+H2O(g) CO2(g)+H2(g) ΔH = -41.3kJ·mol-1
CO2(g)+H2(g) ΔH = -41.3kJ·mol-1
完成热化学反应方程式:3H2(g)+3CO(g) CH3OCH3(g)+CO2(g);ΔH = 。
CH3OCH3(g)+CO2(g);ΔH = 。
(3)某科研机构研制的一种新型的质子交换膜二甲醚燃料电池(DDFC),该电池有较高的安全性。该电池总反应为CH3OCH3+3O2=2CO2+3H2O,其工作原理如图所示。
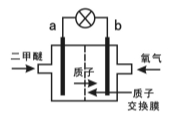
电极a的电极反应式为 。
-
甲醇是一种重要的化工原料,在生产中有着重要的应用。工业上用天然气为原料,分为两阶段制备甲醇:
(ⅰ)制备合成气:CH4(g)+H2O(g) CO(g)+3H2(g)
CO(g)+3H2(g) 
(ⅱ)合成甲醇:CO(g)+2H2(g) CH3OH(g)
CH3OH(g) 
请回答下列问题:
(1)制备合成气:将1.0mol CH4和2.0mol H2O(g)通入反应室(容积为100L),在一定条件下发生反应(i);CH4的平衡转化率与温度、压强的关系如图所示。
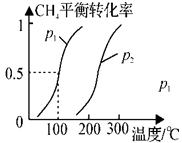
①已知100℃时达到平衡的时间为5min,则从反应开始到平衡,用氢气表示的平均反应速率为:v(H2)= 。
100℃时该反应的平衡常数K= ;若升高温度,平衡常数K将 (填“增大”、“减小”或“不变”)。
②图中p1 p2(填“<”、”“>”或“=”)。
③为解决合成气中H2过量而CO不足的问题,原料气中需添加CO2,发生反应如下:CO2(g)+H2(g) CO(g)+H2O(g),为了使合成气配比最佳,理论上原料气中甲烷与二氧化碳体积比为 。
CO(g)+H2O(g),为了使合成气配比最佳,理论上原料气中甲烷与二氧化碳体积比为 。
(2)合成甲醇:在Cu2O/ZnO作催化剂的条件下,向2L的密闭容器中通入1mol
CO(g)和2mol H2(g),发生反应(ⅱ)。
①反应(ⅱ)需在 (填“高温”或“低温”)才能自发进行。
②据研究,反应过程中起催化作用的为Cu2O,反应体系中含少量的CO2 有利于维持Cu2O的量不变,原因是_________________(用化学方程式表示)。











