-
NO、NO2是大气污染物,但只要合理利用,NO、NO2也是重要的资源。回答下列问题:
(1)氨的合成。已知:N2和H2生成NH3的反应为: N2(g)+
N2(g)+ H2(g)
H2(g) NH3(g) ΔH=-46.2kJ·mol-1
NH3(g) ΔH=-46.2kJ·mol-1
在Fe催化剂作用下的反应历程为(※表示吸附态):
化学吸附:N2(g)→2N※;H2(g) 2H※;
2H※;
表面反应:N※+H※ NH※;NH※+H※
NH※;NH※+H※ NH2※;NH2※+H※
NH2※;NH2※+H※ NH3※;
NH3※;
脱附:NH3※ NH3(g)
NH3(g)
其中N2的吸附分解反应活化能高、速率慢,决定了合成氨的整体反应速率。则利于提高合成氨平衡产率的条件有(________)
A.低温 B.高温 C.低压 D.高压 E.催化剂
(2)NH3还原法可将NO还原为N2进行脱除。已知:
①4NH3(g)+3O2(g)=2N2(g)+6H2O(g) ΔH1=-1530kJ·mol-1
②N2(g)+O2(g)=2NO(g) ΔH2=+180kJ·mol-1
写出NH3还原NO的热化学方程式__。
(3)亚硝酰氯(ClNO)是合成有机物的中间体。将一定量的NO与Cl2充入一密闭容器中,发生反应:2NO(g)+Cl2(g) 2ClNO(g) △H<0。平衡后,改变外界条件X,测得NO的转化率α(NO)随X的变化如图所示,则条件X可能是__(填字母代号)。
2ClNO(g) △H<0。平衡后,改变外界条件X,测得NO的转化率α(NO)随X的变化如图所示,则条件X可能是__(填字母代号)。

a.温度 b.压强 c. d.与催化剂的接触面积
d.与催化剂的接触面积
(4)在密闭容器中充入4molCO和5molNO发生反应2NO(g)+2CO(g) N2(g)+2CO2(g) △H=-746.5kJ•mol-1,如图甲为平衡时NO的体积分数与温度、压强的关系曲线图。
N2(g)+2CO2(g) △H=-746.5kJ•mol-1,如图甲为平衡时NO的体积分数与温度、压强的关系曲线图。

①温度T1__T2(填“>”或“<”)。
②若反应在D点达到平衡,此时对反应进行升温且同时扩大容器体积使平衡压强减小,则重新达到平衡时,D点应向图中A~G点中的__点移动。
③探究催化剂对CO、NO转化的影响。某研究小组将NO和CO以一定的流速通过两种不同的催化剂进行反应,相同时间内测量逸出气体中NO含量,从而确定尾气脱氮率(即NO的转化率),结果如图乙所示。温度低于200℃时,图中曲线I脱氮率随温度升高而变化不大的主要原因为__;a点__(填“是”或“不是”)对应温度下的平衡脱氮率,说明其理由__。
-
合理利用和转化NO2、SO2、CO、NO等污染性气体是环保领域的重要课题。
(1)用CH4催化还原氮氧化物可以消除氮氧化物污染。已知:
① ;
; ;
;
② ,
, ;
;
③ ,
, ;
;
1 mol CH4(g)与NO2(g)反应生成N2(g)、CO2(g)和H2O(1)的反应热为________。
(2)已知 的反应历程分两步:
的反应历程分两步:
① (快);
(快); ,
, ;
;
② (慢);
(慢); ,
,
一定温度下,反应 达到平衡状态,该反应的平衡常数的表达式K=____(用
达到平衡状态,该反应的平衡常数的表达式K=____(用 表示),反应①的活化能E1与反应②的活化能E2的大小关系为E1____E2(填“>”“<”或“=”)。
表示),反应①的活化能E1与反应②的活化能E2的大小关系为E1____E2(填“>”“<”或“=”)。
(3)用活性炭还原法处理氮氧化物的有关反应为: 。向恒容密闭容器中加入一定量的活性炭和NO,恒温(T℃)时,各物质的浓度随时间的变化如下表:
。向恒容密闭容器中加入一定量的活性炭和NO,恒温(T℃)时,各物质的浓度随时间的变化如下表:
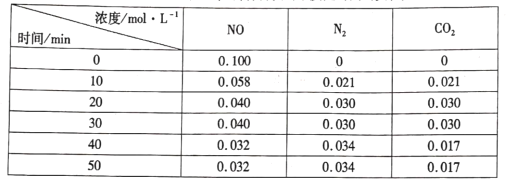
①T℃时,该反应的平衡常数的计算式为______。
②在31 min时,若只改变某一条件使平衡发生移动,40 min、50 min时各物质的浓度如上表所示,则改变的条件是____
③在51 min时,保持温度和容器体积不变再充人NO和N2,使二者的浓度均增加至原来的两倍,此时反应v正____v逆(填“>”、“<”或“=”)。
(4)反应N2O4(g)  2NO2(g) △H>0,在一定条件下N2O4与NO2的消耗速率与各自的分压(分压=总压×物质的量分数)有如下关系:
2NO2(g) △H>0,在一定条件下N2O4与NO2的消耗速率与各自的分压(分压=总压×物质的量分数)有如下关系: ,其中k1、k2是与温度有关的常数,相应的速率与N2O4或NO2的分压关系如图所示。
,其中k1、k2是与温度有关的常数,相应的速率与N2O4或NO2的分压关系如图所示。
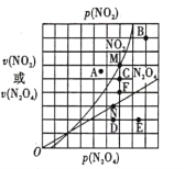
在T℃时,图中M、N点能表示该反应达到平衡状态,理由是___________ 。改变温度,v(NO2)会由M点变为A、B或C,v(N2O4)会由N点变为D、E或F,当升高到某一温度时,反应重新达到平衡,相应的点分别为_______(填字母)。
-
研究NOx、CO、SO2等大气污染气体的治理,对保护环境有重要的意义。回答下列问题:
(1)NOx与CO反应生成无污染气体的相关热化学方程式如下:
①NO2(g)+CO(g) CO2(g)+NO(g) ΔH1=−234.0kJ·mol−1
CO2(g)+NO(g) ΔH1=−234.0kJ·mol−1
②4NO(g) 2NO2(g)+N2(g) ΔH2=−291.8kJ·mol−1
2NO2(g)+N2(g) ΔH2=−291.8kJ·mol−1
反应③2NO2(g)+4CO(g) N2(g)+4CO2(g)的ΔH3=___kJ·mol−1,有利于提高该反应NO2平衡转化率的条件是___(填标号)。
N2(g)+4CO2(g)的ΔH3=___kJ·mol−1,有利于提高该反应NO2平衡转化率的条件是___(填标号)。
A.高温低压 B.低温高压 C.高温高压 D.低温低压
(2)在一定温度下,向2L的恒容密闭容器中充入4.0molNO2和4.0molCO,在催化剂作用下发生反应:2NO2(g)+4CO(g) N2(g)+4CO2(g),测得相关数据如下:
N2(g)+4CO2(g),测得相关数据如下:
| 0min | 5min | 10min | 15min | 20min |
| c(NO2)/mol·L−1 | 2.0 | 1.7 | 1.56 | 1.5 | 1.5 |
| c(N2)/mol·L−1 | 0 | 0.15 | 0.22 | 0.25 | 0.25 |
①其他条件不变,若不使用催化剂,则0~5minNO2的转化率将___(填“变大”、“变小”或“不变”)。
②以下表述能说明该反应已达到平衡状态的是___。
A.CO的反应速率为N2的4倍
B.气体的颜色不再变化
C.化学平衡常数K不再变化
D.混合气的压强不再变化
③该温度下反应的化学平衡常数K=__(保留两位有效数字)。
④在20min时,保持温度不变,继续向容器中再加入2.0molNO2和2.0molN2,则化学平衡__移动(填“正向”、“逆向”或“不”)。
(3)在高效催化剂的作用下用CH4还原NO2,也可消除氮氧化物的污染。
①CH4还原NO2反应的化学方程式为___。
②在相同条件下,选用A、B、C三种不同催化剂进行反应,生成N2的物质的量与时间变化如图图1所示,其中活化能最大的是___[Ea(A)、Ea(B)、Ea(C)分别表示三种催化剂下该反应的活化能]。

③在催化剂A作用下,测得相同时间内处理NO2的量与温度的关系如图2所示,曲线先增大后减小的可能原因是___。
-
研究NO2、SO2、CO等大气污染气体的处理及利用的方法具有重要意义。
(1)一定条件下,NO2与SO2反应生成SO3和NO两种气体。将体积比为1∶2的NO2、SO2气体置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是____________(填字母)。
a. 体系压强保持不变
b. 混合气体颜色保持不变
c. 体系中SO3的体积分数保持不变
d. 每消耗1 mol SO2的同时生成1 mol NO
测得上述反应平衡时NO2与SO2体积比为1∶6,则平衡常数K=____________。
(2)新型氨法烟气脱硫技术的化学原理是采用氨水吸收烟气中的SO2,再用一定量的磷酸与上述吸收产物反应。该技术的优点除了能回收利用SO2外,还能得到一种复合肥料,该复合肥料可能的化学式为________(写出一种即可)。
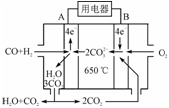
(3)右图是MCFC燃料电池,它是以水煤气(CO、H2)为燃料,一定比例Li2CO3和Na2CO3低熔混合物为电解质。A为电池的________(填“正”或“负”)极,写出B极电极反应式:________________________。
(4)工业上常用Na2CO3溶液吸收法处理氮的氧化物(以NO和NO2的混合物为例)。
已知:NO不能与Na2CO3溶液反应。
NO+NO2+Na2CO3===2NaNO2+CO2
2NO2+Na2CO3===NaNO2+NaNO3+CO2
① 用足量的Na2CO3溶液完全吸收NO和NO2的混合物,每产生22.4 L(标准状况)CO2(全部逸出)时,吸收液质量就增加44 g,则混合气体中NO和NO2的体积比为__________。
② 用Na2CO3溶液吸收法处理氮的氧化物存在的缺点是____________。
-
研究NO2、SO2、CO等大气污染气体的处理及利用的方法具有重要意义。
⑴一定条件下,NO2与SO2反应生成SO3和NO两种气体。将体积比为1∶2的NO2、SO2气体置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是________(填字母)。
a.体系压强保持不变 b.混合气体颜色保持不变
c.体系中SO3的体积分数保持不变 d.每消耗1 mol SO2的同时生成1 mol NO
测得上述反应平衡时NO2与SO2体积比为1∶6,则平衡常数K=________。
⑵新型氨法烟气脱硫技术的化学原理是采用氨水吸收烟气中的SO2,再用一定量的磷酸与上述吸收产物反应。该技术的优点除了能回收利用SO2外,还能得到一种复合肥料,该复合肥料可能的化学式为________(写出一种即可)。
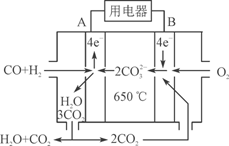
⑶右图是MCFC燃料电池,它是以水煤气(CO、H2)为燃料,一定比例Li2CO3和Na2CO3低熔混合物为电解质。A为电池的________(填“正”或“负”)极,写出B极电极反应式:________________________。
⑷工业上常用Na2CO3溶液吸收法处理氮的氧化物(以NO和NO2的混合物为例)。
已知:NO不能与Na2CO3溶液反应。
NO+NO2+Na2CO3=2NaNO2+CO2
2NO2+Na2CO3=NaNO2+NaNO3+CO2
①用足量的Na2CO3溶液完全吸收NO和NO2的混合物,每产生22.4 L(标准状况)CO2(全部逸出)时,吸收液质量就增加44 g,则混合气体中NO和NO2的体积比为
____________。
②用Na2CO3溶液吸收法处理氮的氧化物存在的缺点是____________。
-
从煤化工行业中可以得到许多重要的工业资源。回答下列问题:
(1)从煤的气化获得的化工原料气中含有的少量羰基硫(COS)会引起催化制中毒,大气污染等问题。
①羰基硫与烧碱溶液反应生成两种正盐的离子方程式为_________________________________。
②羰基硫的脱硫方法之一为COS(g)+H2(g)=H2S(g)+ CO(g) ΔH=+7kJ·mol-1,已知反应中部分物质的键能数据如下:
| 化学键 | C=O | C=S | H-S | H-H |
| 键能(kJ·mol-1) | 745 | 577 | 339 | 436 |
则CO分子中的碳氧键的键能为_________________。
(2)羰基硫在高温下发生水解反应:COS(g)+H2O(g) H2S(g)+CO2(g)。T℃时,将0.30 molCOS(g)与0.50mol H2O(g)充入10L的恒容密闭容器中,30 s后反应达到平衡状态,此时H2S的物质的量分数为0.30。
H2S(g)+CO2(g)。T℃时,将0.30 molCOS(g)与0.50mol H2O(g)充入10L的恒容密闭容器中,30 s后反应达到平衡状态,此时H2S的物质的量分数为0.30。
①0~30 s内,COS的平均反应速率v(COS)=___________,该反应的平衡常数K=__________(保留3位有效数字)。
②向反应容器中再分别充入下列气体,能使COS的转化率增大的是_________(填字母)。
A.COS B.H2O C.H2S D.CO2
(3)将含H2S尾气的空气按一定流速通入酸性FeCl3溶液中,可实现含H2S尾气的空气脱硫。在FeCl3 溶液吸收H2S的过程中,溶液中的n(Fe3+)及被吸收的n(H2S)随时间t的变化如图所示。
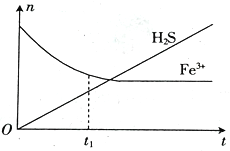
①由图中信息可知,0~t1时间段内,一定发生的反应是__________________________(用离子方程式表示)。
②t1时刻后,溶液中n(Fe3+)保持微量减少至基本不变,其原因是__________________________________。
-
合理处理燃气中的H2S,不仅可减少对大气的污染,还可进行资源化利用。回答下列问题:
(1)H2S和S的燃烧热如表所示,
| 物质 | 燃烧热/△H(kJ•mol-1) |
| H2S | -a |
| S | -b |

请写出常温下H2S与SO2反应的热化学方程式______。
(2)可以把H2S设计为一种燃料电池,原理如图a所示:其中,Fe2+在电池工作中的作用是______;请写出 I室发生的离子方程式______。
(3)为探究H2S的直接热解2H2S(g)=2H2(g )+S2(g)。在一体积为2L的密闭容器中充入2 mol H2S与1 molAr (起到稀释作用),进行实验。
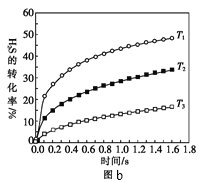
①某同学测出不同温度下H2S的物质的量与反应时间的图象,图b是截取该图象的中间某部分。请计算T2温度下,0-l0s内,H2S的反应速率v=______mo•L-1•s-1;
②图b中,T1、T2、T3三个温度,最高的是______;比较A点与B点的逆反应速率的大小,vA(逆)______vB(逆)(填“>”、“<”或“=”);
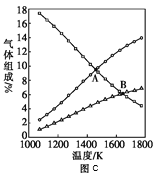
③图c是表示反应2H2S(g)=2H2(g)+S2(g)平衡时,装置内各组分气体物质的量分数=与温度的关系(其中Ar气体变化曲线未画出)。请计算:C点的平衡常数K=______;D点平衡时,H2S的转化率=______。
-
合理处理燃气中的H2S,不仅可减少对大气的污染,还可进行资源化利用。回答下列问题:
(1)H2S和S的燃烧热如表所示,
| 物质 | 燃烧热/△H(kJ•mol-1) |
| H2S | -a |
| S | -b |

请写出常温下H2S与SO2反应的热化学方程式______。
(2)可以把H2S设计为一种燃料电池,原理如图a所示:其中,Fe2+在电池工作中的作用是______;请写出 I室发生的离子方程式______。
(3)为探究H2S的直接热解2H2S(g)=2H2(g )+S2(g)。在一体积为2L的密闭容器中充入2 mol H2S与1 molAr (起到稀释作用),进行实验。
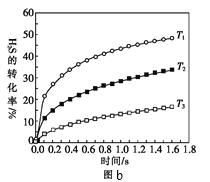
①某同学测出不同温度下H2S的物质的量与反应时间的图象,图b是截取该图象的中间某部分。请计算T2温度下,0-l0s内,H2S的反应速率v=______mo•L-1•s-1;
②图b中,T1、T2、T3三个温度,最高的是______;比较A点与B点的逆反应速率的大小,vA(逆)______vB(逆)(填“>”、“<”或“=”);
③图c是表示反应2H2S(g)=2H2(g)+S2(g)平衡时,装置内各组分气体物质的量分数=与温度的关系(其中Ar气体变化曲线未画出)。请计算:C点的平衡常数K=______;D点平衡时,H2S的转化率=______。
-
氮的氧化物是造成大气污染的主要物质。研究氮氧化物的反应机理对于消除环境污染有重要意义。回答下列问题:
(1)已知:2NO2(g)= N2O4(g) △H=-55.3kJ/mol
N2O5(g)=2NO2(g)+ O2(g) △H=+53.1 kJ/mol
O2(g) △H=+53.1 kJ/mol
则:N2O5(g)=N2O4(g)+ O2(g) △H=___________ kJ/mol
O2(g) △H=___________ kJ/mol
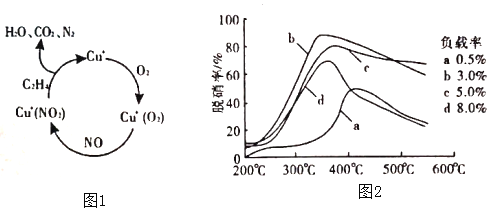
(2)以乙烯(C2H4)作为还原剂脱硝(NO),脱硝机理如图1。若反应中n(NO)︰n(O2)=2︰1,则总反应的化学方程式为___________;脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如图2,为达到最佳脱硝效果,应采用的条件是___________。
(3)T1温度时在容积为2L的恒容密闭容器中发生反应:2NO(g)+O2(g) 2NO2(g) △H<0。实验测得:υ正=υ(NO)消耗=2υ(O2)消耗=k正c2(NO)·c(O2),υ逆=(NO2) 消耗=k逆c2(NO2),k正、k逆为速率常数只受温度影响。不同时刻测得容器中n(NO)、n(O2)如表:
2NO2(g) △H<0。实验测得:υ正=υ(NO)消耗=2υ(O2)消耗=k正c2(NO)·c(O2),υ逆=(NO2) 消耗=k逆c2(NO2),k正、k逆为速率常数只受温度影响。不同时刻测得容器中n(NO)、n(O2)如表:

①从0~2s内该反应的平均速率υ(NO)=___________mol/(L·s)。
②T1温度时化学平衡常数K=___________ L/mol。 (结果保留3位有效数字)。
③化学平衡常数K与速率常数k正、k逆的数学关系是K=___________。若将容器的温度改变为T2时其k正=k逆,则T2___________T1(填“>”、“<”或“=")。
④已知2NO(g)+O2(g) 2NO2的反应历程为:
2NO2的反应历程为:
第一步NO+NO N2O2 快速反应 第二步N2O2+O2→2NO2 慢反应
N2O2 快速反应 第二步N2O2+O2→2NO2 慢反应
下列叙述正确的是___________(填标号)。
A. υ(第一步的正反应)< υ(第二步的反应) B.总反应快慢由第二步决定
C.第二步的活化能比第一步的高 D.第二步中N2O2与O2的碰撞100%有效
-
NOx、SO2、CO等大气污染物的处理及利用在工业上具有重要意义。
(l)一定条件下,NO2 与SO2反应生成SO3和NO两种气体。将体积比为l: 1 的NO2 和SO2气体置于恒容密闭容器中发生上述反应,下列能说明该反应达到化学平衡状态的是____(填字母)。
a.混合气休平均摩尔质量不变 b.混合气休颜色保持不变
c.每消耗1 molSO2的同时生成1 mol NO d.容器内的气体密度不变
(2)燃煤锅炉将排放大量SO2,污染大气造成公害,常采用下列两种方法消除燃煤SO2的污染。使排放的烟气通过足量的浓氨水洗涤,化学方程式是_________。在煤中加适量生石灰,使SO2 与生石灰反应,化学方程式为_______。
(3)工业处理CO的其中一种方法是利用H2O(g)+ CO(g) H2(g)+CO2(g)△H<0来制备氢气。已知在恒容体系内发生此反应,某温度下该反应的平衡常数K=1。若起始时c(CO)= l mol/L,c(H2O)= 2 mol/L。
H2(g)+CO2(g)△H<0来制备氢气。已知在恒容体系内发生此反应,某温度下该反应的平衡常数K=1。若起始时c(CO)= l mol/L,c(H2O)= 2 mol/L。
试回答下列问题:
① 该温度下,反应进行一段时间后,测得H2O的浓度为1.6 mol/L ,则此时该反应v (正)___ v(逆)(填“>”“<”或“=”);若在平衡建立之后,向体系内通入一定量的Ar, H2的平衡产率将____(填“增大”“减小”或“不变”)。
② 上述反应生成的H2与CO2可以设计成原电池来合成CH3OH,装置如图所示:
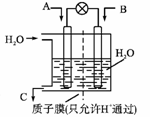
若A为CO2, B为H2 , C 为CH3OH,则通入CO2的一极为_____极;
若A改为SO2, B为O2, C 为H2SO4,则正极的电极反应式为____________。
(4)已知在催化转化装置内,汽车尾气中的NO、CO能发生如下反应:
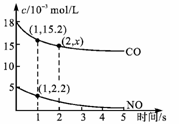
2NO(g)+2CO(g)  N2(g)+2CO2(g) △H=-746.8KJ/mol, 利用传感器记录某温度下上述反应的进程,测量所得数据如图。已知达到平衡时NO的转化率为80%,则该反应的平衡常数为____(保留小数点后一位小数)
N2(g)+2CO2(g) △H=-746.8KJ/mol, 利用传感器记录某温度下上述反应的进程,测量所得数据如图。已知达到平衡时NO的转化率为80%,则该反应的平衡常数为____(保留小数点后一位小数)
N2(g)+
H2(g)
NH3(g) ΔH=-46.2kJ·mol-1
2H※;
NH※;NH※+H※
NH2※;NH2※+H※
NH3※;
NH3(g)
2ClNO(g) △H<0。平衡后,改变外界条件X,测得NO的转化率α(NO)随X的变化如图所示,则条件X可能是__(填字母代号)。

d.与催化剂的接触面积
N2(g)+2CO2(g) △H=-746.5kJ•mol-1,如图甲为平衡时NO的体积分数与温度、压强的关系曲线图。
















