-
煤气化和液化是现代能源工业中重点考虑的能源综合利用方案。最常见的气化方法为用煤生产水煤气,而当前比较流行的液化方法为用煤生产CH 3OH。已知制备甲醇的有关化学反应及平衡常数如下:①CO 2(g)+3H 2(g)=CH 3OH(g)+H 2 O(g) Δ H 1 =-90.8KJ/mol,②CO(g)+H2O(g)=CO2(g)+H2(g) Δ H 2 =-41.2kJ/mol,③CO(g)+2H2(g)=CH3OH(g)Δ H 3 850 ℃平衡常数分别为k1=160, K2=243,K3=160,甲醇可以与乙酸反应制香料CH 3OH(l)+CH3COOH(l) CH3COOCH3(l)+H2O(l)
CH3COOCH3(l)+H2O(l)
(1)则反应Δ H 3= ___________ 制香料的K的表达式_____________
(2)由CO合成甲醇时,以下有关该反应的说法正确的是________(填序号)。
A.恒温、恒容条件下,若容器内的压强不发生变化,则可逆反应达到平衡
B.一定条件下,H 2 的消耗速率是CO的消耗速率的2倍时,可逆反应达到平衡
C.使用合适的催化剂能缩短达到平衡的时间并提高CH 3OH的产率
D.某温度下,将2 mol CO和6 mol H 2 充入2 L密闭容器中,充分反应,达到平衡后,测得c (CO)=0.2 mol·L - 1 ,则CO的转化率为80%
(3)850 ℃时,在密闭容器中进行反应①开始时只加入CO2 、H 2,反应10min后测得各组分的浓度如下比较正逆反应的速率的大小:
v正 __________ v逆(填“>、<或=”) 该时间段内反应速率v(H2)= __________
| 物质 | H 2 | CO 2 | CH 3 OH | H 2 O |
| 浓度(mol/L) | 0.2 | 0.2 | 0.4 | 0.4 |
(4)在一定条件下3L恒容密闭容器中,充入一定量的H2和CO2仅发生反应①,实验测得反应物在不同起始投入量下,反应体系中CO2的平衡转化率与温度的关系曲线,如图1所示。
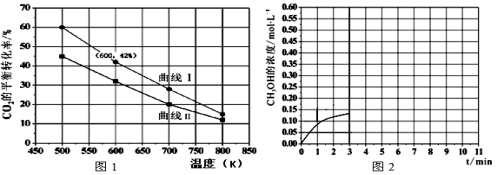
①H2和CO2的起始的投入量以A和B两种方式投入
A:n(H2)=3mol,n(CO2)=1.5mol
B:n(H2)=3mol,n(CO2)=2mol,曲线I代表哪种投入方式____(用A、B表示)
②在温度为500K的条件下,按照A方式充入3mol H2和1.5mol CO2,该反应10min时达到平衡,在此条件下,系统中CH3OH的浓度随反应时间的变化趋势如图2所示,当反应时间达到3min时,迅速将体系温度升至600K,请在图2中画出3~10min内容器中CH3OH浓度的变化趋势曲线___。
-
煤气化和液化是现代能源工业中重点考虑的能源综合利用方案。最常见的气化方法为用煤生产水煤气,而当前比较流行的液化方法为用煤生产CH3OH。
(1)已知:CO2(g)+3H2(g)===CH3OH(g)+H2O(g) ΔH1
2CO(g)+O2(g)===2CO2(g) ΔH2
2H2(g)+O2(g)===2H2O(g) ΔH3
则反应CO(g)+2H2(g)===CH3OH(g)的ΔH=______。
(2)如图是该反应在不同温度下CO的转化率随时间变化的曲线。
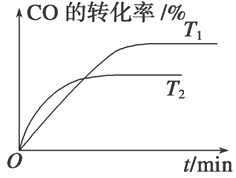
①T1和T2温度下的平衡常数大小关系是K1________K2(填“>”、“<”或“=”)。
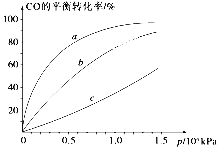
②由CO合成甲醇时,CO在250 ℃、300 ℃、350 ℃下达到平衡时转化率与压强的关系曲线如下图所示,则曲线c所表示的温度为________ ℃。实际生产条件控制在250 ℃、1.3×104 kPa左右,选择此压强的理由是____________。
③以下有关该反应的说法正确的是________(填序号)。
A.恒温、恒容条件下,若容器内的压强不再发生变化,则可逆反应达到平衡
B.一定条件下,H2的消耗速率是CO的消耗速率的2倍时,可逆反应达到平衡
C.使用合适的催化剂能缩短达到平衡的时间并提高CH3OH的产率
D.某温度下,将2 mol CO和6 mol H2充入2 L密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2 mol·L-1,则CO的转化率为80%
(3)一定温度下,向2 L固定体积的密闭容器中加入1 mol CH3OH(g),发生反应:CH3OH(g)  CO(g)+2H2(g),H2的物质的量随时间变化的曲线如图所示。
CO(g)+2H2(g),H2的物质的量随时间变化的曲线如图所示。
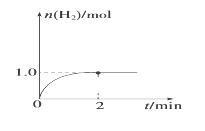
0~2 min内的平均反应速率v(CH3OH)=__________。该温度下,反应CO(g)+2H2(g)  CH3OH(g)的平衡常数K=__________。相同温度下,在一个恒容容器中加入一定量的CO(g)和H2发生:CO(g)+2H2(g)
CH3OH(g)的平衡常数K=__________。相同温度下,在一个恒容容器中加入一定量的CO(g)和H2发生:CO(g)+2H2(g)  CH3OH(g)的反应,某时刻测得体系中各物质的量浓度如下:C(CO)=0.25 mol·L-1,C(H2)=1.0 mol·L-1,C(CH3OH)=0.75 mol·L-1,则此时该反应_____进行(填“向正反应方向”“向逆反应方向”或“处于平衡状态”)。
CH3OH(g)的反应,某时刻测得体系中各物质的量浓度如下:C(CO)=0.25 mol·L-1,C(H2)=1.0 mol·L-1,C(CH3OH)=0.75 mol·L-1,则此时该反应_____进行(填“向正反应方向”“向逆反应方向”或“处于平衡状态”)。
-
煤气化和液化是现代能源工业中重点考虑的能源综合利用方案。最常见的气化方法为用煤生产水煤气,而当前比较流行的液化方法为用煤生产CH3OH。
(1)已知:CO2(g)+3H2(g)===CH3OH(g)+H2O(g) ΔH1
2CO(g)+O2(g)===2CO2(g) ΔH2
2H2(g)+O2(g)===2H2O(g) ΔH3
则反应CO(g)+2H2(g)===CH3OH(g)的ΔH=______。
(2)如图是该反应在不同温度下CO的转化率随时间变化的曲线。
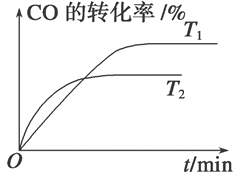
①T1和T2温度下的平衡常数大小关系是K1________K2(填“>”、“<”或“=”)。
②由CO合成甲醇时,CO在250 ℃、300 ℃、350 ℃下达到平衡时转化率与压强的关系曲线如下图所示,则曲线c所表示的温度为________ ℃。实际生产条件控制在250 ℃、1.3×104 kPa左右,选择此压强的理由是____________。
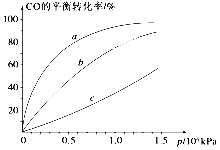
③以下有关该反应的说法正确的是________(填序号)。
A.恒温、恒容条件下,若容器内的压强不再发生变化,则可逆反应达到平衡
B.一定条件下,H2的消耗速率是CO的消耗速率的2倍时,可逆反应达到平衡
C.使用合适的催化剂能缩短达到平衡的时间并提高CH3OH的产率
D.某温度下,将2 mol CO和6 mol H2充入2 L密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2 mol·L-1,则CO的转化率为80%
(3)一定温度下,向2 L固定体积的密闭容器中加入1 mol CH3OH(g),发生反应:CH3OH(g)  CO(g)+2H2(g),H2的物质的量随时间变化的曲线如图所示。
CO(g)+2H2(g),H2的物质的量随时间变化的曲线如图所示。
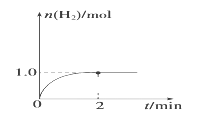
0~2 min内的平均反应速率v(CH3OH)=__________。该温度下,反应CO(g)+2H2(g)  CH3OH(g)的平衡常数K=__________。相同温度下,在一个恒容容器中加入一定量的CO(g)和H2发生:CO(g)+2H2(g)
CH3OH(g)的平衡常数K=__________。相同温度下,在一个恒容容器中加入一定量的CO(g)和H2发生:CO(g)+2H2(g)  CH3OH(g)的反应,某时刻测得体系中各物质的量浓度如下:C(CO)=0.25 mol·L-1,C(H2)=1.0 mol·L-1,C(CH3OH)=0.75 mol·L-1,则此时该反应_____进行(填“向正反应方向”“向逆反应方向”或“处于平衡状态”)。
CH3OH(g)的反应,某时刻测得体系中各物质的量浓度如下:C(CO)=0.25 mol·L-1,C(H2)=1.0 mol·L-1,C(CH3OH)=0.75 mol·L-1,则此时该反应_____进行(填“向正反应方向”“向逆反应方向”或“处于平衡状态”)。
-
煤气化和液化是现代能源工业中重点考虑的能源综合利用方案。最常见的气化方法为用煤生产水煤气,而当前比较流行的液化方法为用煤生产CH3OH。
(1)已知:CO2(g)+3H2(g)=CH3OH(g)+H2O(g)△H1
2CO(g)+O2(g)=2CO2(g)△H2
2H2(g)+O2(g)=2H2O(g)△H3
则反应CO(g)+2H2(g)=CH3OH(g)的△H=_____。
(2)如图是该反应在不同温度下CO的转化率随时间变化的曲线。
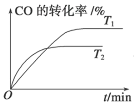
①T1和T2温度下的平衡常数大小关系K1_____K2是不后填“>”、“<”或“=”)。
②由CO合成甲醇时,CO在250℃、300℃、350℃下达到平衡时转化率与压强的关系曲线如下图所示,则曲线c所表示的温度为_____℃。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是_____。
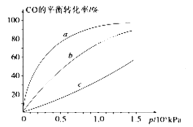
③以下有关该反应的说法正确的是_____(填序号)
A.恒温、恒容条件下,若容器内的压强不再发生变化,则可逆反应达到平衡
B.一定条件下,H2的消耗速率是CO的消耗速率的2倍时,可逆反应达到平衡。
C.使用合适的催化剂能缩短达到平衡的时间并提高CH3OH的产率。
D.某温度下,将2mo1CO和6molH2充入2L密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2mol·L-1,则CO的转化率为80%
(3)一定温度下,向2L固定体积的密闭容器中加入1molCH3OH(g),发生反应:CH3OH(g) CO(g)+2H2(g),H2的物质的量随时间变化的曲线如图所示。
CO(g)+2H2(g),H2的物质的量随时间变化的曲线如图所示。
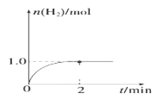
0~2min内的平均反应速率v(CH3OH)=_____。该温度下,反应CO(g)+2H2(g) CH3OH(g)的平衡常数K=_____。相同温度下,在一个恒容容器中加入一定量的CO和H2,发生反应2H2(g)+CO(g)=CH3OH(g)的平衡常数K=_____.相同温度下,若开始时加入CH3OH(g)的物质的量是原来的2倍,则____是原来的2倍。
CH3OH(g)的平衡常数K=_____。相同温度下,在一个恒容容器中加入一定量的CO和H2,发生反应2H2(g)+CO(g)=CH3OH(g)的平衡常数K=_____.相同温度下,若开始时加入CH3OH(g)的物质的量是原来的2倍,则____是原来的2倍。
A.平衡常数 B. CH3OH的平衡浓度 C.达到平衡的时间 D.平衡时气体的密度
-
煤气化和液化是现代能源工业中重点考虑的能量综合利用方案。最常见的气化方法为用煤生成水煤气,而当前比较流行的液化方法用煤生成CH3OH。
(1)已知:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) △H1
2CO(g)+O2(g)=2CO2(g) △H2
2H2(g)+O2(g)=2H2O(g) △H3
则反应CO(g) +2H2(g)=CH3OH(g) 的△H=_______。
(2)如图是该反应在不同温度下CO的转化率随时间变化的曲线。
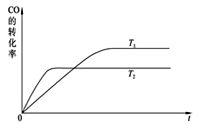
①T1和T2温度下平衡常数大小关系是K1____K2(填“>”“<”或“=”)。
②由CO合成甲醇时,CO在250℃、300℃、350℃下达到平衡时转化率与压强的关系曲线如下图所示,则曲线c所表示的温度为______℃,实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是______。
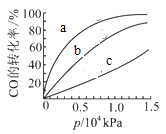
③以下有关该反应的说法正确的是_________(填序号)。
A.恒温、恒容条件下同,若容器内的压强不发生变化,则可逆反应达到平衡
B.一定条件下,H2的消耗速率是CO的消耗速率的2倍时,可逆反应达到平衡
C.使用合适的催化剂能缩短达到平衡的时间并提高CH3OH的产率
D.某温度下,将2molCO和6molH2充入2L密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2mol/L,则CO的转化率为80%
(3)一定温度下,向2L固定体积的密闭容器中加入1molCH3OH,发生反应:CH3OH(g)  CO(g) +2H2(g),H2的物质的量随时间变化的曲线如图所示。
CO(g) +2H2(g),H2的物质的量随时间变化的曲线如图所示。

0~2min内的平均反应速率v(CH3OH)= ____________;该温度下,CO(g)+2H2(g) CH3OH(g)的平衡常数K=____________;相同温度下,若开始加入CH3OH(g)的物质的量是原来的2倍,则_____ 是原来的2倍.
CH3OH(g)的平衡常数K=____________;相同温度下,若开始加入CH3OH(g)的物质的量是原来的2倍,则_____ 是原来的2倍.
A.平衡常数 B.CH3OH的平衡浓度 C.达到平衡的时间 D.平衡时气体的密度
-
下列有关资源综合利用的说法不正确的是( )
A.煤的气化、液化均为化学变化,而石油的常压蒸馏和减压蒸馏均是物理变化
B.绿色化学的核心就是利用化学原理吸收处理工业生产污染物并将其转化为有用物质
C.利用石油的裂化可以提高汽油的产量和质量
D.将苦卤水浓缩、氧化,鼓入空气和水蒸气可提取溴
-
阅读短文,回答问题。
2017年9月第六届中国国际煤化工发展论坛上,中国石油和化学工业联合会会长总结介绍了我国煤气化、煤液化、煤制烯烃等现代煤化工技术创新成就。燃煤产生的二氧化碳作为温室气体为人熟知,其实二氧化碳是一种被误解、误判的资源。此次论坛上,很多科研机构也在二氧化碳的相关研究方面做了交流。如二氧化碳加氢制甲醇技术和二氧化碳加氢直接合成液体燃料的研究;合成的一种新型催化剂,首次实现了二氧化碳直接高选择性合成汽油烃类组分,成果被Nature Chemistry杂志发表,被认为是二氧化碳转化领域的一大突破,为二氧化碳转化为化学品及燃料提供了重要平台。
请依据以上短文,判断下列说法是否正确(填“对”或“错”)。
(1)以煤为原料可以制得烯烃。______
(2)二氧化碳加氢制甲醇是物理变化。______
(3)二氧化碳直接高选择性合成汽油烃类组分需要使用催化剂。_____。
(4)二氧化碳转化为化学品标志着该技术向工业化迈出了坚实一步。______
-
迄今为止,煤、石油和天然气仍是人类使用的主要能源。对化石燃料的综合利用不仅节约能源,同时还防止环境污染,关于化石燃料的综合利用叙述错误的是( )
A.煤的气化和液化是物理变化
B.石油的裂化为了提高轻质油的产量和质量
C.石油的裂解为了得到短链烃
D.天然气的主要成分是甲烷,合理的开发为人类提供能源
-
化学与社会、生产、生活密切相关,下列说法不正确的是
A. 煤的气化、液化和干馏都是化学变化,是实现煤的综合利用的有效途径
B. 海水淡化可以解决淡水危机,用光催化分解代替电解水制氢气可实现节能环保
C. 我国油品从国IV汽油升级到国V汽油,有助于减少酸雨、雾霾,提高空气质量
D. 天然气、沼气和太阳能分别属于化石能源、可再生能源和二次能源
-
工业上,煤的气化和液化是高效、清洁、综合利用煤炭的重要途径。
(1)一定条件下,将C(s)和H2O(g)分别加入甲、乙两个密闭容器发生反应:C(s)+2H2O(g) CO2(g)+2H2(g) ΔH1>0,相关数据如下表:
CO2(g)+2H2(g) ΔH1>0,相关数据如下表:
| 容器 | 容积/L | 温度/℃ | 起始量/mol | 平衡量/mol |
| C(s) | H2O(g) | H2(g) |
| 甲 | 2 | T1 | 3 | 4 | 3.2 |
| 乙 | 1 | T2 | 1.5 | 2 | 1.2 |
①T1___T2(填“>、<或=”)。
②T1时达到平衡后再加入1molH2O(g),达到新平衡后H2(g)的物质的量分数___(填“增大”“不变”或“减小”);T2时,若起始时乙容器中加入1.5molC(s)、1.2molH2O(g)、0.5molCO2(g)、1.4molH2(g),此时v正___v逆(填“>、<或=”)。
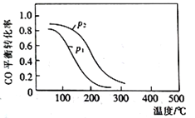
(2)煤液化时发生反应:CO(g)+2H2(g) CH3OH(g)ΔH2,在10L恒容密闭容器中按物质的量之比1:2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如图所示,200℃时,n(H2)随时间的变化如下表所示:
CH3OH(g)ΔH2,在10L恒容密闭容器中按物质的量之比1:2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如图所示,200℃时,n(H2)随时间的变化如下表所示:
| t/min | 0 | 1 | 3 | 5 |
| n(H2)/mol | 8.0 | 5.4 | 4.0 | 4.0 |
①ΔH2___0(填“>、<或=”)。
②下列说法正确的是___(填标号)。
a.温度越高,该反应的平衡常数越大
b.达平衡后再充入稀有气体,CO的转化率提高
c.容器内气体压强不再变化时,反应达到最大限度
d.图中压强P1<P2
③0-3min内用CH3OH表示的反应速率v(CH3OH)=___mol/(L·min)(结果保留两位有效数值)。
④200℃时,该反应的平衡常数K=___。向上述200℃达到平衡的恒容密闭容器中再加入2molCO、2molH2、2molCH3OH,保持温度不变,则化学平衡___(填“正向”、“逆向”或“不”)移动。


CO(g)+2H2(g),H2的物质的量随时间变化的曲线如图所示。

CH3OH(g)的平衡常数K=_____。相同温度下,在一个恒容容器中加入一定量的CO和H2,发生反应2H2(g)+CO(g)=CH3OH(g)的平衡常数K=_____.相同温度下,若开始时加入CH3OH(g)的物质的量是原来的2倍,则____是原来的2倍。










