已知:p[]=-lg[
]。室温下,向0.10 mol/L HX溶液中滴加0.10 mol/LNaOH溶液,溶液pH随p[
]变化关系如图所示。下列说法正确的是
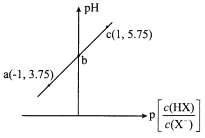
A.溶液中水的电离程度:a>b>c
B.c点溶液中:c(Na+)=10c(HX)
C.室温下NaX的水解平衡常数为10-4.75
D.图中b点坐标为(0,4.75)
高三化学单选题中等难度题
已知:p[]=-lg[
]。室温下,向0.10 mol/L HX溶液中滴加0.10 mol/LNaOH溶液,溶液pH随p[
]变化关系如图所示。下列说法正确的是

A.溶液中水的电离程度:a>b>c
B.c点溶液中:c(Na+)=10c(HX)
C.室温下NaX的水解平衡常数为10-4.75
D.图中b点坐标为(0,4.75)
高三化学单选题中等难度题
已知:p[]=-lg[
]。室温下,向0.10 mol/L HX溶液中滴加0.10 mol/LNaOH溶液,溶液pH随p[
]变化关系如图所示。下列说法正确的是

A.溶液中水的电离程度:a>b>c
B.c点溶液中:c(Na+)=10c(HX)
C.室温下NaX的水解平衡常数为10-4.75
D.图中b点坐标为(0,4.75)
高三化学单选题中等难度题查看答案及解析
已知:p[]=-lg[
]。室温下,向0.10 mol/L HX溶液中滴加0.10 mol/LNaOH溶液,溶液pH随p[
]变化关系如图所示。下列说法正确的是
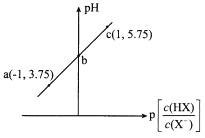
A.溶液中水的电离程度:a>b>c
B.c点溶液中:c(Na+)=10c(HX)
C.室温下NaX的水解平衡常数为10-4.75
D.图中b点坐标为(0,4.75)
高三化学单选题中等难度题查看答案及解析
室温下,向20.00 mL 0.10 mol·L−1一元弱碱MOH溶液中滴入0.10 mol·L−1的盐酸,溶液的AG与所加盐酸的体积关系如图所示,已知AG = lg 。
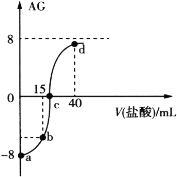
下列有关叙述不正确的是( )
A.50℃下,AG=0,此时溶液显中性
B.a点对应溶液中H2O电离出的c(H+)=1.0×10−11 mol·L−1
C.b点对应溶液中 4c(M+)+4c(MOH)=3c(Cl−)
D.d点对应溶液中c(Cl−)>c(H+)> c(M+)>c(MOH)
高三化学单选题中等难度题查看答案及解析
室温下,将 0.10 mol·L-1 盐酸滴入 20.00 mL 0.10 mol·L-1 氨水中,溶液中 pH 和 pOH 随加入盐酸体积变化曲线如图所示。已知:pOH=-lg c(OH-),下列正确的是
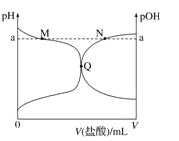
A. M 点所示溶液中可能存在c(Cl-)> c(NH4+)
B. N 点所示溶液中可能存在:c (NH4+)+ c(NH3﹒H2O)= c(Cl-)
C. Q 点盐酸与氨水恰好中和
D. M 点到Q点所示溶液中水的电离程度先变大后减小
高三化学单选题困难题查看答案及解析
室温下,将 0.10 mol·L-1 盐酸滴入 20.00 mL 0.10 mol·L-1 氨水中,溶液中 pH 和 pOH 随加入盐酸体积变化曲线如图所示。已知:pOH=-lg c(OH-),下列正确的是
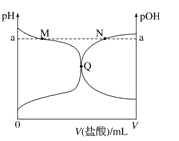
A. M 点所示溶液中可能存在c(Cl-)> c(NH4+)
B. N 点所示溶液中可能存在:c (NH4+)+ c(NH3﹒H2O)= c(Cl-)
C. Q 点盐酸与氨水恰好中和
D. M 点到Q点所示溶液中水的电离程度先变大后减小
高三化学单选题困难题查看答案及解析
室温下,将 0.10 mol·L-1 盐酸滴入 20.00 mL 0.10 mol·L-1 氨水中,溶液中 pH 和 pOH 随加入盐酸体积变化曲线如图所示。已知:pOH=-lg c(OH-),下列正确的是
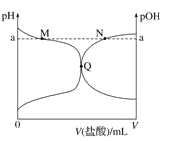
A. M 点所示溶液中可能存在c(Cl-)> c(NH4+)
B. N 点所示溶液中可能存在:c (NH4+)+ c(NH3﹒H2O)= c(Cl-)
C. Q 点盐酸与氨水恰好中和
D. M 点到Q点所示溶液中水的电离程度先变大后减小
高三化学单选题困难题查看答案及解析
室温下,将0.10 mol·L-1盐酸逐滴滴入20.00 mL 0.10 mol·L-1氨水中,溶液中pH和pOH随加入盐酸体积变化曲线如图所示。已知:pOH= -lg c(OH-)。
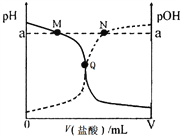
下列说法正确的是
A. M点所示溶液c(NH4+)+c(NH3·H2O)= c(Cl-)
B. N点所示溶液中:c(NH4+)>c(Cl-)
C. Q点所示消耗盐酸的体积等于氨水的体积
D. M点和N点所示溶液中水的离子积相同
高三化学单选题困难题查看答案及解析
室温下,将0.10 mol·L-1盐酸滴入20.00 mL 0.10mol·L-1氨水中,溶液中pH和pOH随加入盐酸体积变化曲线如图所示。已知:pOH=-lg c(OH-),下列说法正确的是
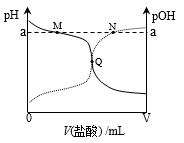
A. M点所示溶液中c(NH4+)+c(NH3·H2O)=c(Cl-)
B. N点所示溶液中溶质一定含NH4Cl,可能还含HCl
C. Q点消耗盐酸的体积等于氨水的体积
D. Q点所示溶液中c(NH4+)> c(Cl-)> c(NH3·H2O)> c(OH-)> c(H+)
高三化学选择题困难题查看答案及解析
室温下,将0.10 mol·L-1盐酸滴入20.00 mL 0.10mol·L-1氨水中,溶液中pH和pOH随加入盐酸体积变化曲线如图所示。已知:pOH=-lg c(OH-),下列说法正确的是
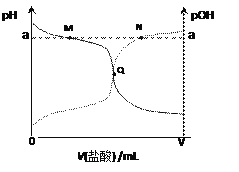
A. N点所在曲线为pH变化曲线
B. M、N两点的溶液中NH4+的物质的量:M>N
C. Q点消耗盐酸的体积大于氨水的体积
D. 随着盐酸滴入,溶液导电性持续增强
高三化学单选题困难题查看答案及解析
室温下,将0.10 mol·L-1盐酸滴入20.00 mL 0.10mol·L-1氨水中,溶液中pH和pOH随加入盐酸体积变化曲线如图所示。已知:pOH=-lg c(OH-),下列说法正确的是
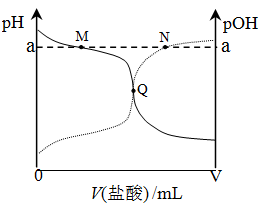
A.M点所示溶液中c(NH4+)+c(NH3·H2O)=c(Cl-)
B.N点所示溶液中c(NH4+)>c(Cl-)
C.Q点消耗盐酸的体积等于氨水的体积
D.M点和N点所示溶液中水的电离程度相同
高三化学选择题困难题查看答案及解析