-
从某废催化剂(含ZnO、CuO、Fe2O3、石墨及MnO2等)中回收金属并制取活性氧化锌的工艺流程如下(已知:Zn及其氧化物、氢氧化物的性质与Al及其相应化合物性质类似):
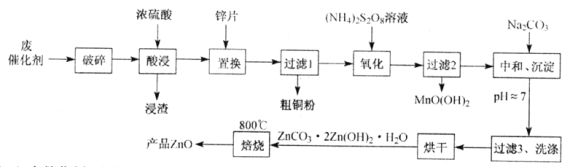
(1)废催化剂“破碎”的目的是____________________________________________。
(2)“氧化”时Mn2+被氧化的离子方程式为_________________________________。
(3)“中和、沉淀”时,若pH过高,则碱式碳酸锌的产率偏小。写出其反应的离子方程式(任写一个即可):____________________________________________。
(4)测得“粗铜粉”中铜的质量分数的实验步骤如下:
I.准确称取粗铜粉mg,加入足量盐酸和H2O2溶液使其完全溶解。
Ⅱ.将溶液煮沸1~2min,除去过量的H2O2。
Ⅲ.滴入铁掩蔽剂排除Fe3+的干扰。然后加入稍过量的KI溶液(反应:2Cu2++4I-=2CuI↓+I2),再加入几滴淀粉溶液作指示剂,用 c mol ·L-1Na2S2O3标准溶液滴定至蓝色消失(I2+2S2O32-=2I-+S4O62-)且半分钟内不变色,共消耗Na2S2O3标准溶液VmL。
①铜的质量分数为______________________。
②缺少步骤Ⅱ哙会使测得的铜的质量分数___________(填“偏大”、“偏小”、或“不变”)
-
从某废催化剂(含ZnO、CuO、Fe2O3、石墨及MnO2等)中回收金属并制取活性氧化锌的工艺流程如下(已知:Zn及其氧化物、氢氧化物的性质与Al及其相应化合物性质类似):

(1)废催化剂“破碎”的目的是____________________________________________。
(2)“氧化”时Mn2+被氧化的离子方程式为_________________________________。
(3)“中和、沉淀”时,若pH过高,则碱式碳酸锌的产率偏小。写出其反应的离子方程式(任写一个即可):____________________________________________。
(4)测得“粗铜粉”中铜的质量分数的实验步骤如下:
I.准确称取粗铜粉mg,加入足量盐酸和H2O2溶液使其完全溶解。
Ⅱ.将溶液煮沸1~2min,除去过量的H2O2。
Ⅲ.滴入铁掩蔽剂排除Fe3+的干扰。然后加入稍过量的KI溶液(反应:2Cu2++4I-=2CuI↓+I2),再加入几滴淀粉溶液作指示剂,用 c mol ·L-1Na2S2O3标准溶液滴定至蓝色消失(I2+2S2O32-=2I-+S4O62-)且半分钟内不变色,共消耗Na2S2O3标准溶液VmL。
①铜的质量分数为______________________。
②缺少步骤Ⅱ哙会使测得的铜的质量分数___________(填“偏大”、“偏小”、或“不变”)
-
从某废催化剂(含ZnO、CuO、Fe2O3、石墨及MnO2等)中回收金属并制取活性氧化锌的工艺流程如下(已知:Zn及其氧化物、氢氧化物的性质与Al及其相应化合物性质类似):

(1)废催化剂“破碎”的目的是____________________________________________。
(2)“氧化”时Mn2+被氧化的离子方程式为_________________________________。
(3)“中和、沉淀”时,若pH过高,则碱式碳酸锌的产率偏小。写出其反应的离子方程式(任写一个即可):____________________________________________。
(4)测得“粗铜粉”中铜的质量分数的实验步骤如下:
I.准确称取粗铜粉mg,加入足量盐酸和H2O2溶液使其完全溶解。
Ⅱ.将溶液煮沸1~2min,除去过量的H2O2。
Ⅲ.滴入铁掩蔽剂排除Fe3+的干扰。然后加入稍过量的KI溶液(反应:2Cu2++4I-=2CuI↓+I2),再加入几滴淀粉溶液作指示剂,用 c mol ·L-1Na2S2O3标准溶液滴定至蓝色消失(I2+2S2O32-=2I-+S4O62-)且半分钟内不变色,共消耗Na2S2O3标准溶液VmL。
①铜的质量分数为______________________。
②缺少步骤Ⅱ哙会使测得的铜的质量分数___________(填“偏大”、“偏小”、或“不变”)
-
从某废催化剂(含ZnO、CuO、Fe2O3、石墨及MnO2等)中回收金属并制取活性氧化锌的工艺流程如图(已知:Zn及其氧化物、氢氧化物的性质与Al及其相应化合物性质类似):

(1)“氧化”时Mn2+被氧化的离子方程式为___________________________________。
(2)“中和、沉淀”时,若pH过高,则碱式碳酸锌的产率偏小。写出其反应的离子方程式(任写一个即可):_________________________________。
-
一种从废甲醇催化剂(含ZnO、CuO及少量Fe2O3、石墨及MnO2等)回收铜并制取活性氧化锌的工艺流程如下:
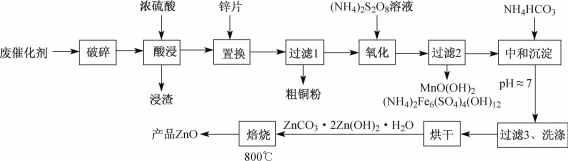
回答下列问题:
(1)废催化剂“破碎”的目的是________,“酸浸”后“浸渣”的主要成分是________。
(2)“氧化”时Mn2+被氧化的离子方程式为________。
(3)“中和沉淀”时pH对锌转化为碱式碳酸锌的转化率影响如图所示:pH>7时,转化率开始减小的原因是________[用离子方程式说明,已知Zn(OH)2性质与Al(OH)3类似]。
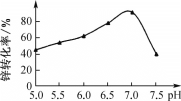
(4)“过滤3、洗涤”时,能证明已洗涤干净的操作方法是________;所得滤液中主要溶质是________。
(5)测定“粗铜粉”中铜的质量分数的实验步骤如下:
Ⅰ.准确称取粗铜粉mg,加入足量HCl和H2O2使其完全溶解(Cu+H2O2+2H+=Cu2++2H2O,Zn及Fe也同时溶解)。
Ⅱ.将溶液煮沸1~2min,除去过量的H2O2。
Ⅲ.依次滴入适量氨水、醋酸及NH4HF2溶液,以排除Fe3+的干扰。然后加入稍过量的KI(2Cu2++4I-=2CuI↓+I2),再加入1mL淀粉溶液作指示剂,用cmol·L-1Na2S2O3标准溶液滴定至蓝色消失(I2+2S2O32-=2I-+S4O62-)且半分钟内不变色,共消耗Na2S2O3标准溶液VmL。
①铜的质量分数为________(列出计算表达式)。
②缺少步骤Ⅱ会使测定的铜的质量分数________(填“偏大”“偏小”或“不变”)。
-
废物利用有利于环境保护、资源节约,一种从废催化剂(含ZnO、CuO及少量石墨、Fe2O3及MnO2等)回收铜并制取活性氧化锌的工艺流程如图:
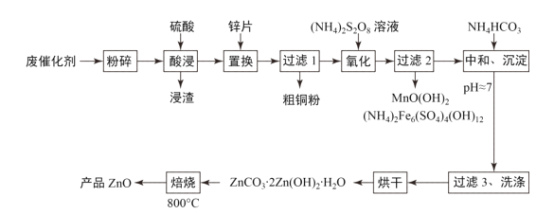
(1)为提高酸浸的速率,还可采取的措施为___。
(2)“氧化”时2molMn2+被氧化为MnO(OH)2,需要(NH4)2S2O8的物质的量为___。
(3)已知Zn(OH)2性质与Al(OH)3类似,在“中和、沉淀”时pH不能过大,请用文字结合离子方程式解释原因___。
(4)“过滤3、洗涤”时,对所得滤液蒸发浓缩、冷却结晶可得___(填主要物质的化学式)固体。
(5)“焙烧”过程中化学方程式为___。
(6)经测定,1kg废催化剂可得160g粗铜粉,又知粗铜粉中铜的质量分数为80%,则废催化剂中铜的质量分数为___%,若“酸浸”时硫酸浓度变小而又没有及时补充,则测定结果会比实际情况___(填“偏大”“偏小”或“无影响”)。
-
现从锌制品加工企业回收的废渣(含有ZnO、FeO、Fe2O3、CuO、Al2O3等杂质)来制取氧化锌,流程如下:
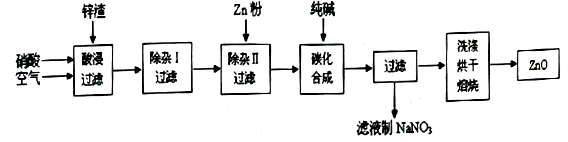
有关氢氧化物完全沉淀的pH见下表:
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 6.7 | 8.0 |
(l)在酸浸过程中,要提高锌元素的浸出率,可以采取________措施。
(2)上述流程中多处涉及“过滤”,实验室中过滤操作需要使用的玻璃仪器有________。
(3)在“除杂I”步骤中,将溶液调至pH=4的目的是________。在“除杂II”后,溶液的pH约为6,则此步过滤时滤渣中含有________。
(4)在“碳化合成”中,生成的产物之一为碱式碳酸锌[Zn2(OH)2CO3],同时放出CO2,请写出该反应的化学方程式。
(5)从滤液中提取NaNO3晶体的操作步骤为________。
(6)在实验室如何洗涤过滤出的碱式碳酸锌?________。
-
现从锌制品加工企业回收的废渣(含有ZnO、FeO、Fe2O3、CuO、Al2O3等杂质)来制取氧化锌,流程如下:
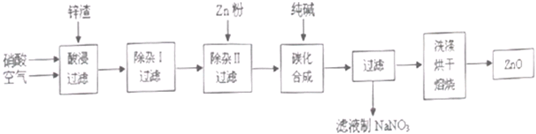
有关氢氧化物完全沉淀的pH见下表
| 沉淀物 | AI(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 6.7 | 8.0 |
(l)在酸浸过程中,要提高浸出率,可以采取______措施.
(2)上述流程中多处涉及“过滤’,实验室中过滤操作需要使用的玻璃仪器有______.
(3)在“除杂I”步骤中,将溶液调至pH=4的目的是______.
在“除杂Ⅱ”后,溶液的pH约为6,则此步过滤时滤渣中含有______.
(4)在“碳化合成”中,生成的产物之一为碱式碳酸锌[Zn2(OH)2CO3],同时放出CO2,请写出该反应的化学方程式______.
(5)从滤液中提取NaNO3晶体的操作步骤为______.
(6)在实验室如何洗涤过滤出的碱式碳酸锌?______.
-
以炼锌烟尘(主要成份为ZnO,含少量CuO和FeO)为原料,可以制取氧化锌和金属锌。
Ⅰ.制取氧化锌主要工艺如下:

下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为l.0mol/L计算)。
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Zn2+ | 5.2 | 6.4 |
| Fe2+ | 5.8 | 8.8 |
(1)为了加快反应,“酸溶”需要适当加热,但温度不宜太高,原因是_________。
(2)加入H2O2溶液发生反应的离子方程式_______。
(3)流程图中,为了降低溶液的酸度,调节pH范围为_______;若试剂X为Zn2(OH)2CO3,加入X除杂质的离子方程式为________。
(4)已知,室温下,Ksp[Fe(OH)3]=4.0×10-38,当pH=3时,溶液中c(Fe3+)为______。从ZnCl2溶液中提取无水ZnCl2的方法是__________.
Ⅱ.制取金属锌采用碱溶解ZnO(s)+2NaOH (aq)+H2O=Na2[Zn(OH)4](aq),然后电解浸取液。
(5)炼锌烟尘采用碱溶,而不采用酸溶后电解,主要原因是______。
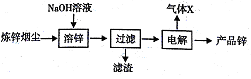
(6)以石墨作电极电解时,阳极产生的气体为______;阴极的电极反应为______。
-
利用工业炼铅产生的锌灰(主要成分为ZnO、PbO、FeO、MnO2、CuO)可回收制备ZnCl2,工艺流程如下:
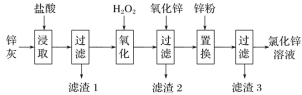
回答下列问题
(1)“浸取”实验中,反应体系的温度、反应时间对锰脱除效果的影响如下表,则适合的温度和反应时间分别是________、________。
表1 温度对锰脱除效果的影响
| 温度/℃ | ρ(Mn2+)/mg/L | 除锰率/% |
| 10 | 0.325 | 87.9 |
| 30 | 0.341 | 89.5 |
| 50 | 0.424 | 84.3 |
| 70 | 0.646 | 76.1 |
表2 反应时间对锰脱除效果的影响
| 时间/h | ρ(Mn2+)/mg/L | 除锰率/% |
| 1.0 | 0.995 | 63.1 |
| 1.5 | 0.794 | 70.6 |
| 2.0 | 0.328 | 87.9 |
| 2.5 | 0.325 | 87.9 |
(2)“滤渣1”的主要成分是________。
(3)H2O2溶液的作用是___________,已知“滤渣2”的主要成分是Fe(OH)3,则氧化锌的作用是____________。“置换”实验中发生反应的离子方程式有Zn+Pb2+=Pb+Zn2+、_________。
(4)由锌灰制取金属锌可采用碱溶解,然后电解浸取液,已知:ZnO溶于NaOH溶液中生成[Zn(OH)4]2−,则阴极的电极反应为____________________________________________。
(5)ZnCl2晶体溶解于饱和Na2CO3溶液中,得到6.46 g的碱式碳酸锌[Znx(CO3)y(OH)z],为了测定其组成,充分加热分解,产生的气体依次通入浓硫酸和碱石灰,质量分别增重了0.72g和0.88g,则该碱式碳酸锌的化学式为________________。











