-
已知:2H2O(l)=2H2(g)+O2(g) △H=+571.0 kJ/mol。以太阳能为热源分解Fe3O4,经热化学铁氧化合物循环分解水制H2的过程如下:

过程I:2Fe3O4(s)=6FeO(s)+O2(g) △H=+313.2 kJ/mol
过程II:……
下列说法不正确的是
A.过程I中每消耗232gFe3O4转移2mol电子:
B.过程II热化学方程式为:3FeO(s)+H2O(l)=H2(g)+Fe3O4(s) △H=+128.9 kJ/mol
C.过程I、II中能量转化的形式依次是:太阳能→化学能→热能
D.过程I中正反应的活化能大于逆反应的活化能
-
已知:2H2O(l)=2H2(g)+O2(g) ΔH=+571.0kJ/mol。以太阳能为热源分解Fe3O4,经热化学铁氧化合物循环分解水制H2的过程如下:

过程Ⅰ:2Fe3O4(s)=6FeO(s)+O2(g) ΔH=+313.2kJ/mol
过程Ⅱ:……
下列说法不正确的是( )
A.过程Ⅰ中每消耗232gFe3O4转移2mol电子
B.过程Ⅱ热化学方程式为:3FeO(s)+H2O(l)=H2(g)+Fe3O4(s) ΔH=-128.9kJ/mol
C.过程Ⅰ、Ⅱ中能量转化的形式依次是:太阳能→化学能→热能
D.铁氧化合物循环制H2具有成本低、产物易分离等优点
-
下列热化学方程式及其有关叙述正确的是( )
A.氢气的燃烧热为285.8kJ·mol-1,则水分解的热化学方程式为2H2O(l)=2H2(g)+O2(g) ΔH =+571.6kJ·mol-1
B.已知2C(石墨,s)+O2(g)=2CO(g) ΔH =+221kJ·mol-1,则石墨的燃烧热110.5kJ·mol-1
C.已知N2(g)+3H2(g)  2NH3(g) ΔH=-92.4kJ·mol-1,则在一定条件下将1mol N2和3mol H2置于一密闭容器中充分反应,放出92.4kJ的热量
2NH3(g) ΔH=-92.4kJ·mol-1,则在一定条件下将1mol N2和3mol H2置于一密闭容器中充分反应,放出92.4kJ的热量
D.已知乙炔的燃烧热为 ,则表示乙炔燃烧热的热化学方程式为
,则表示乙炔燃烧热的热化学方程式为 ΔH=
ΔH=
-
科学家研究以太阳能为热源分解Fe3O4,最终循环分解水制H2,其中一步重要反应为:2Fe3O4(s) 6FeO(s)+O2(g) △H=a kJ/mol。在一定压强下, Fe3O4的平衡转化率随温度变化的a(Fe3O4)―T曲线如图所示。下列有关说法不正确的是
6FeO(s)+O2(g) △H=a kJ/mol。在一定压强下, Fe3O4的平衡转化率随温度变化的a(Fe3O4)―T曲线如图所示。下列有关说法不正确的是
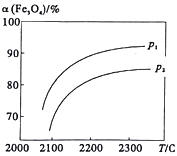
A. a>0
B. 压强p1>p2
C. 升高温度,该反应的平衡常数增大
D. 将体系中O2分离出去,能提高Fe3O4的转化率
-
通过以下反应均可获取H2。下列有关说法正确的是( )
①太阳光催化分解水制氢:2H2O(l)= 2H2(g)+ O2(g) △H1=+ 571.6kJ.mol-1
②焦炭与水反应制氢: C(s) + H2O(g) = CO(g) +H2(g) △H2=+ 131.3kJ.mol-1
③甲烷与水反应制氢:CH4(g) + H2O(g) = CO(g) + 3H2(g) △H3=+ 206.1kJ.mol-1
A. 反应①中电能转化为化学能
B. 反应②可设计成原电池
C. 反应③使用催化剂,△H3 减小
D. 反应CH4(g) = C(s)+ 2H2(g) 的 △H = + 74.8kJ.mol-1
-
[2016·江苏]通过以下反应均可获取H2。下列有关说法正确的是
①太阳光催化分解水制氢:2H2O(l) 2H2(g)+ O2(g) ΔH1=571.6 kJ·mol–1
2H2(g)+ O2(g) ΔH1=571.6 kJ·mol–1
②焦炭与水反应制氢:C(s)+ H2O(g) CO(g)+ H2(g) ΔH2=131.3 kJ·mol–1
CO(g)+ H2(g) ΔH2=131.3 kJ·mol–1
③甲烷与水反应制氢:CH4(g)+ H2O(g) CO(g)+3H2(g) ΔH3=206.1 kJ·mol–1
CO(g)+3H2(g) ΔH3=206.1 kJ·mol–1
A.反应①中电能转化为化学能
B.反应②为放热反应
C.反应③使用催化剂,ΔH3减小
D.反应CH4(g) C(s)+2H2(g)的ΔH=74.8 kJ·mol–1
C(s)+2H2(g)的ΔH=74.8 kJ·mol–1
-
下列有关热化学方程式及其叙述正确的是( )
A. H2的燃烧热为285.8 kJ/mol,则H2O分解的热化学方程式为:2H2O(l) = 2H2(g)+O2(g) ΔH=+285.8 kJ/mol
B. 1 mol CH4完全燃烧生成CO2(g)和H2O(l)时放出890 kJ的热量,其热化学方程式为:1/2CH4(g)+O2(g) = 1/2CO2(g)+H2O(l) ΔH=-445 kJ/mol
C. 已知2C(s)+O2(g)= 2CO(g) ΔH=-221 kJ/mol,则C的燃烧热为110.5 kJ/mol
D. HF与NaOH溶液反应:H+(aq)+OH-(aq) = H2O(l) ΔH=-57.3 kJ/mol
-
通过以下反应均可获取H2。下列有关说法正确的是( )
①太阳光催化分解水制氢:2H2O(l)=2H2(g)+O2(g) △H1=+571.6kJ·mol–1
②焦炭与水反应制氢:C(s)+H2O(g)=CO(g)+H 2(g) △H2=+131.3kJ·mol–1
2(g) △H2=+131.3kJ·mol–1
③甲烷与水反应制氢:CH4(g)+H2O(g)=CO(g)+3H2(g) △H3=+206.1kJ·mol–1
A.反应①中电能转化为化学能
B.反应②为放热反应
C.反应③使用催化剂,△H3减小
D.反应CH4(g)=C(s)+2H2(g)的△H=+74.8kJ·mol–1
-
通过以下反应均可获取H2。下列有关说法正确的是( )
①太阳光催化分解水制氢:2H2O(l)=2H2(g)+ O2(g) ΔH1=+571.6kJ·mol–1
②焦炭与水反应制氢:C(s)+ H2O(g) =CO(g)+ H2(g)ΔH2=+131.3kJ·mol–1
③甲烷与水反应制氢:CH4(g)+ H2O(g)=CO(g)+3H2(g)ΔH3=+206.1kJ·mol–1
A. 反应①中电能转化为化学能
B. 反应②为放热反应
C. 反应③使用催化剂,ΔH3减小
D. 反应CH4(g)=C(s)+2H2(g)的ΔH=+74.8kJ·mol–1
-
通过以下反应均可获取H2。下列有关说法正确的是( )
①太阳光催化分解水制氢:2H2O(l)=2H2(g)+ O2(g) ΔH1=571.6kJ·mol–1
②焦炭与水反应制氢:C(s)+ H2O(g) =CO(g)+ H2(g)ΔH2=131.3kJ·mol–1
③甲烷与水反应制氢:CH4(g)+ H2O(g)=CO(g)+3H2(g)ΔH3=206.1kJ·mol–1
A.反应①中电能转化为化学能
B.反应②为吸热反应
C.反应③使用催化剂,ΔH3减小
D.反应CH4(g)=C(s)+2H2(g)的ΔH=74.8kJ·mol–1


 6FeO(s)+O2(g) △H=a kJ/mol。在一定压强下, Fe3O4的平衡转化率随温度变化的a(Fe3O4)―T曲线如图所示。下列有关说法不正确的是
6FeO(s)+O2(g) △H=a kJ/mol。在一定压强下, Fe3O4的平衡转化率随温度变化的a(Fe3O4)―T曲线如图所示。下列有关说法不正确的是