科学家研究以太阳能为热源分解Fe3O4,最终循环分解水制H2,其中一步重要反应为:2Fe3O4(s) 6FeO(s)+O2(g) △H=a kJ/mol。在一定压强下, Fe3O4的平衡转化率随温度变化的a(Fe3O4)―T曲线如图所示。下列有关说法不正确的是
6FeO(s)+O2(g) △H=a kJ/mol。在一定压强下, Fe3O4的平衡转化率随温度变化的a(Fe3O4)―T曲线如图所示。下列有关说法不正确的是
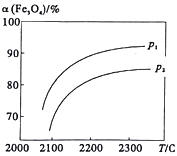
A. a>0
B. 压强p1>p2
C. 升高温度,该反应的平衡常数增大
D. 将体系中O2分离出去,能提高Fe3O4的转化率
高二化学单选题中等难度题
科学家研究以太阳能为热源分解Fe3O4,最终循环分解水制H2,其中一步重要反应为:2Fe3O4(s) 6FeO(s)+O2(g) △H=a kJ/mol。在一定压强下, Fe3O4的平衡转化率随温度变化的a(Fe3O4)―T曲线如图所示。下列有关说法不正确的是
6FeO(s)+O2(g) △H=a kJ/mol。在一定压强下, Fe3O4的平衡转化率随温度变化的a(Fe3O4)―T曲线如图所示。下列有关说法不正确的是

A. a>0
B. 压强p1>p2
C. 升高温度,该反应的平衡常数增大
D. 将体系中O2分离出去,能提高Fe3O4的转化率
高二化学单选题中等难度题
科学家研究以太阳能为热源分解Fe3O4,最终循环分解水制H2,其中一步重要反应为:2Fe3O4(s) 6FeO(s)+O2(g) △H=a kJ/mol。在一定压强下, Fe3O4的平衡转化率随温度变化的a(Fe3O4)―T曲线如图所示。下列有关说法不正确的是
6FeO(s)+O2(g) △H=a kJ/mol。在一定压强下, Fe3O4的平衡转化率随温度变化的a(Fe3O4)―T曲线如图所示。下列有关说法不正确的是

A. a>0
B. 压强p1>p2
C. 升高温度,该反应的平衡常数增大
D. 将体系中O2分离出去,能提高Fe3O4的转化率
高二化学单选题中等难度题查看答案及解析
已知:2H2O(l)=2H2(g)+O2(g) △H=+571.0 kJ/mol。以太阳能为热源分解Fe3O4,经热化学铁氧化合物循环分解水制H2的过程如下:

过程I:2Fe3O4(s)=6FeO(s)+O2(g) △H=+313.2 kJ/mol
过程II:……
下列说法不正确的是
A.过程I中每消耗232gFe3O4转移2mol电子:
B.过程II热化学方程式为:3FeO(s)+H2O(l)=H2(g)+Fe3O4(s) △H=+128.9 kJ/mol
C.过程I、II中能量转化的形式依次是:太阳能→化学能→热能
D.过程I中正反应的活化能大于逆反应的活化能
高二化学单选题中等难度题查看答案及解析
已知:2H2O(l)=2H2(g)+O2(g) ΔH=+571.0kJ/mol。以太阳能为热源分解Fe3O4,经热化学铁氧化合物循环分解水制H2的过程如下:

过程Ⅰ:2Fe3O4(s)=6FeO(s)+O2(g) ΔH=+313.2kJ/mol
过程Ⅱ:……
下列说法不正确的是( )
A.过程Ⅰ中每消耗232gFe3O4转移2mol电子
B.过程Ⅱ热化学方程式为:3FeO(s)+H2O(l)=H2(g)+Fe3O4(s) ΔH=-128.9kJ/mol
C.过程Ⅰ、Ⅱ中能量转化的形式依次是:太阳能→化学能→热能
D.铁氧化合物循环制H2具有成本低、产物易分离等优点
高二化学多选题中等难度题查看答案及解析
研究NO2、SO2、CO等大气污染气体的处理具有重要意义。
(1)有科学家提出可利用FeO吸收和利用CO2,相关热化学方程式如下:
6FeO(s) + CO2(g) = 2Fe3O4(s) + C(s) △H= —76.0kJ/mol
C(s) + 2H2O(g) = CO2(g) + 2H2(g) △H= + 113.4kJ/mol
写出FeO(s)和H2O(g)生成Fe3O4(s)和H2(g)的热化学方程式________。
(2)如图为1 mol NO2(g)和1 mol CO(g)反应生成NO(g)和CO2(g)过程中的能量变化示意图。已知E1=134 kJ·mol-1,E2=368 kJ·mol-1(E1、E2为反应的活化能)。

若在反应体系中加入催化剂,反应速率增大,则E1、ΔH的变化分别是________、________(填“增大”、“减小”或“不变”);该反应放出的热量为__________kJ。
(3)若反应SO2(g)+I2(g)+2H2O(g) ═ H2SO4(l)+2HI(g)在150 ℃下能自发进行,则ΔH____________ 0 (填“大于”、“ 小于”或“大于或小于都可”)。
高二化学填空题中等难度题查看答案及解析
(6分)氢能是一种极具发展潜力的清洁能源。以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如下图所示:

反应Ⅱ:2H2SO4(l)=2SO2(g)+O2(g)+2H2O(g) △H=+550 kJ·mol-1
它由两步反应组成:i.H2SO4(l)=SO3(g)+H2O(g) △H=+177 kJ·mol-1
ii.SO3(g)分解。
L(L1、L2)、X可分别代表压强和温度。下图表示L一定时,ii中SO3(g)的平衡转化率随X的变化关系。
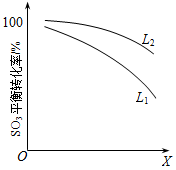
①X代表的物理量是 。
②判断L1、L2的大小关系,L1 L2
并简述理由: 。
高二化学简答题困难题查看答案及解析
科学家积极探索新技术对CO2进行综合利用。
Ⅰ.CO2可用FeO 吸收同时获得H2。
i. 6FeO(s) +CO2(g)=2Fe3O4(s) +C(s) △Hl =-76.0 kJ·mol-1
ⅱ. C(s) +2H2O(g)=CO2(g) +2H2(g) △H2 = +113.4 kJ·mol-1
(1)则3FeO(s) +H2O(g)= Fe3O4(s) +H2(g) △H3 =_________。
Ⅱ.CO2可用来生产燃料甲醇。
CO2(g)+3H2(g)CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1。在体积为1L的恒容密闭容器中,充入1 mol CO2和3 mol H2,一定条件下发生反应:测得CO2和CH3OH(g)的浓度随时间变化如图所示。

(2)从反应开始到平衡,氢气的平均反应速率v(H2)=_________ mol·(L·min) -1。
(3)氢气的转化率=________________________。
(4)该反应的平衡常数为______________________(保留小数点后2位)。
(5)下列措施中能使平衡体系中n(CH3OH)/n(CO2)增大的是_________________。
A.升高温度 B.充入He(g),使体系压强增大
C.再充入1 mol H2 D.将H2O(g)从体系中分离出去
(6)当反应达到平衡时,CH3OH的体积分数为m1,然后向容器中再加入一定量H2,待反应再一次达到平衡后,CH3OH的体积分数为m2,则m1________m2的关系(填“>”、“<”或“=”)。
高二化学综合题中等难度题查看答案及解析
(15分)资源化利用CO2不仅可以减少温室气体的排放,还可以重新获得燃料或重要工业产品。
(1)有科学家提出可利用FeO吸收和利用CO2,相关热化学方程式为:6FeO(s)+CO2(g)=2Fe3O4(s)+C(s) △H=-76.0kJ/mol,该反应中每生成1mol Fe3O4,转移电子的数目为 。
(2)在一定条件下,二氧化碳转化为甲烷的反应为:CO2(g)+4H2(g) CH4(g)+2H2O(g) △H<0
①向一容积为2L的恒容密闭容器中充入一定量的CO2和H2,在300℃时发生上述反应,达到平衡时各物质的浓度分别为CO2 0.2mol/L, H2 0.8 mol/L, CH4 0.8 mol/L, H2O 1.6 mol/L。起始充入CO2和H2的物质的量分别为 、 。CO2的平衡转化率为 。
②现有两个相同的恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ,在Ⅰ中充入1mol CO2和4molH2,在Ⅱ中充入1mol CH4和2molH2O(g),300℃开始反应,达到平衡时,下列说法正确的是( )(填字母)。
A、容器Ⅰ、Ⅱ中正反应速率相同
B、容器Ⅰ、Ⅱ中反应的平衡常数相同
C、容器Ⅰ中CO2的物质的量比容器Ⅱ中的多
D、容器Ⅰ中CO2的转化率与容器Ⅱ中CH4的转化率之和小于1
(3)华盛顿大学的研究人员研究出一种方法,可实现水泥生产时CO2零排放,其基本原理如下图所示:
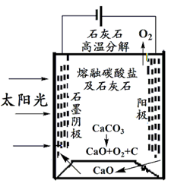
①上述生产过程的能量转化方式是 、 。
②上述电解反应在温度小于900℃时进行,碳酸钙分解为CaO和CO2,电解质为熔融碳酸钠,则阳极电极反应式为 ,阴极电极反应式为 。
高二化学填空题困难题查看答案及解析
科学家积极探索新技术对CO2进行综合利用。
Ⅰ.CO2可用FeO 吸收获得H2。
ⅰ.6FeO(s)+CO2(g)=2Fe3O4(s)+C(s) △Hl=-76.0kJ·mol-1
ⅱ.C(s)+2H2O(g)=CO2(g)+2H2(g) △H2=+113.4kJ·mol-1
(1)3FeO(s)+H2O(g)=Fe3O4(s)+H2(g) △H3=____kJ·mol-1。
(2)在反应i中,每放出38.0kJ热量,有___gFeO被氧化。
Ⅱ.CO2可用来生产燃料甲醇。
CO2(g)+3H2(g)CH3OH(g)+H2O(g) ΔH=-49.0kJ·mol-1。在体积为1L的恒容密闭容器中,充入1molCO2和3molH2,一定条件下发生反应:测得CO2和CH3OH(g)的浓度随时间变化如图所示。
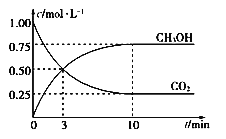
(3)从反应开始到平衡,氢气的平均反应速率v(H2)=___mol·(L·min)-1。
(4)氢气的转化率=___。
(5)该反应的平衡常数为____(保留小数点后2位)。
(6)下列措施中能使平衡体系中增大的是___。
A.升高温度 B.充入He(g),使体系压强增大
C.再充入1 molH2 D.将H2O(g)从体系中分离出去
(7)以甲醇为燃料,空气和熔融K2CO3构成燃料电池,则负极的电极反应为___。
III.CO2可用碱溶液吸收获得相应的原料。
(8)利用100 mL3mol·L-1NaOH溶液吸收4.48LCO2(标准状况),得到吸收液,该吸收液中离子浓度从大到小的关系为___。
高二化学综合题困难题查看答案及解析
为了缓解温空效应,科学家提出了多种回收和利用CO2的方案。
(1)方案1: 利用FeO吸收CO2获得H2
ⅰ.6FeO(s)+CO2(g)=2Fe3O4(s)+C(s) ΔH1=-76.0kJ/mol
ⅱ.C(s)+2H2O(g)=CO2(g)+2H2(g) ΔH2 =+113. 4kJ/mol
请写出由FeO制备H2的热化学方程式_________________。
方案2: 利用CO2制备CH4
300℃时,向2L恒容密闭容器中充入2molCO2和8molH2发生反应: CO2(g)+4H2(g)CH4(g)+ 2H2O(g) ΔH4,混合气体中CH4的浓度与反应时间的关系如图所示。

(2)① 从反应开始到恰好达到平衡时,H2的平均反应速率v(H2)=_________________。
② 300℃时,反应的平衡常数K= _______________。
③ 300℃时,如果该容器中有1.6molCO2、2.0molH2、5.6molCH4、4.0molH2O(g)。则v正____________v逆(填“>”“<”或“=" )
(3)下列有关说法正确的是(填序号)_______________。
A.容器内密度不变,说明反应达到平衡状态
B.容器内压强不变,说明反应达到平衡状态
C.300℃时,向平衡后的容器中再充入2molCO2和8molH2,重新达到平衡时CH4的浓度等于1.6mo/L
D.每断开2molC=O键的同时断开4molC-H键,说明反应达到平衡状态
E.达到平衡后,分离出水蒸气,既能加快反应速率又能使平衡正方向移动
(4)已知200℃时,该反应的平衡常数K=64.8(L/mol)2。则ΔH4________0(填“>”“<”或“=”)。
方案3:利用“Na-CO2”电池将CO2变废为宝。我国科研人员研制出的可充电“Na-CO2”电池钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应为4Na+3CO22Na2CO3+C。放电时该电池“吸入”CO2,其工作原理如图所示:(假设开始时两极的质量相等)

(5)①放电时,正极的电极反应式为_______________。
②若生成的Na2CO3和C全部沉积在电极表面,当转移0.2mole-时,两极的质量差为 _____g。
高二化学综合题困难题查看答案及解析
人类研究氢能源从未间断过,而热化学循环分解水制 H2是在水反应体系中加入一种中间物,经历不同的反应阶段,最终将水分解为H2和O2,这是一种节约能源、节省反应物料的技术,下图是热化学循环制氢气的流程:

(1)实验测得,1 g H2燃烧生成液态水放出142.9 kJ的热量,则表示氢气燃烧热的热化学方程式为_______。
(2)整个流程参与循环的物质是________和________(填化学式),最难进行的反应是____________(填序号)。
(3)汞虽然有毒,但用途广泛。用汞和溴化钙作催化剂,可以在较低温度下经过下列反应使水分解制氢气和氧气:①CaBr2+2H2O=Ca(OH)2+2HBr↑;②……③HgBr2+Ca(OH)2=CaBr2+HgO+H2O;④2HgO=2Hg+O2↑。反应②的化学方程式为________________________。
(4)合成氨用的H2可以甲烷为原料制得。有关化学反应的能量变化如图所示,则CH4(g)与H2O(g)反应生成CO(g)和H2(g)的热化学方程式为___________。


高二化学综合题中等难度题查看答案及解析