-
Zn(OH)2、ZnS分别为白色、淡黄色难溶物,二者溶解度均随温度升高而增大。某温度下,Ksp[Zn(OH)2]=1.0×10-18。向物质的量浓度相同的NaOH和Na2S的混合溶液中滴加ZnSO4溶液,溶液中阳离子、阴离子浓度关系如图所示。图中p(Zn)=-lgc(Zn2+),p(B)=-lgc(OH-)或-1gc(S2-)。下列说法错误的是( )
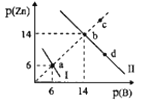
A.曲线l表示的是Zn2+与OH-浓度关系的曲线
B.该温度下,Ksp(ZnS)=1.0×10-28
C.升高温度时,b点一定会向c点移动
D.已知此温度下Ka2(H2S)═4.0×10-16,向0.01mol•L-lNaHS溶液中滴加等体积0.2mol•L-1ZnSO4溶液不能产生沉淀
-
已知25℃物质的溶度积常数为:FeS:Ksp=6.3×10﹣18;CuS:Ksp=1.3×10﹣36;
ZnS:Ksp=1.6×10﹣24.下列说法正确的是( )
A. 相同温度下,CuS的溶解度大于ZnS的溶解度
B. 除去工业废水中的Cu2+,可以选用FeS做沉淀剂
C. 足量CuSO4溶解在0.1mol/L的H2S溶液中,Cu2+能达到的最大浓度为1.3×10﹣35mol/L
D. 在ZnS的饱和溶液中,加入FeCl2溶液,一定不产生FeS沉淀
-
下列说法不正确的是
A.Ksp只与难溶电解质的性质和温度有关
B.两种难溶电解质,Ksp小的,溶解度一定小
C.其他条件不变,离子浓度改变时,Ksp不变
D.由于Ksp(ZnS) ﹥Ksp(CuS),所以ZnS沉淀在一定条件下可转化为CuS沉淀
-
下列有关说法中正确的是()
A.Ksp(AB2)<Ksp(CD),说明AB2 的溶解度小于CD 的溶解度
B.在ZnS的沉淀溶解平衡体系中加入蒸馏水,ZnS的Ksp增大
C.AgCl 分别在同浓度的CaCl2溶液和NaCl 溶液中溶解度不同
D.在CaCO3的沉淀溶解平衡体系中加入稀盐酸,沉淀溶解平衡不移动
-
已知如下物质的溶度积常数FeS:Ksp=6.3×10-18;CuS:Ksp=1.3×10-36;ZnS:Ksp=1.6×10-24.下列说法正确的是( )
A.同温度下,CuS的溶解度大于ZnS的溶解度
B.将足量CuSO4溶解在0.1 mol•L-1的H2S溶液中,Cu2+能达到的最大浓度为1.3×10-35 mol•L-1
C.因为H2SO4是强酸,所以Cu2++H2S═CuS↓+2H+不能发生
D.除去工业废水中的Cu2+,可以选用FeS做沉淀剂
-
下列说法不正确的是
A. Ksp只与温度有关
B. 两种难溶电解质,Ksp小的,溶解度不一定小
C. 其他条件不变,离子浓度改变时,Ksp不变
D. 由于Ksp(ZnS)>Ksp(CuS),所以ZnS沉淀在一定条件下可转化为CuS沉淀
-
下列说法不正确的是( )
A.Ksp只与难溶电解质的性质和温度有关
B.由于Ksp(ZnS)>Ksp(CuS),ZnS的溶解度大于CuS
C.其他条件不变,离子浓度改变时,Ksp不变
D.两种难溶电解质作比较时,Ksp越小的电解质,其溶解度一定越小
-
下列说法正确的是
A. 只有难溶电解质才存在沉淀溶解平衡
B. 溶度积Ksp与温度有关,温度越高,溶度积越大
C. 难溶电解质的溶度积Ksp越小,则它的溶解度越小
D. 已知Ksp(ZnS)>Ksp(CuS),则ZnS沉淀在一定条件下可以转化为CuS 沉淀
-
有关AgCl沉淀的溶解平衡的说法正确的是( )
A. AgCl沉淀的生成和溶解仍在不断进行,但速率相等
B. AgCl不溶于水,溶液中没有Cl-和Ag+
C. 升高温度,AgCl的溶解度增大,Ksp不变
D. 向AgCl饱和溶液中加入NaCl固体,AgCl的溶解度和Ksp都不变
-
印染工业常用亚氯酸钠(NaClO2)漂白织物。用过氧化氢法生产亚氯酸钠的工艺流程如下:

已知:①NaClO2的溶解度随温度的升高而增大,适当条件下可结晶析出NaClO2·3H2O。
②Ksp(FeS)=6.3×10-18;Ksp(CuS)= 6.3×10-36;Ksp(PbS)=2.4×10-28。
(1)发生器中反应的还原剂是_________(填化学式,下同)。吸收塔内ClO2在碱性条件下与H2O2生成NaClO2 的离子方程式为_______
(2)从滤液中得到的NaClO2·3H2O的操作依次是_______、(填字母)、洗染、干燥。
a.蒸馏 b.灼烧 c.冷却结晶 d.蒸发浓缩 e.过滤
(3)亚氯酸钠漂白织物时真正起作用的是HClO2。下表是25℃时HClO2及几种常见弱酸的电离平衡常数。
| 弱酸 | HClO2 | HF | HCN | H2S |
| Ka/mol·L-1 | 1×10-2 | 6.3×10-4 | 4.9×10-10 | K1=9.1×10-8 K2=1.1×10-12 |
①常温下,物质的量浓度相同的NaF、NaCN 两种溶液的PH由大到小的顺序为________。
②等体积等物质的量浓度的HClO2与NaOH溶液充分反应后,溶液中各离子浓度由大到小的顺序为_____。
③Na2S是常用的沉淀剂。某工业污水中含有等浓度的Cu2+、Fe2+、Pb2+,滴加Na2S溶液后最先析出的沉淀是______;当最后一种离子沉淀完全时(该离子浓度为10-5 mol·L-l),此时体系中S2-的浓度为________。

