-
(本题共14分)工业上用氨气与空气混合,通过“氨的催化氧化”等反应工业合成硝酸及其他产品。
1.将NH3与O2在一定条件下充分反应后全部转化为硝酸溶液,则此硝酸溶液中溶质的质量分数为_________________,若所得硝酸密度为ρg/cm3,则其物质的量浓度为 (保留两位小数)。
2.某化肥厂以氨为原料制备 NH4NO3,已知由氨制 NO 的产率是 96%,NO 制硝酸的产率是 92%,氨被硝酸的吸收率为100%,则制备80吨 NH4NO3所需氨的体积(标准状况)为 m3(保留两位小数)。
3.一定量的浓硝酸与铜反应生成NO、NO2、N2O4混合气体。测出混合气体密度是同温同压下氢气的28倍。再将气体通过足量水充分吸收后,体积变为原来的2/3(相同条件下测定)。计算混合气体中NO2的体积分数。
4.合成氨原料气由CH4在高温下与水蒸气、空气反应而得。反应原理如下:
CH4+2H2O→CO2+4H2 2CH4+O2+2H2O→2CO2+6H2
将反应后的混合气中CO2、H2O (g)通过吸收和干燥除去后,只含N2和H2。为使进入合成氨反应塔两者体积比为1∶3。计算起始气体中CH4和空气的比例。(已知空气中O2和N2的体积比为1∶4)。
高三化学计算题极难题查看答案及解析
-
工业上用氨气与空气混合,通过“氨的催化氧化”等反应工业合成硝酸及其他产品。
1.将NH3与O2在一定条件下充分反应后全部转化为硝酸溶液,则此硝酸溶液中溶质的质量分数为_________________,若所得硝酸密度为ρg/cm3,则其物质的量浓度为_______(保留两位小数)。
2.某化肥厂以氨为原料制备 NH4NO3,已知由氨制 NO 的产率是 96%,NO 制硝酸的产率是 92%,氨被硝酸的吸收率为100%,则制备80吨 NH4NO3所需氨的体积(标准状况)为________m3(保留两位小数)。
3.一定量的浓硝酸与铜反应生成NO、NO2、N2O4混合气体。测出混合气体密度是同温同压下氢气的28倍。再将气体通过足量水充分吸收后,体积变为原来的2/3(相同条件下测定)。计算混合气体中NO2的体积分数_____________。
4.合成氨原料气由CH4在高温下与水蒸气、空气反应而得。反应原理如下:
CH4+2H2O→CO2+4H22CH4+O2+2H2O→2CO2+6H2
将反应后的混合气中CO2、H2O (g)通过吸收和干燥除去后,只含N2和H2。为使进入合成氨反应塔两者体积比为1∶3。计算起始气体中CH4和空气的比例。(已知空气中O2和N2的体积比为1∶4)。_____________
高三化学计算题中等难度题查看答案及解析
-
(10分)合成氨是人类科学技术发展史上的一项重大突破,目前工业上用氢气和氮气直接合成氨,制得的氨通过催化氧化可生产硝酸。
在一定条件下,若N2和H2以体积比1:3的比例充入一体积不变的密闭容器中反应,达到平衡状态时,测得混合气体中氨的体积分数为20.0%,则:
(1)合成氨反应达到平衡的标志 ▲ 。
A.容器内气体压强保持不变
B.容器内各物质的浓度不随时间变化
C.当υ(H2,正)=0.3mol·L-1·min-1,υ(NH3,逆)=0.2mol·L-1·min-1时
D.1个N≡N键断裂的同时,有3个H-H键形成
(2)达到平衡时,N2和H2的转化率分别为▲ 。
(3)用氨催化氧化可生产硝酸,取所生产的硝酸溶液100mL,与足量的铜反应,生成的NO2和NO混合气体在标准状况下体积为6.72L,物质的量之比为2:1,求所生产硝酸的物质的量浓度?(请写出该小题的计算过程)
▲ 。
(4)某厂用NH3生产硝酸,然后再制硝酸铵,其过程如下:
其中反应②为:4NO+3O2+2H2O
4HNO3,原料气为氨气和空气的混合物。
若实际生产中,反应①、②、③的转化率(或利用率)分别为a、b、c,则生产硝酸的氨气占所用氨气总量的体积分数为▲ 。
高三化学填空题简单题查看答案及解析
-
合成氨是人类科学技术发展史上的一项重大突破,目前工业上用氢气和氮气直接合成氨,制得的氨通过催化氧化可生产硝酸。
在一定条件下,若N2和H2以体积比1:3的比例充入一体积不变的密闭容器中反应,达到平衡状态时,测得混合气体中氨的体积分数为20.0%,则:
(1)合成氨反应达到平衡的标志▲ 。
A.容器内气体压强保持不变
B.容器内各物质的浓度不随时间变化
C.当υ(H2,正)=0.3mol·L-1·min-1,υ(NH3,逆)=0.2mol·L-1·min-1时
D.1个N≡N键断裂的同时,有3个H-H键形成
(2)达到平衡时,N2和H2的转化率分别为▲ 。
(3)用氨催化氧化可生产硝酸,取所生产的硝酸溶液100mL,与足量的铜反应,生成的NO2和NO混合气体在标准状况下体积为6.72L,物质的量之比为2:1,求所生产硝酸的物质的量浓度?(请写出该小题的计算过程)
▲ 。
(4)某厂用NH3生产硝酸,然后再制硝酸铵,其过程如下:
其中反应②为:4NO+3O2+2H2O
4HNO3,原料气为氨气和空气的混合物。
若实际生产中,反应①、②、③的转化率(或利用率)分别为a、b、c,则生产硝酸的氨气占所用氨气总量的体积分数为▲ 。
高三化学填空题中等难度题查看答案及解析
-
工业上用氨气与空气的混合气在一定条件下制硝酸,发生的反应是:
①4NH3+5O2→4NO+6H2O
②4NO+3O2+2H2O→4HNO3
设空气中氧气的体积分数为0.20,氮气体积分数为0.80,请完成下列填空及计算:
(1)为使氨气恰好完全氧化为一氧化氮,氨气与空气的混合气中氨的体积分数(用小数表示)为______(保留2位小数).
(2)现将1mol的氨气与12mol的空气混合反应,可得到硝酸______mol;
(3)向上述溶液中加入______mL 20%的硝酸(密度为1.11g/mL),才能得到69%的硝酸溶液.
(4)现有100mol的原料气,其中含氨气为xmol,反应后生成的硝酸ymol.在得到硝酸的条件下,写出x与y的关系式.(写出解题过程)高三化学解答题中等难度题查看答案及解析
-
工业上用氨气与空气的混合气在一定条件下制硝酸,发生的反应是:
①4NH3+5O2→4NO+6H2O
②4NO+3O2+2H2O→4HNO3
设空气中氧气的体积分数为0.20,氮气体积分数为0.80,请完成下列填空及计算:
(1)为使氨气恰好完全氧化为一氧化氮,氨气与空气的混合气中氨的体积分数(用小数表示)为______(保留2位小数).
(2)现将1mol的氨气与12mol的空气混合反应,可得到硝酸______mol;
(3)向上述溶液中加入______mL 20%的硝酸(密度为1.11g/mL),才能得到69%的硝酸溶液.
(4)现有100mol的原料气,其中含氨气为xmol,反应后生成的硝酸ymol.在得到硝酸的条件下,写出x与y的关系式.(写出解题过程)高三化学解答题中等难度题查看答案及解析
-
工业合成氨与制备硝酸一般可连续生产,流程如图1:
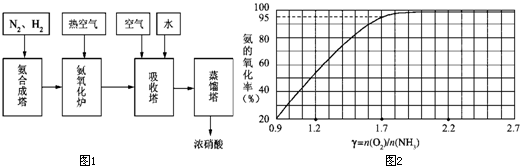
在800℃、铂催化剂存在条件下,氨与氧气反应的主要产物是NO 和H2O.在实际生产中氨的氧化率与混合气中氧氨比(氧气与氨气物质的量比,以γ{n(O2)/n(NH3)}表示)的关系如图2所示.
请回答下列各题:
(1)若氨氧化率达到100%,理论上γ{n(O2)/n (NH3)}为1.25,而实际生产要将γ值维持在1.7~2.2之间,其原因是______.
(2)若使氨的氧化率达到95%,应控制氨在氨、空气混合气体中的体积分数约为______
(设氧气占空气的体积分数为20%).将γ=1.75的氨、空气混合气体通入800℃、盛有铂催化剂的氧化炉,充分反应后导入到吸收塔的气体的主要成分是______.
(3)现以a mol NH3和足量空气为原料(不考虑N2的反应)最大程度制取NH4NO3,经过一系列转化反应后,向反应后的混合物中加入b g水,得到密度为ρ g•mL-1的溶液,计算该溶液中NH4NO3物质的量浓度可能的最大值______.高三化学解答题中等难度题查看答案及解析
-
密胺是重要的工业原料,结构简式如下图。工业上用液氨和二氧化碳为原料,硅胶为催化剂,在一定条件下,通过系列反应生成密胺。若原料完全反应生成密胺,则NH3和CO2的质量之比应为
A.17:44 B.22:17 C.17:22 D.2:1
高三化学选择题中等难度题查看答案及解析
-
下列化学与生产.生活相关的说法正确的是
A.生铁、青铜等合金比纯金属耐腐性强
B.石油主要由各种烃组成的混合物,可以通过分馏的方法分离出C8H18
C.分离工业合成氨产品的方法是将氨气液化
D.氨的催化氧化的适宜条件为高温、高压、催化剂
高三化学单选题中等难度题查看答案及解析
-
氮的氧化物(NOx)是大气污染物之一,工业上在一定温度和催化剂条件下用NH3将NOx还原生成N2,某同学在实验室中对NH3与NOx反应进行了探究。回答下列问题:
(1)氨气的制备
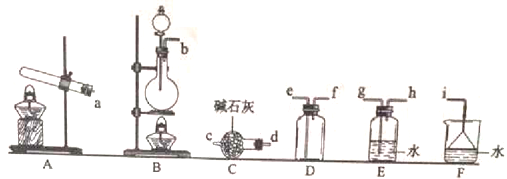
①氨气的发生装置可以选择上图中的_________,反应的化学方程式为_______________。
②预收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:发生装置→______(按气流方向,用小写字母表示)。
(2)氨气与二氧化氮的反应
将上述收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。在一定温度下按图示装置进行实验。

操作步骤
实验现象
解释原因
打开K1,推动注射器活塞,使X中的气体缓慢通入Y管中
①Y管中_____________
②反应的化学方程式
____________
将注射器活塞退回原处并固定,待装置恢复到室温
Y管中有少量水珠
生成的气态水凝集
打开K2
③_______________
④______________
高三化学实验题极难题查看答案及解析