-
醋酸(CH3COOH)是一种常见的弱酸。
(1)为用实验证明醋酸是弱电解质,实验小组同学设计如下几种方案:
①用pH试纸测出0.1mol/L的醋酸溶液pH:若pH___1(填“>”、“<”或“=”),则证明醋酸是弱酸;
②先测0.1mol/L醋酸的pH ;量取该溶液5mL用蒸馏水稀释至500mL,再测其pH,若________________,则证明醋酸是弱电解质;
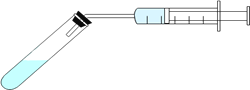
③分别配制pH相同的醋酸和盐酸,各取10mL与足量的锌粒反应(装置如图),测试在不同时间间隔中得到H2的量,即可证明醋酸是弱电解质。下列示意图(X为醋酸,Y为盐酸)中,符合该实验结果的是__________(选填字母);
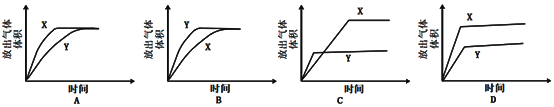
但在该实验中难以实现之处为__________________________________。(举例)
(2)醋酸和氢氧化钠反应生成醋酸钠(CH3COONa)。
①将CH3COONa固体溶于蒸馏水后其溶液显碱性,其原因是(用离子方程式表示)______________________________;在该溶液中,下列关系式中正确的是________;(选填字母)
A.c(Na+)=c(CH3COO-)+c(CH3COOH)
B.c(OH-)=c(H+)+c(CH3COOH)
C.c(CH3COO-)+c(OH-)=c(H+)+c(Na+)
D.c(CH3COO-)>c(OH-)>c(Na+)>c(H+)
②醋酸和氢氧化钠反应后得到溶液中溶质的组成有多种可能:
若得到的溶液中c(Na+)>c(OH-)>c(CH3COO-)>c(H+),试推断该溶液中的溶质为_____;
若得到的溶液中c(CH3COO-)>c(Na+)>c(H+)>c(OH-),则可以推断该溶液中的溶质可能为____;
③将amol/LCH3COOH稀溶液和bmol/LNaOH稀溶液等体积混合:
若测得溶液中c(OH-)=c(H+),则a___b;(选填“>”、“<”、“=”、“≤”或“≥”)
若测得溶液中c(OH-)>c(H+),则a___b;(选填“>”、“<”、“=”、“≤”或“≥”)
-
为了检验某溶液中是否含有常见的四种无机离子,某化学小组的同学进行了如下所示的实验操作。其中检验过程中产生的气体能使湿润的红色石蕊试纸变蓝。由该实验能得出的正确结论是( )
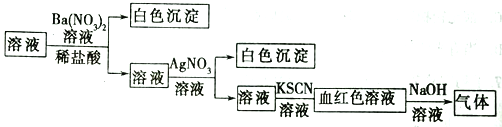
A. 原溶液中一定含有SO42- B. 原溶液中一定含有NH4+
C. 原溶液中一定含有Cl- D. 原溶液中一定含有Fe3+
-
为了检验某溶液中是否含有常见的四种无机离子,某化学小组的同学进行了如下所示的实验操作。其中检验过程中产生的气体能使湿润的红色石蕊试纸变蓝。由该实验能得出的正确结论是( )

A. 原溶液中一定含有SO42- B. 原溶液中一定含有NH4+
C. 原溶液中一定含有Cl- D. 原溶液中一定含有Fe3+
-
为了检验某溶液中是否含有常见的四种无机离子,某化学小组的同学进行了如下所示的实验操作。其中检验过程中产生的气体能使湿润的红色石蕊试纸变蓝。由该实验能得出的正确结论是( )
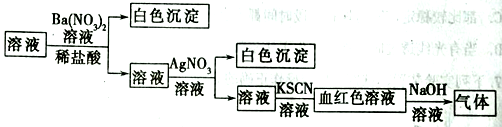
A.原溶液中一定含有SO42- B.原溶液中一定含有NH4+
C.原溶液中一定含有Cl- D.原溶液中一定含有Fe3+
-
(10分)某探究小组在如下实验方案设计中,用铝片、铜片、铁片三种金属和氢氧化钠溶液、稀硝酸、浓硫酸、浓盐酸四种溶液进行实验。请根据要求填空:
(1)若欲证明上述三种金属的活动性强弱,则有关反应的化学方程式为____________。
(2)室温下,将三种金属分别投入上述某种溶液中,均不能观察到明显的现象,这种溶液是___________。
(3)上述某一溶液只能和三种金属中的一种发生化学反应,其离子方程式为_______________________。
(4)室温下,上述某一溶液能和三种金属发生反应,该溶液是_____________。
(5)可用于除去氧化铜粉末中混有的少量氧化铝粉,该溶液是_____________。
-
(15分)某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验。
Ⅰ.(1)试用实验室提供的下列试剂,设计两个原理不同的简单实验(只要写出实验的方案即可),证明镁元素的金属性比铝元素强。
试剂:镁条、铝条、氯化铝溶液、氯化镁溶液、稀盐酸、氢氧化钠溶液
方案一:_____________________________________________________________;
方案二:_____________________________________________________________。
Ⅱ.利用下图装置可验证同周期元素非金属性的变化规律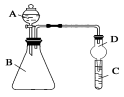
(1)仪器A的名称为________,干燥管D的作用为________________。
(2)若要证明非金属性:Cl>S,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加___________,观察到C中溶液___________________________的现象,即可证明。反应的离子方程式为________________________________________________________。
从环境保护的观点考虑,此装置缺少尾气处理装置,可用________溶液吸收尾气。
(3)若要证明非金属性:N>C,则在A中加稀硝酸,B中加碳酸钙,C中加澄清石灰水;观察到C中溶液变浑浊的现象,即可证明。该实验原理为______________________________。但有的同学在实验中一切操作正确的情况下没观察到上述现像,试分析可能的原因是___________________________。
-
经精选后的铝土矿A(主要成份为Al2O3,含有一定量的Fe2O3、SiO2杂质),可用A来制备电解铝原料——氧化铝,某课外小组同学模拟该过程,设计了如下方案:

请回答:
(1)A中Al2O3与过量氢氧化钠溶液反应的化学方程式是________________
(2)操作I的名称是________________。
(3)下列说法中正确的是________(填选项)。
a 操作Ⅱ是灼烧 b. 滤液3所含阳离子是Fe3+、Al3+
c. 试剂b可用氢氧化钠 d. 为保证转化完全,所加试剂a和试剂b均应过量
(4)写出滤液2、4混合后生成Al(OH)3的离子方程式是______________________ __
-
铜是人类认识并应用最早的金属之一,我国是最早使用铜器的国家之一。铁与人类生活密切相关,几乎无处不在,是地壳中含量仅次于铝的金属。某研究性学习小组为了证明铁的金属活动性比铜强,设计了如下实验方案:
(1)将铁片置于硫酸铜溶液中有铜析出
(2)足量的铁粉和铜粉与浓硫酸在加热条件下反应分别生成FeSO4和CuSO4
(3)将铜片置于FeCl3溶液中铜片逐渐溶解
(4)把铁片和铜片置于盛有稀硫酸的烧杯中,并用导线连接,铁片上无气泡产生,而铜片上有气泡产生
(5)把铁片和铜片置于盛有浓硝酸的烧杯中,并用导线连接,铁片上有气泡产生,而铜片上无气泡产生
以上实验方案设计合理的有
A.两种 B.三种 C.四种 D.五种
-
为验证氯气的漂白原理,某化学兴趣小组的同学设计了如下实验。
[思考探究]
(1)甲同学设计方案如下:

其中a、b分别是干燥的有色布条和湿润的有色布条其中的一种,请问它们的顺序如何?能否颠倒?____________________________。
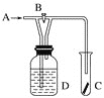
(2)乙同学认为上述设计还较为繁琐,又对实验做了如下改进:C试管中放干燥的红布条,广口瓶D中放水,B是开关,A处通入干燥的氯气。
①如何操作验证氯气是否能与水反应?________________________。
②广口瓶D中的液体能换成氯化钠溶液吗?石灰水呢?_______________。
③图中的实验设计是否有不合理之处?若有,请加以改进。_____________。
-
下面是某化学兴趣小组的同学学习元素周期律时设计的两套实验方案。
(实验一)实验步骤如下:
向新制的Na2S溶液中滴加新制的氯水
设计该实验方案的目的是:探究同周期元素的性质递变规律。
(1)实验①的现象是_____________________,反应的离子方程式是_________________。
(实验二)为验证Cl、Br的非金属性强弱,设计了如下实验:(可供选择的试剂有:氯水、溴水、NaCl溶液、NaBr溶液、酒精、四氯化碳)实验步骤如图.
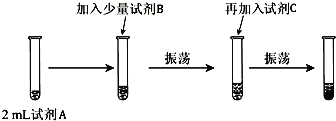
(2)试剂A是NaBr溶液,试剂B是氯水,加C后出现分层,则试剂C是____________.
(3)加入C振荡、静置后看到的现象是:______________________________________。以上反应可以证明Cl的非金属性__________(填“强于”或“弱于”)Br的非金属性。









