-
为验证氯气的漂白原理,某化学兴趣小组的同学设计了如下实验。
[思考探究]
(1)甲同学设计方案如下:

其中a、b分别是干燥的有色布条和湿润的有色布条其中的一种,请问它们的顺序如何?能否颠倒?____________________________。
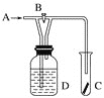
(2)乙同学认为上述设计还较为繁琐,又对实验做了如下改进:C试管中放干燥的红布条,广口瓶D中放水,B是开关,A处通入干燥的氯气。
①如何操作验证氯气是否能与水反应?________________________。
②广口瓶D中的液体能换成氯化钠溶液吗?石灰水呢?_______________。
③图中的实验设计是否有不合理之处?若有,请加以改进。_____________。
-
(8分)某化学兴趣小组欲在实验室探究氯气的性质及模拟工业制取漂白粉,设计了如下装置进行实验:
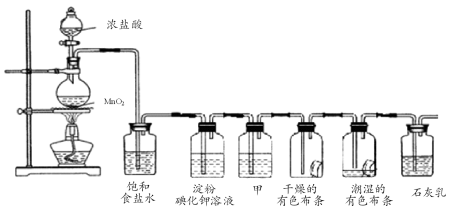
请按要求回答下列问题:
(1)淀粉碘化钾溶液中观察到的现象是 ,反应的离子方程式为 。
(2)若干燥的有色布条不褪色,潮湿的有色布条褪色,则甲中盛放 (填名称)。
(3)C12与石灰乳反应制取漂白粉的化学方程式为 。
(4)该兴趣小组用8.7g MnO2与足量的浓盐酸制备氯气,则理论上最多可制得标准状况下的Cl2 L。
-
某兴趣小组为验证SO2和Cl2的漂白性,设计了如下方案,请你参与回答下列问题(尾气处理装置未画出)。

⑴ 如右图所示,通入干燥的Cl2后,同学们发现甲中红色布条不褪色,乙中红色布条褪色了,说明Cl2本身_______漂白性(填“有”或“没有”),Cl2和水反应的生成物HClO_______漂白性(填“有”或“没有”),将乙中的布条取出烘干,发现未变为原来的红色,说明HClO的漂白是_______(填“可恢复的”或“不可恢复的”)。
⑵ 如图丙所示,向品红溶液中通入SO2,同学们发现品红溶液褪色了,停止通气体,加热试管,发现溶液又变为红色,说明SO2的漂白是_______(填“可恢复的”或“不可恢复的”)。

你认为 利用SO2的漂白性来漂泊食品(填“能”或“不能”)
如图丁所示,将干燥的Cl2和SO2按其体积比1∶1混合,通入石蕊溶液中,发现石蕊溶液变红,不褪色,原因是它们与水一起反应生成了HCl和 H2SO4。写出对应的化学方程式 _______________________________________________________。
-
(16分)某学习小组设计了如下图所示的实验方案来探究氯气的性质。
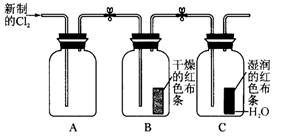
(1)实验时甲同学在A装置中未加入任何试剂,发现B、C中的红色布条均褪色,由此甲同学得出结论:氯气具有漂白性。
实验时乙同学向A装置中加入了某种试剂,发现B中的红色布条不褪色而C中的红色布条褪色,由此乙同学得出结论:氯气没有漂白性。
你认为乙同学向A装置中加入的试剂是 ,甲、乙同学的结论正确的是 。
(2)丙同学思考后认为上面的实验装置存在缺陷,并提出了解决方法。你认为存在的缺陷是 ,解决方法为(用化学方程式表示) 。
(3)丁同学在A装置中加入滴有酚酞的NaOH溶液,观察到A装置中溶液红色逐渐褪去。他提出两种可能原因:①氯气与水反应生成次氯酸,次氯酸具有强氧化性将酚酞氧化使溶液褪色;②氯气与NaOH溶液反应使溶液褪色。请你帮助他设计一个简单的实验验证褪色的原因(简述实验步骤)。
。
-
氯气是一种重要的化工原料,在工农业生产、生活中有着重要的应用。某化学兴趣小组同学对氯气的性质进行如下探究:
(1)兴趣小组同学按下图装置进行实验,探究 Cl2 的漂白性。
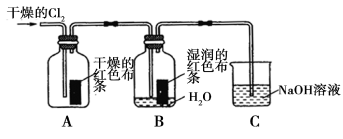
① 通 入Cl2 后 , 观 察 到 的 现 象 是 根 据 现 象 可 得 出 的 结 论是 。
②集气瓶 B发生反应的离子方程式是 。
③C装置的作用是 ,若有2.24L(标准状况下)Cl2被NaOH溶液完全吸收,则反应过程中转移的电子为 _mol。
(2)兴趣小组同学按下图装置进行实验,探究 Cl2 的氧化性。
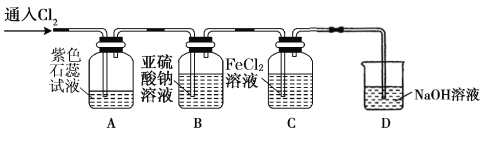
①实验开始后,观察装置 A 中的现象是 。
②装置 C 中发生反应的离子方程式是 。
③停止通入氯气,取装置 B中少量溶液于洁净的试管中,向其中滴加足量稀盐酸,再向其中滴加氯化钡溶液,有白色沉淀生成。则通入 Cl2 时装置 B 中发生 反应的离子方程式是 。
-
(16分)氯气是一种重要的化工原料,在工农业生产、生活中有着重要的应用。某化学兴趣小组同学对氯气的性质进行如下探究:
(1)兴趣小组同学按下图装置进行实验,探究Cl2的漂白性。
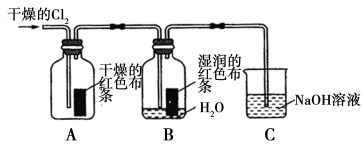
①通入Cl2后,观察到的现象是 根据现象可得出的结论是______。
②集气瓶B发生反应的离子方程式是______。
③C装置的作用是______,若有2.24 L(标准状况下)Cl2被NaOH溶液完全吸收,则反应过程中转移的电子数为________mol。
(2)兴趣小组同学按下图装置进行实验,探究Cl2的氧化性。
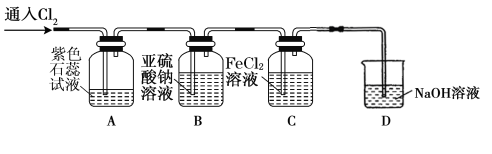
①实验开始后,观察装置A中的现象是: 。
②装置C中发生反应的离子方程式是 。
③停止通入氯气,取装置B中少量溶液于洁净的试管中,向其中滴加足量稀盐酸,再向其中滴加氯化钡溶液,有白色沉淀生成。则通入Cl2时装置B中发生反应的离子方程式是 。
-
氯气是一种重要的化工原料,在工农业生产、生活中有着重要的应用。某化学兴趣小组同学对氯气的性质进行如下探究:
(1)兴趣小组同学按下图装置进行实验,探究Cl2的漂白性。
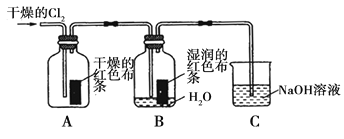
①通入Cl2 后,观察到的现象是 根据现象可得出的结论是 。
②集气瓶B发生反应的离子方程式是 。
③C装置的作用是 ,若有2.24L(标准状况下)Cl2被NaOH溶液完全吸收,则反应过程中转移的电子为 _mol。
(2)兴趣小组同学按下图装置进行实验,探究Cl2的氧化性。
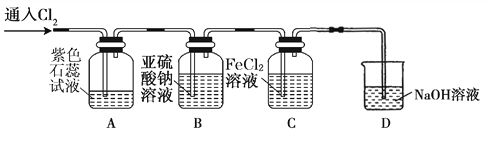
①实验开始后,观察装置A 中的现象是 。
②装置C中发生反应的离子方程式是 。
③停止通入氯气,取装置B中少量溶液于洁净的试管中,向其中滴加足量稀盐酸,再向其中滴加氯化钡溶液,有白色沉淀生成。则通入Cl2时装置B中发生 反应的离子方程式是 。
-
氯气是一种重要的化工原料,在工农业生产、生活中有着重要的应用。某化学兴趣小组同学对氯气的性质进行如下探究:
(1)兴趣小组同学按下图装置进行实验,探究Cl2的漂白性。
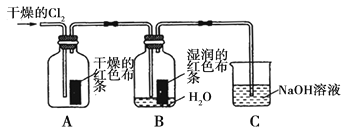
①通入Cl2 后,观察到的现象是 根据现象可得出的结论是 。
②集气瓶B发生反应的离子方程式是 。
③C装置的作用是 ,若有2.24L(标准状况下)Cl2被NaOH溶液完全吸收,则反应过程中转移的电子为 _mol。
(2)兴趣小组同学按下图装置进行实验,探究Cl2的氧化性。
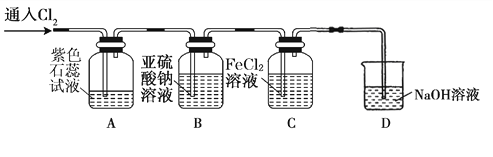
①实验开始后,观察装置A 中的现象是 。
②装置C中发生反应的离子方程式是 。
③停止通入氯气,取装置B中少量溶液于洁净的试管中,向其中滴加足量稀盐酸,再向其中滴加氯化钡溶液,有白色沉淀生成。则通入Cl2时装置B中发生 反应的离子方程式是 。
-
某化学兴趣小组欲在实验室探究氯气的性质及模拟工业制取漂白粉,设计了如下装置进行实验(实验室制取氯气的反应为MnO2 + 4 HCI(浓) MnCl2 + C12↑+ 2 H2O):
MnCl2 + C12↑+ 2 H2O):
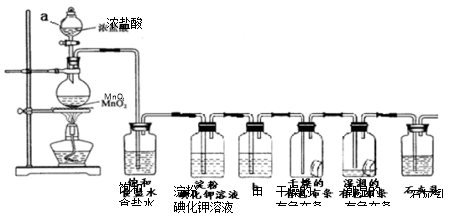
请按要求回答下列问题:
(1)淀粉碘化钾溶液中观察到的现象是_________,反应的离子方程式____________。
(2)若干燥的有色布条不褪色,湿润的有色布条褪色,则甲中盛放________(填名称)。
(3)C12与石灰乳反应制取漂白粉的化学方程式为___________________。
(4)该兴趣小组用8.7g MnO2与足量的浓盐酸制备氯气,则理论上最多可制得标准状况下的Cl2______________L。
-
某化学兴趣小组欲在实验室探究氯气的性质及模拟工业制取漂白粉,设计了如下装置进行实验:
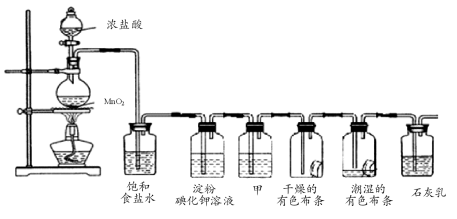
请按要求回答下列问题:
(1)浓盐酸和二氧化锰反应的化学方程式是 ,饱和的食盐水的作用是
(2)淀粉碘化钾溶液中观察到的现象是 ,反应的离子方程式为 。
(3)若干燥的有色布条不褪色,潮湿的有色布条褪色,则甲中盛放 (填名称)。
(4)C12与石灰乳反应制取漂白粉的化学方程式为 。漂白粉的有效成分是 。
(5)该兴趣小组用8.7g MnO2与足量的浓盐酸制备氯气,则理论上最多可制得标准状况下的Cl2 L。















