-
下列说法错误的是( )
A. 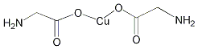 σ键和π键比例为7:1
σ键和π键比例为7:1
B. 某元素气态基态原子的逐级电离能(kJ•mol﹣1)分别为738、1451、7733、10540、13630、17995、21703,当它与氯气反应时可能生成的阳离子是X2+
C. C22﹣与O22+互为等电子体,1 mol O22+中含有的π键数目为2NA, O22+的电子式可表示为 
D. 已知反应N2O4(l)+2N2H4(l)═3N2(g)+4H2O(l),若该反应中有4 mol N﹣H键断裂,则形成的π键数目为3NA
-
下列说法错误的是( )
A. 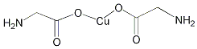 σ键和π键比例为7:1
σ键和π键比例为7:1
B. 某元素气态基态原子的逐级电离能(kJ•mol﹣1)分别为738、1451、7733、10540、13630、17995、21703,当它与氯气反应时可能生成的阳离子是X2+
C. C22﹣与O22+互为等电子体,1 mol O22+中含有的π键数目为2NA, O22+的电子式为
D. 已知反应N2O4(l)+2N2H4(l)═3N2(g)+4H2O(l),若该反应中有4 mol N﹣H键断裂,则形成的π键数目为3NA
-
下列说法不正确的是( )
A.乙烯分子中的 σ键和π键比例为 5:1
B.某元素气态基态原子的逐级电离能(kJ•mol﹣1)分别为 738、1451、7733、10540、13630、17995、21703, 当它与氯气反应时可能生成的阳离子是 X2+
C.Na、P、Cl 的电负性依次增大
D.向配合物[TiCl(H2O)5]Cl2•H2O 溶液中加入足量的 AgNO3 溶液,所有 Cl-均被完全沉淀
-
下列说法不正确的是( )
A.某金属元素气态基态原子的逐级电离能的数值分别为738、1451、7733、10540、13630、17995、21703…,当它与氯气反应时生成的阳离子是X2+
B.在[Cu(NH3)4]2+离子中,Cu2+给出孤对电子,NH3提供空轨道
C.标况下22.4LC2H2中所含的π键数和18g冰中所含的氢键数均为2mol
D.PCl5和AlCl3形成的加合物PCl5·AlCl3由[PCl4]+和[AlCl4]-构成,化合物中的阴阳离子均为正四面体构型
-
下列说法不正确的是
A.某金属元素气态基态原子的逐级电离能的数值分别为738、1451、7733、10540、13630、17995、21703…,当它与氯气反应时生成的阳离子是X3+
B. 均能一步实现
均能一步实现
C.33gCH≡C-CH=CH-CH3中所含的π键数、12g石墨中所含的碳碳键数均为1.5mol
D.灼烧白色粉末,火焰成黄色,证明原粉末中有Na+,可能含有K+
-
以下有关元素性质的说法不正确的是
A.具有下列价电子排布式的原子中,①3s23p1 ②3s23p2 ③3s23p3 ④3s23p4电负性最大的是③
B.某元素气态基态原子的逐级电离能(kJ·mol-1)分别为738、1451、7733、10540、13630、17995、21703,当它与氯气反应时可能生成的阳离子是X2+
C.①Na、K、Rb ②N、P、As ③O、S、Se ④Na、P、Cl,元素的第一电离能随原子序数增大而递增的是④
D.具有下列电子排布式的原子中,①1s22s22p63s23p2 ②1s22s22p3 ③1s22s22p2 ④1s22s22p63s23p4 原子半径最大的是①
-
已知X和Y均为第三周期元素,其原子的第一至第四电离如下表所示:下列说法正确的是
| 电离能/kJ·mol-1 | I1 | I2 | I3 | I4 |
| X | 578 | 1817 | 2745 | 11578 |
| Y | 738 | 1451 | 7733 | 10540 |
A. X通常显+3价,Y通常显+1价
B. X的第一电离能力大于Y的第一电离能
C. X、Y的最高价氧化物的水化物都不能与氢氧化钠反应
D. 工业上制取X采用的是电解熔融的X的氧化物,制取Y采取的是电解熔融的Y的氯化物
-
已知X、Y、Z为同一周期的三种元素,其原子的部分电离能(kJ·mol-1)如下表所示:
| 元素 电离能/kJ·mol-1 | X | Y | Z |
| I1 | 496 | 738 | 577 |
| I2 | 4 562 | 1 451 | 1 817 |
| I3 | 6 912 | 7 733 | 2 754 |
| I4 | 9 540 | 10 540 | 11 578 |
下列说法正确的是( )
A. 三种元素中,X元素的第一电离能最小,其电负性在同一周期元素中也最小
B. 三种元素中,Y元素的第一电离能最大,其电负性也最大
C. 等物质的量的X、Y、Z三种单质与少量盐酸反应时放出的氢气的物质的量之比为111
D. 三种单质与盐酸反应放出等量氢气时,消耗X、Y、Z的物质的量之比为321
-
已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:
| 电离能(kJ/mol) | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |

(1)某同学根据上述信息,推断B的核外电子排布如图所示,该同学所画的电子排布图违背了________。
(2)ACl2分子中A的杂化类型为________。
(3)氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料。已知金刚石中的C-C的键长为154.45pm,C60中C-C键长为145-140pm,有同学据此认为C60的熔点高于金刚石,你认为此观点是否正确________(填“正确”或“不正确”),并阐述作出判断的理由:________。
(4)科学家把C60和钾掺杂在一起制造了一种富勒烯化合物,其晶胞如图所示,该物质在低温时是一种超导体。写出基态钾原子的价电子排布式________,该物质中K原子和C60分子的个数比为________。

(5)C、Si、N原子电负性由大到小的顺序是________,NCl3分子的VSEPR模型为________。
-
已知X、Y和Z为第三周期元素,其原子的第一至第四电离能如下表:
| 电离能/kJ·mol—1 | I1 | I2 | I3 | I4 |
| X | 578 | 1817 | 2745 | 11578 |
| Y | 738 | 1451 | 7733 | 10540 |
| Z | 496 | 4562 | 6912 | 9543 |
则X、Y、Z的电负性从大到小的顺序为( )
A.Z > Y > X B.X > Z > Y C.X > Y > Z D.Y > Z > X
 σ键和π键比例为7:1
σ键和π键比例为7:1 σ键和π键比例为7:1
σ键和π键比例为7:1