碳酸钠在不同温度下可以失去部分或全部的结晶水,现有一种碳酸钠晶体(Na2CO3·nH2O)样品,可采用在不同温度下加热样品(温度逐渐升高)来测定其组成。某学生的实验流程如下,以下说法不正确的是( )

A.实验所用定量实验仪器为电子天平
B.灼烧在坩埚中进行
C.操作只在空气中进行冷却
D.流程中有恒重操作
高二化学单选题中等难度题
碳酸钠在不同温度下可以失去部分或全部的结晶水,现有一种碳酸钠晶体(Na2CO3·nH2O)样品,可采用在不同温度下加热样品(温度逐渐升高)来测定其组成。某学生的实验流程如下,以下说法不正确的是( )

A.实验所用定量实验仪器为电子天平
B.灼烧在坩埚中进行
C.操作只在空气中进行冷却
D.流程中有恒重操作
高二化学单选题中等难度题
碳酸钠在不同温度下可以失去部分或全部的结晶水,现有一种碳酸钠晶体(Na2CO3·nH2O)样品,可采用在不同温度下加热样品(温度逐渐升高)来测定其组成。某学生的实验流程如下,以下说法不正确的是( )

A.实验所用定量实验仪器为电子天平
B.灼烧在坩埚中进行
C.操作只在空气中进行冷却
D.流程中有恒重操作
高二化学单选题中等难度题查看答案及解析
碳酸钠的结晶水合物在不同温度下可以失去部分或全部的结晶水,现有一种碳酸钠晶体( Na 2CO3·nH2O )。为测定其组成,某同学在不同温度下加热样品(温度逐渐升高),实验结果记录如 下:

(1)该实验称量用的仪器是_____;实验记录中的容器是指_____(填仪器名字);冷却必须放在_____中进行(填仪器名称)。
(2)该学生停止实验的依据是_____。
(3)该样品中 n 的值为_____。(保留一位小数)
(4)若该实验过程中出现下列操作,其中可能会使实验结果 n的值偏大的是(______)
A.容器内壁原来附着有受热不分解的物质
B.碳酸钠晶体样品已有少量风化
C.加热后容器在空气中冷却
D.加热过程中有少量晶体溅出
(5)如果碳酸钠晶体样品不纯,测定结果(______)
A.没有偏差 B.一定偏小
C.一定偏大 D.无法确定
高二化学综合题中等难度题查看答案及解析
硫酸铜晶体在不同温度下可失去部分或全部结晶水甚至分解成氧化物。某学生在不同温度下给8.000 g硫酸铜晶体加热(温度逐渐升高),实验结果记录如下:
| 实验次序 | 温度(℃) | 冷却后剩余固体的质量(g) |
| 1 | 102 | 6.848 |
| 2 | 113 | 5.696 |
| 3 | 258 | 5.120 |
| 4 | 570 | 2.560 |
(1)第1次实验后,试样晶体失去结晶水的质量是_____ g。
(2)通过计算确定第二次实验后固体物质的化学式为______________。
(3)第四次实验后,剩余固体为一种黑色粉末(假设为纯净物),将该黑色粉末溶解于稀硫酸中,至少需要0.50mol/L的稀硫酸多少毫升?(写出计算过程)
高二化学实验题中等难度题查看答案及解析
硫酸铜晶体在不同温度下可失去部分或全部结晶水甚至分解成氧化物。某学生在不同温度下给8.000 g硫酸铜晶体加热(温度逐渐升高),实验结果记录如下:
| 实验次序 | 温度(℃) | 冷却后剩余固体的质量(g) |
| 1 | 102 | 6.848 |
| 2 | 113 | 5.696 |
| 3 | 258 | 5.120 |
| 4 | 570 | 2.560 |
(1)第1次实验后,试样晶体失去结晶水的质量是________g。
(2)通过计算确定第二次实验后固体物质的化学式为______________。
(3)第四次实验后,剩余固体为一种黑色粉末(假设为纯净物),将该黑色粉末溶解于稀硫酸中,至少需要0.50mol/L的稀硫酸多少毫升?(写出计算过程)
高二化学计算题困难题查看答案及解析
高二化学选择题中等难度题查看答案及解析
pg某结晶水合物A•nH2O受热失去全部结晶水,质量变为qg,由此可以知道结晶水合物的式量为( )
A.18pn/(p-q) B.18pn/p C.18 qn/p D.18qn/(p-q)
高二化学选择题中等难度题查看答案及解析
将某种碳酸钠晶体(Na2CO3 · nH2O)和碳酸氢钠的混合物11.24 g,加热到质量不再减少,剩余残渣8.48 g 。加热时产生的气体依次通过浓H2SO4和NaOH溶液后,NaOH溶液增重1.32 g(假设气体全部被吸收)。试计算:
(1)求n的值
(2)求混合物中碳酸钠晶体与碳酸氢钠的物质的量。
高二化学计算题简单题查看答案及解析
(4分)将某种碳酸钠晶体(Na2CO3 · nH2O)和碳酸氢钠的混合物11.24 g,加热到质量不再减少,剩余残渣8.48 g 。加热时产生的气体依次通过浓H2SO4和NaOH溶液后,NaOH溶液增重1.32 g(假设气体全部被吸收)。试计算:
(1)混合物中NaHCO3的质量分数为% 。
(2)混合物中碳酸钠晶体与碳酸氢钠的物质的量之比为。(写出计算过程)
高二化学计算题简单题查看答案及解析
锶(Sr)为第5周期ⅡA族元素。高纯六水氯化锶晶体(SrCl2.6H2O)具有很高的经济价值,61℃时晶体开始失去结晶水,100℃时失去全部结晶水。用工业碳酸锶粉末(含少量Ba、Fe的化合物等杂质)制备高纯六水氯化锶晶体的过程如下图所示。
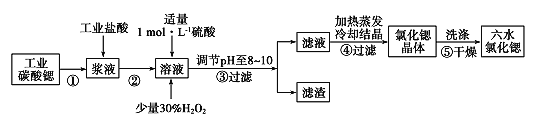
请回答:
(1)常温下,氯化锶溶液pH____7(填“大于”、“等于”或“小于”);
(2)步骤③所得滤渣的主要成分是______(填化学式),调节溶液pH至8~10,宜选用的试剂为 ______。
A.稀硫酸 B.氢氧化锶粉末 C.氢氧化钠 D.氧化锶粉末
(3)步骤⑤中,洗涤氯化锶晶体最好选用____。
A.水 B.稀硫酸 C.氢氧化钠溶液 D.氯化锶饱和溶液
(4)工业上用热风吹干六水氯化锶,选择的适宜温度范围是____(填字母)。
A.50~60℃ B.70~80℃ C.80~100℃ D.100℃以上
(5)若滤液中Ba2+浓度为1×10-6 mol/L,依据下表数据可以推算滤液中Sr2+物质的量浓度为 ________。
 .
.
高二化学工业流程中等难度题查看答案及解析
锶(Sr)为第5周期ⅡA族元素。高纯六水氯化锶晶体(SrCl2·6H2O)具有很高的经济价值,61℃时晶体开始失去结晶水,100℃时失去全部结晶水。用工业碳酸锶粉末(含少量Ba、Fe的化合物等杂质)制备高纯六水氯化锶晶体的过程如下图所示。

请回答:
(1)常温下,氯化锶溶液pH____7(已知金属性Ca<Sr)(填“大于”、“等于”或“小于”);
(2)写出在浆液中加入盐酸时主要发生的离子方程式________;
(3)步骤③所得滤渣的主要成分是______(填化学式),调节溶液pH至8~10,宜选用的试剂为 ______。
A.稀硫酸 B.氢氧化锶粉末 C.氢氧化钠 D.氧化锶粉末
(4)步骤⑤中,洗涤氯化锶晶体最好选用____。
A.水 B.稀硫酸 C.氢氧化钠溶液 D.氯化锶饱和溶液
(5)工业上用热风吹干六水氯化锶,选择的适宜温度范围是____(填字母)。
A.50~60℃ B.70~80℃ C.80~100℃ D.100℃以上
高二化学工业流程中等难度题查看答案及解析