-
(1)水下发射导弹时常采用一种火箭燃料肼(N2H4)。已知在101kPa时,32.0g液态的N2H4在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),N2H4完全燃烧的热化学方程式为_______________________。
(2)我国科学家在1973年就已经将上述反应设计成燃料电池,该燃料电池的电解质溶液是20%~30%的KOH溶液。则该燃料电池放电时:
①正极的电极反应式为_______________________。
②负极的电极反应式为_______________________。
(3)用N2H4做火箭燃料常采用N2O4做氧化剂,反应得到的产物对环境无害,则反应的化学方程式为:______________________。
高三化学填空题中等难度题查看答案及解析
-
(10分)、Ⅰ:(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在101kPa时,32.0gN2H4在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),N2H4完全燃烧反应的热化学方程式是________。
(2)肼—空气燃料电池是一种碱性燃料电池,电解质溶液是20%一30%的KOH溶液。肼—空气燃料电池放电时:正极的电极反应式是________。
Ⅱ:探究家庭制备次氯酸钠溶液的发生器如右图,原理是用石墨做电极电解饱和食盐水。
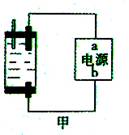
(1)若通电后,为使氯气被全部吸收,则电源的a极的名称是________。
(2)电解饱和食盐水的离子方程式为________,所得的次氯酸钠溶液中加入几滴石蕊试液,观察到的现象是 ________ ,
用离子方程式和简要文字说明理由________。
高三化学填空题中等难度题查看答案及解析
-
(10分)
1:(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在101kPa时,32.0gN2H4在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),N2H4完全燃烧反应的热化学方程式是________。
(2)肼—空气燃料电池是一种碱性燃料电池,电解质溶液是20%一30%的KOH溶液。肼—空气燃料电池放电时:正极的电极反应式是________。
Ⅱ:探究家庭制备次氯酸钠溶液的发生器如图,原理是用石墨做电极电解饱和食盐水。
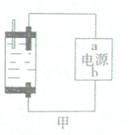
(1)若通电后,为使氯气被全部吸收,则电源的a极的名称是________。
(2)电解饱和食盐水的离子方程式为________,所得的次氯酸钠溶液中加入几滴石蕊试液,观察到的现象是 ________ ,用离子方程式和简要文字说明理由________。
高三化学填空题简单题查看答案及解析
-
(12分)(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在101kPa时,32.0gN2H4在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),N2H4完全燃烧反应的热化方程式是________。
(2)肼一空气燃料电池是一种碱性燃料电池,电解质溶液是20%—30%的 KOH溶液。
肼—空气燃料电池放电时:
正极的电极反应式是________。
负极的电极反应式是
(3)右图是一个电化学过程示意图。

①锌片上发生的电极反应是________。
②假设使用肼一空气燃料电池作为本过程中的电源,铜片的质量变化128g,则肼一空气燃料电池理论上消耗标标准状况下的空气________L(假设空气中氧气体积含量为20%)
高三化学填空题中等难度题查看答案及解析
-
(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在101kPa时,32.0gN2H4在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),N2H4完全燃烧反应的热化学方程式是 。
(2)肼—空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼—空气燃料电池放电时:正极的电极反应式是 。
负极的电极反应式是 。
(3)下图是一个电化学过程示意图。
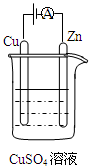
①锌片上发生的电极反应是
________ 。
②假设使用肼—空气燃料电池作为本过程中的电源,铜片的质量变化128g,则肼一空气燃料电池理论上消耗标准状况下的空气________ L(假设空气中氧气体积含量为20%)
(4)传统制备肼的方法,是以NaClO氧化NH3,制得肼的稀溶液。该反应的离子方程式
高三化学填空题中等难度题查看答案及解析
-
(10分)⑴肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在101kPa时,32.0gN2H4在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),N2H4完全燃烧反应的热化学方程式是 。
⑵肼—空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼—空气燃料电池放电时:正极的电极反应式是 。
负极的电极反应式是 。
⑶右图是一个电化学过程示意图。
① 锌片上发生的电极反应是 。

②假设使用肼—空气燃料电池作为本过程中的电源,铜片的质量变
化128g,则肼一空气燃料电池理论上消耗标准状况下的空气________ L
(假设空气中氧气体积含量为20%)
⑷传统制备肼的方法,是以NaClO氧化NH3,制得肼的稀溶液。该反
应的离子方程式 。
高三化学填空题中等难度题查看答案及解析
-
(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在101kPa时,32.0gN2H4在氧气中完全燃烧生成氮气和水,放出热量624kJ(25℃时),N2H4完全燃烧反应的热化学方程式是__________________。
(2)肼—空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼—空气燃料电池放电时:负极的电极反应式是_______________________________________ 。
(3)用CO做燃料电池电解CuSO4溶液、FeCl3和FeCl2混合液的示意图如图1所示,其中A、B、D均为石墨电极,C为铜电极.工作一段时间后,断开K,此时A、B两极上产生的气体体积相同.

①写出通入CO的电极反应式____________________________________
②乙中B极产生的气体在标准状况下的体积为_____________.
③丙装置溶液中金属阳离子的物质的量与转移电子的物质的量变化关系如图2所示,则图中③线表示的是____________(填离子符号)的变化;反应结束后,要使丙装置中金属阳离子恰好完全沉淀,需要_____________mL 8.0mol·L﹣1 NaOH溶液。
高三化学简答题困难题查看答案及解析
-
(10分)(1)肼(N2H4)又称联氨,是一种可燃性液体,可用作火箭燃料。已知在101kPa,320g N2H4在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),N2H4完全燃烧的热化学方程式是:________
(2)肼—空气燃料电池是一种碱性燃料电池,电解质溶液是20~30%的KOH溶液。肼—空气燃料电池放电时,正极的电极反应式是________;负极的电极反应式是 ________。
(3)如图是一个电化学过程示意图。假设使用肼—空气燃料电池作为本过程的电源,铜片质量变化128g,则肼—空气燃料电池理论上消耗标准状况下的空气________L(假设空气中氧气的体积含量为20%)。

(4)传统制备肼的方法是以NaClO氧化NH3制得肼的稀溶液,该反应的离子方程式是________。
高三化学填空题简单题查看答案及解析
-
氮元素能够形成多种化合物。请回答下列问题:
(1)联氨(N2H4)常温下为液态,在空气中迅速完全燃烧生成N2,同时大量放热,可作导弹、宇宙飞船、火箭的燃料。
已知:H2 (g)+1/2 O2(g) = H2O(l) △H1= —285.8kJ/mol
N2(g)+2H2(g) = N2H4(l) △H2= + 50.6kJ/mol
则N2H4(l)在空气燃烧生成液态水的热化学方程式为_______________________。
(2)利用氨气生产氢氰酸(HCN)的反应CH4(g)+NH3 (g)=HCN(g)+3H2(g) △H>0
①一定温度下,向2L恒容容器中充入1mol CH4(g)和2mol NH3(g)发生上述反应,4min达到平衡时,测得CH4平衡转化率为66.67%, 0~4min内,用H2表示的该反应速率v (H2) =___________。保持温度和容积不变,再向平衡后的容器中充入2mol NH3和2molH2,此时v正 ___v逆(选填“>”“<”或“=”)。
②平衡体系中HCN的物质的量(n) 随某物理量变化曲线如图所示(图中x、L分别表示温度或压强)。

若x为温度,则曲线,____ (选填“L1”或“L2”)能正确表示n (HCN) 与温度的关系;
若x为压强,则曲线____ (选填“L1”或“L2”)能正确表示n ( HCN)与压强的关系。
(3)NH3 能够形成Ag(NH3)2+。
已知溶液中存在Ag+ (aq)+2NH3 (aq)==Ag( NH3)2+(aq ),常温下该反应平衡常数K1=1.10×107,反应AgCl (s)+2NH3 (aq)
Ag( NH3)2+(aq) +Cl-(aq)的化学平衡常数K2=1.936×10-3,则Ksp(AgCl)=____________。
(4)硫氧化物和氮氧化物是常见的大气污染物,利用如图所示装置(电极均为惰性电极)可吸收SO2,并用阴极排出的溶液吸收NO2。
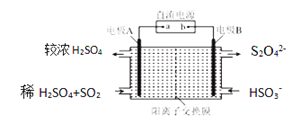
①电极A的电极反应式为__________________________________。
②在碱性条件下,用阴极排出的溶液吸收NO2,使其转化为无害气体,同时有SO32-生成。该反应离子方程式为________________________________。
高三化学综合题中等难度题查看答案及解析
-
氮元素能够形成多种化合物。请回答下列问题:
(1)联氨(N2H4)常温下为液态,在空气中迅速完全燃烧生成N2,同时放出大量热,可作导弹、宇宙飞船、火箭的燃料。
已知:H2(g)+1/2O2(g)==H2O(l);△H1=-285.8kJ/mol
N2(g)+2H2(g)=N2H4(l);△H2=+50.6kJ/mol
则N2H4(l)在空气燃烧生成液态水的热化学方程式为_____________。
(2)工业上利用氨气生产氢氰酸(HCN)的反应为CH4(g)+NH3(g)
HCN(g)+3H2(g) △H>0。
①一定温度下,向2L恒容容器中充入1mol CH4(g)和2mol NH3(g)发生上述反应,4min达到平衡时,测得CH4的转化率为66.67%。0~4min內,用H2表示的该反应速率v(H2)=_____。
保持温度和容积不变,再句平衡后的容器中充入2molNH3和2molH2,此时v正___v逆(选填“>”“<”或“=”)。
②平衡体系中HCN的物质的量(n)随某物理量变化曲线如图所示(图中x、L分别表示温度或压强)。

若x为温度,则曲线,____(选填“L1”或“L2”)能正确表示n (HCN) 与温度的关系;
若x为压强,则曲线____(选填“L1”或“L2”)能正确表示n HCN)与压强的关系。
(3)NH3能够形成Ag(NH3)2+。
①溶液中存在Ag+ (aq)+2NH3 (aq)==Ag( NH3)2+(aq )时,其平衡常数的表达式为K稳=_______。
②常温下,K稳[Ag(NH3)2+]=1.10×107,反应AgCl (s)+2NH3 (aq)
Ag( NH3)2+(aq) +Cl-(aq)的化学平衡常数K=1.936×10-3,则Ksp(AgCl)=_____。
(4)硫氧化物和氮氧化物是常见的大气污染物,利用如图所示发置(电极均为惰性电极)可吸收SO2,并用阴极排出的溶液吸收NO2。

①电极A的电极反应式为______________。
②在碱性条件下,用阴极排出的溶液吸收NO2,使其转化为无害气体。同时有SO32-生成。该反应离子方程式为______________。
高三化学综合题中等难度题查看答案及解析