-
我国的四大发明之一黑火药,爆炸时发生反应的化学方程式为:S + 2KNO3 + 3C → K2S + 3CO2↑+ N2↑。请根据其中所含的元素回答下列问题:
(1)如图所示为元素周期表中钾元素框图,数据“39.10”表示的是________;钾元素在周期表中的位置为___________________。

(2)上述元素中,简单离子电子层结构与氩原子相同,且离子半径最大的元素,其原子核外有_____种不同能级的电子;已知其氧化物中一种对应水化物能与氯单质反应,该反应的化学方程式是__________________________________。
(3)上述反应生成物中,属于非电解质的是_________________(写结构式);其中熔点最高的物质的电子式是______________。
(4)上述化学方程式的元素中,属于同周期元素的非金属性由强到弱的顺序为_______________,能证明其递变规律的事实是_______________(填字母)。
A、最高价氧化物对应水化物的酸性 B、气态氢化物的沸点
C、单质与氢气反应的难易程度 D、其两两组合形成的化合物中元素的化合价
(5)上述反应中,如1.5mol还原剂________(填“得到”或“失去”)________ mol电子,则生成_________ g还原产物。
-
黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为为:S(s) + 2KNO3(s) + 3C(s) == K2S(s) + N2(g) + 3CO2(g) ΔH= x kJ·mol-1 。已知碳的燃烧热ΔH1 = a kJ·mol-1;S(s) + 2K(s) == K2S(s); ΔH2= b kJ·mol-1;2K(s) + N2(g)+3O2(g)==2KNO3(s); ΔH3= c kJ·mol-1 。则x为( )
A.3a+b-c B.c +3a-b C.a+b-c D.c+a-b
-
黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为:
S(s) + 2KNO3(s) + 3C(s) = K2S(s) + N2(g) + 3CO2(g) ΔH= x kJ•mol-1
已知硫的燃烧热 ΔH1= a kJ•mol-1
S(s) + 2K(s) = K2S(s) ΔH2= b kJ•mol-1
2K(s) + N2(g) + 3O2(g) = 2KNO3(s) ΔH3= c kJ•mol-1,则x为
A.3a + b - c B.c + 3a - b
C.a + b - c D.c + a - b
-
黑火药是中国四大发明之一,其爆炸的化学反应方程式是:
2KNO3 + 3C + S→ + N2↑ + 3CO2↑
+ N2↑ + 3CO2↑
(1)方程式中第二周期元素中非金属性由强到弱的顺序依次为________。
(2)上述元素中,元素原子最外层有2个未成对电子的是________。
(3)在生成物中:A物质的晶体类型为________;构成晶体A的微粒半径大小关系为________(用微粒符号表示);含极性共价键的非极性分子为________。
(4)已知CN—与N2结构相似,写出HCN分子的结构式________。
-
“一硫二硝三木炭”描述的是我国四大发明之一的黑火药配方,黑火药爆炸时发生的反应为S+2KNO3+3C  K2S+N2↑+3CO2↑,对于该反应说法不正确的是
K2S+N2↑+3CO2↑,对于该反应说法不正确的是
A. 氧化产物是CO2
B. 爆炸的原因是反应释放大量热,并生成大量气体
C. 反应中有三种元素的化合价发生变化
D. 氧化剂与还原剂的物质的量之比为1:3
-
(物质结构与性质)黑火药是我国古代的四大发明之一。黑火药爆炸时发生的反应为:
2KNO3+S+3C=K2S+N2↑+3CO2↑。回答下列问题:
(1)基态钾原子的核外电子排布式为____________,第一电离能:K____________(填“>”或“<”)Na。
(2)NO3-的空间构型为_____________。
(3)固态硫易溶于CS2,熔点为112℃,沸点为444.8℃。其分子结构为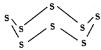 ,S8中硫原子的杂化轨道类型是____________,S8分子中至多有________个硫原子处于同一平面。
,S8中硫原子的杂化轨道类型是____________,S8分子中至多有________个硫原子处于同一平面。
(4)N2分子中σ键与π键的个数比为___________,,N2的沸点比CO的沸点__________(填“高”或“低”)。
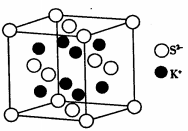
(5)K2S的晶胞结构如图所示。其中K+的配位数为_____________,S2-的配位数为__________;若晶胞中距离最近的两个S2-核间距为acm,则K2S晶体的密度为__________g·cm-3(列出计算式,不必计算出结果)。
-
20世纪前,黑火药是世界上唯一的火箭推进剂,黑火药爆炸的化学方程式为:S + 2KNO3 +3C = K2S +N2↑ +3CO2↑。20世纪60年代,火箭使用的是液体推进剂,常用的氧化剂有四氧化二氮、液氧等,可燃物有肼(N2 H4)、液氢等。
(1)K原子核外电子云有___种不同的伸展方向,电子填充了__个轨道;写出硫原子的核外电子排布式__,比较反应所涉及的原子的原子半径大小:__;
(2)写出产物中含极性键的非极性分子的结构式__,产物K2S的电子式为___;
(3)已知S和氯水反应会生成两种强酸,其离子方程式为_______;
(4)以上的火箭推进剂一般含有氮元素,含氮化合物种类丰富。有一含氮化合物,具有很强的爆炸性,86g该化合物爆炸分解会生成标况下N267. 2L和另一种气体单质H2。写出其爆炸的化学方程式____。
-
黑火药是我国古代的四大发明之一。黑火药爆炸时发生的反应为:2KNO3+S+3C=K2S+N2↑+3CO2↑。回答下列问题:
(1)基态钾原子的核外电子排布式为____________,第一电离能:K______ (填“>”或“<”)Na。
(2)NO3-的空间构型为_____________。
(3)固态硫易溶于CS2,熔点为112℃,沸点为444.8℃。其分子结构为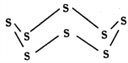 ,S8中硫原子的杂化轨道类型是____________,S8分子中至多有________个硫原子处于同一平面。
,S8中硫原子的杂化轨道类型是____________,S8分子中至多有________个硫原子处于同一平面。
(4)N2分子中σ键与π键的个数比为________,N2的沸点比CO的沸点____(填“高”或“低”)。
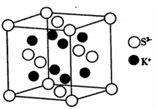
(5)K2S的晶胞结构如图所示。其中K+的配位数为_______,S2-的配位数为____;若晶胞中距离最近的两个S2-核间距为a cm,则K2S晶体的密度为____g·cm-3(列出计算式,不必计算出结果)。
-
火药制备是我国古代闻名世界的化学工艺,原理为 2KNO3+S+3C=K2S+N2↑+ 3CO2 ↑。下列表示反应中相关微粒的化学用语正确的是
A.K+的结构示意图: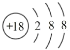 B.K2S 的电子式:
B.K2S 的电子式:
C.CO2 的结构式为:O=C=O D.16O2与 18O3 互为同位素
-
我国的四大发明之一黑火药, 爆炸时的主要反应是:S +2KNO3 +3C=K2S +3CO2↑+N2↑,下列说法不正确的是
A. 每生成 0.5 mol N2, 反应中转移 6 mol 电子
B. 硝酸钾、 硫磺在黑火药爆炸的反应中是氧化剂
C. KNO3 有强氧化性, 乘坐汽车、 火车、 飞机时不能随身携带
D. 上述反应的生成物都是无毒的, 所以燃放爆竹时不会污染环境
 ,S8中硫原子的杂化轨道类型是____________,S8分子中至多有________个硫原子处于同一平面。
,S8中硫原子的杂化轨道类型是____________,S8分子中至多有________个硫原子处于同一平面。
 ,S8中硫原子的杂化轨道类型是____________,S8分子中至多有________个硫原子处于同一平面。
,S8中硫原子的杂化轨道类型是____________,S8分子中至多有________个硫原子处于同一平面。
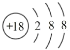 B.K2S 的电子式:
B.K2S 的电子式: